支气管哮喘的发病机制有哪些原因?

中医学认为, 哮喘属于中医哮病范畴, 痰阻气道、气机失调为本病的基本病机。现代医学认为TH1/TH2类细胞因子失衡、细胞因子、基质金属蛋白酶 (matrix metalloproteinase, MMP) 及其组织抑制剂 (tissue inhibitor of metalloprotein-ase, TIMP) 、遗传学因素、神经调节等在哮喘的发生发展过程中起着重要作用。
1 支气管哮喘中医病因病机
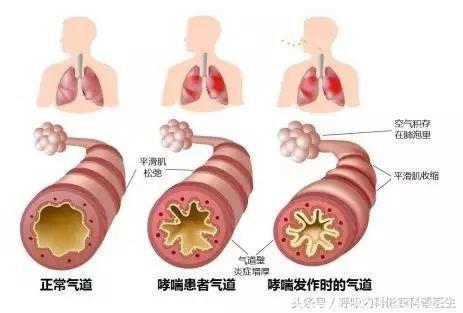
哮喘的病机痰实为哮喘的主要病理基础, 是哮喘发作的中心环节。痰邪内伏则阻滞气机, 气机郁滞则津血运行失畅而生痰留瘀;瘀血阻滞, 血脉壅塞则又可导致气机不利, 津液凝滞生痰。一旦外邪侵袭而触动, 则气逆而喘, 哮喘顿作。外邪之中, 风邪首当其冲, 或有风寒或有风热。若长期发作, 伤及肺肾, 则可从实转虚, 表现肺肾脏气虚弱之候。故痰阻气道、气机失调为本病的基本病机。
哮喘属于“哮证”范畴, 中医对哮喘病因病机主要有宿根论 (邪气内伏说、寒邪和痰饮内伏说、气滞和痰饮内伏说、先天禀赋异常说、素患哮喘未愈说、发展宿根说) 、外邪论、情志劳役论、正虚论等学说。核心就是风、火、寒、痰、瘀、虚数端, 即风邪外袭、火邪致病、寒邪为患、痰邪伏肺、瘀血阻滞、虚为根本。哮喘病机为气血痰的异常, 肺脾肾三脏受累, 而肝与痰的生成、瘀血的产生及气之升降出入失常关系密切, 由此揭示了哮喘与肝的关系。
2 现代医学对哮喘发病机制的认识
2.1 树突状细胞 (DC) 在哮喘发病中的作用
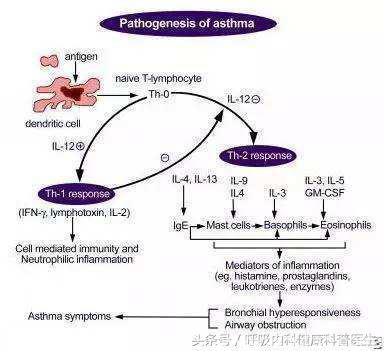
树突状细胞 (Dendritic Cell, DC) 在哮喘发病中起着重要作用。有研究认为分布于气道防线上的DC与吸入的变应原相遇, 参与始动免疫球蛋白Ig E的合成, 然后DC迁移至引流淋巴结, 并在此提呈抗原给T或B细胞。也有研究认为DC参与辅助性T细胞的分化, DC的类型甚至成熟状态在决定TH0细胞向TH1或TH2细胞方向分化过程中起着关键作用。与巨噬细胞产生的白细胞介素-18 (Interleukin-18, IL-18) 一起, DC产生的高水平IL-12在干扰素-γ (Interferon-γ, IFN-γ) 条件下可促使TH0细胞向TH1分化, 而低水平的IL-12在IL-4条件下可促使TH0细胞向TH2分化。DC参与免疫耐受和对微生物基序的识别, 而且通过诱导Treg抑制细胞免疫。
2.2 嗜酸性粒细胞 (EOS) 在哮喘发病中的作用
哮喘患者血清、痰液、鼻腔分泌物、支气管肺泡灌洗液和支气管黏膜活检组织中嗜酸粒细胞水平显著增高, 并与病情的严重程度呈正相关, 随着有效的抗炎治疗而下降。血清单核细胞趋化因子蛋白水平与肺功能之间存在着相关性, 其与气道阻塞程度呈正相关。
嗜酸性粒细胞 (Eosinophil, EOS) 被激活后能释放许多介质和细胞因子, 包括脂类介质、氧自由基、白三烯、白细胞介素、粒细胞-巨噬细胞集落刺激因子等, 参与炎症反应, 并释放具有细胞毒性的蛋白质颗粒, 如嗜酸性细胞阳离子蛋白、嗜酸性细胞神经毒素、嗜酸性细胞过氧化物酶以及主要碱基蛋白等, 这些毒性蛋白颗粒引起气道上皮损伤, 使气道上皮剥离和气道高反应性。
2.3 T淋巴细胞在哮喘发病中的作用
2.3.1 CD4+CD+25调节性T细胞在哮喘发生中的作用
T淋巴细胞在体内的变化将影响到TH1/TH2的平衡, 即CD4+、CD+25调节性T细胞的减少将会导致机体免疫功能紊乱, 从而诱导哮喘的发生, CD4+CD+25调节性T细胞对实验性哮喘小鼠有保护作用。但其作用机制还不十分清楚。
CDC+D+25调节性T细胞是维持机体免疫耐受的重要调控者, 既能抑制TH1细胞, 也能抑制TH2细胞, 还能抑制CD8+T细胞。CD4+CD+25调节性T细胞能够抑制TH1的应答反应, 却能促进TH2的极化, 在TH2细胞分化之前, 去除CD4+CD+25T淋巴细胞, 将显著降低IL-4、IL-5、IL-13 m RNA和蛋白质的表达,。
2.3.2 CD8+T细胞在哮喘发病中的作用
在抗原刺激下, CD8+T细胞可增殖并产生相似TH1和TH2样的细胞因子, 称为Tcl/Tc2。CD8+T细胞对过敏原诱导的Ig E产生气道嗜酸性粒细胞浸润和气道高反应性, 具有抑制性保护作用。由于Tcl在体外抗原刺激下产生大量IFN-γ, 刺激树突细胞产生IL-12, 提示CD8+T细胞通过组织局部微环境调节树突细胞成熟并影响TH2极化。
2.4 细胞因子在哮喘发病中的作用
2.4.1 TH1/TH2类细胞因子失衡在哮喘发病中的作用
TH1/TH2细胞平衡失调, 机体正常的免疫耐受功能受损, 从而导致免疫细胞及其成分对机体自身组织结构和功能的破坏, 是哮喘发病的重要基础。这其中TH2优势是变应性哮喘形成及进展的关键性机制, 哮喘的表型是由TH1/TH2比例关系趋于TH2占优势。TH1占优势时, 感染局限, 预后良好;TH2占优势时, 感染扩散, 预后不良。哮喘发病时, TH1型免疫反应减弱, TH2型免疫反应则异常增强, 可见, TH2细胞的异常增高在哮喘发病机制中尤为重要。
TH2细胞促进B细胞产生大量Ig E (包括抗原特异性Ig E) 和分泌炎症性细胞因子 (包括黏附分子) , 刺激其他细胞 (上皮细胞、内皮细胞、嗜碱细胞、肥大细胞和嗜酸性细胞等) 产生一系列炎症介素 (如白三烯、内皮素、前列腺素和血栓素A2等), 这些化学活性介质达到一定浓度即可使支气管平滑肌挛缩, 毛细血管扩张, 通透性增高, 腺体分泌增多最终诱发速发型 (Ig E增高) 变态反应和慢性气道炎症。
2.4.2 白细胞介素 (IL)
影响支气管哮喘的白细胞介素有很多种, 现在就其中几种主要的进行论述。
IL-4:由TH0细胞产生, 诱导TH0细胞向TH2细胞转化, 并刺激TH2细胞产生IL-4。另外IL-4可促进B细胞增殖并诱导其分化为浆细胞, 产生Ig E、Ig G4, 促进肥大细胞的增殖和分化, 参与哮喘变应性炎症的发生与发展。
IL-5:诱导嗜酸性粒细胞具有特异性, 主要调节嗜酸性粒细胞生长、分化及其活性的细胞因子, CD4+T淋巴细胞趋化到支气管黏膜后产生的IL-5能选择性作用于嗜酸性粒细胞。
IL-6:血管内皮细胞及炎细胞有直接激活和毒性作用,参与哮喘发病机制考虑与以下因素有关: (1) 作用于B淋巴细胞的分化阶段, 产生抗体分泌细胞; (2) 诱导T淋巴细胞分化, 进而激活T细胞, 间接调节B细胞成熟, 使Ig E分泌增高。
IL-10:主要对支气管哮喘气道炎症发展的以下几个关键环节起负调节作用。 (1) 抑制抗原提呈; (2) 诱导T细胞不应答; (3) 直接抑制哮喘患者气道主要炎性细胞。IL-10可显著增加T细胞介导的单核细胞向抑制性巨噬细胞分化, 而抑制小型巨噬细胞减少与支气管哮喘发病有关。
IL-13:通过以下途径在哮喘发病机制中起作用: (1) 调节血管黏附因子表达, 从而促进嗜酸性粒细胞气道浸润; (2) 促TH2类细胞因子表达; (3) 促进B淋巴细胞由产生Ig G、Ig M向产生Ig E转化, 提高Ig E水平。IL-13在支气管迟发型哮喘反应和气道变应性炎症的发生和发展中起重要作用。
2.4.3 肿瘤坏死因子-α (TNF-α)
TNF-α主要由单核巨噬细胞产生, 低水平的TNF-α在组织修复、炎症应答中起作用, 对机体有利;高水平的TNF-α慢性刺激和释放可引起组织免疫病理损伤及炎症介质的瀑布样连锁反应, 最终引起气道痉挛, 使血管通透性增加、微血栓形成、气道黏膜水肿等, 从而导致哮喘发作。另外TNF-α可通过转录因子 (AP-1) 而引起一些与炎性反应有关的细胞因子、受体、酶的基因表达, 引起气道上皮细胞脱落, 诱发或加重哮喘。重度过敏性支气管哮喘的TNF-α水平高于轻、中度患者, TNF-α水平越高, 病情越重。
2.4.4 转化生长因子β1 (TGF-β1)
TGF-β1对免疫功能起抑制作用, 可抑制新鲜分离的T细胞产生IL-4和IFN-γ。由于TGF-β1干预多种免疫细胞的分化和功能, 因而推测其可能对Treg的分化也具有调节作用。TGF-β1还可以影响NK细胞的增殖分化, 干扰B细胞的Ig转换, 通过干预IL-2、IFN-γ的合成而起到免疫抑制作用。TGF-β1除了通过调控Smad3表达, 影响CD4+和CD8+T细胞分化外, 还可通过抑制T-bet和GATA-3表达, 阻断TH1和TH2细胞的分化。
2.5 基质金属蛋白酶 (MMP) 及其组织抑制剂 (TIMP)
气道重塑时, 肺组织内有多种细胞及其分泌的细胞因子参与。其中, 肺泡巨噬细胞 (Alveolar Macrophage, AM) 被认为启动并维持迟发相气道变应性炎症。 MMP-9对气道有炎性破坏作用, 而TIMP-1对气道有修复、重塑作用, 两者在肺组织中的过度表达可能通过气道重塑而导致肺泡壁及小气道破坏, 引起肺泡壁弹性降低, 小气道狭窄、阻塞、塌陷, 导致阻塞性通气功能障碍。
2.6 遗传学因素在哮喘发病中的作用
现在很多专家学者认为哮喘的发病受遗传因素的影响, 渴望能找到“哮喘基因”, 但是基因与支气管哮喘的具体关系尚未搞清楚。
用全基因关联法研究了与哮喘有关的基因发现ORMDL3基因是迄今为止发现的与哮喘关联最有充分证据的基因, 并绘制出单核苷酸多态性 (Single Nucleotide Polymorphisms, SNPs) 与儿童哮喘患病的关系图谱。
2.7 神经调节机制
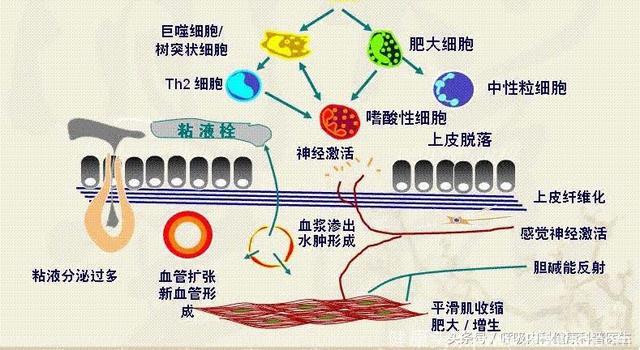
目前针对支气管哮喘在神经调节机制方面的研究比较少。有研究认为气道上皮下有致密的感觉神经纤维, 环境的变化刺激神经肽物质P等释放, 引起支气管收缩、黏液过度分泌等。呼吸道合胞病毒感染促进神经生长因子和营养因子受体的大量表达, 导致感觉神经分布和反应性的变化, 加速炎症反应。
【济南哮喘病医院温馨提醒】点击下方了解更多,获取更多疾病用药知识和免费治疗指导方案!
