专家视角丨王立峰教授:逆向探究CheckMate 078——肿瘤免疫治疗NSCLC东西方人群的PK/PD相似
导读
亚洲肺癌患者和西方肺癌患者在发病率、组织学分型、基因突变上存在一定差异,而且东西方肺癌人群对化疗、靶向药物的反应及副作用也存在不同。然而在前不久AACR大会上公布的CheckMate 078研究却未发现东西方人群在免疫治疗非小细胞肺癌(NSCLC)的疗效和安全性上的差异性。医脉通特意邀请了南京鼓楼医院王立峰教授撰稿,从东西方人群的PK/PD方向来探究肿瘤免疫治疗NSCLC东西方人群疗效及安全性无明显差别的原因。

王立峰 教授
主任医师,副教授,医学博士,硕士研究生导师
南京鼓楼医院肿瘤中心主任医师;肺癌亚专科带头人
美国梅奥医院、德国莱比锡圣乔治医院及意大利锡耶纳LE SCOTTE医院癌症免疫治疗中心临床访问医生、高访学者
南京市卫生青年人才
承担及参与多项国家、省、市级科研项目,先后于近年获得南京市卫生局新技术引进一等奖、中国抗癌协会科技二等奖、江苏省科技进步二等奖、中华医学科技二等奖、江苏省医学科技二等奖等奖项
主攻肺癌的多学科诊治及个体化诊断与治疗
亚洲肺癌患者和西方肺癌患者存在差异。首先,我国是全球肺癌第一大国,发病率远超西方国家。而且我国肺癌患者在组织学类型上也与西方国家不同。再者,肺癌的基因突变在不同人种间的差异很大:例如,欧美国家肺腺癌患者中EGFR突变率只有10-17%,但在亚洲患者中则达到了30%-65%;相反,KRAS突变在西方高加索人群中的检出率为35%-50%,但在中国患者中的检出率不高,有报道称低于5%[1]或者不超过10%[2-4]。最后,亚洲人种对化疗、靶向药物的反应及副作用与欧美人群存在差异:例如,IDEAL1研究结果显示,日裔患者皮疹、腹泻发生率较非日裔患者高,还有资料显示,日本患者的间质性肺病发生率为1.6%,明显高于非日本患者(0.3%)[5]。这些差异有些是因为肺癌筛查范围不广、治疗策略不同、对患者疾病分子分型的检测差异造成的,有些则可能是因为人种、基因的不同造成对药物敏感性的差别。
近年来,免疫治疗发展迅速,延长了肺癌患者的生存时间,将肺癌治疗推进了免疫治疗的新时代,而且东西方人群对免疫治疗非小细胞肺癌(NSCLC)的疗效和安全性上也并未像化疗、靶向治疗一样表现出差异性。
2018年AACR会议公布了Ⅲ期研究CheckMate 078(图1)的部分研究成果,这是首个针对亚洲人群免疫治疗NSCLC的研究,共纳入中国患者451例,俄罗斯患者45例,新加坡患者8例。CheckMate 078研究不仅证实了在中国人群中nivolumab二线治疗NSCLC的疗效和安全性明显优于多西他赛。还将其与CheckMate 017/057研究的一致性作为了研究终点,这三项研究纳入的东西方人群的基线特征不同,但对照CheckMate 017/057研究西方人群的疗效、安全性数据,我们可以看出,CheckMate 078的疗效、安全性数据与CheckMate 017/057研究的数据相似,提示了nivolumab在东西方人群中疗效(图2)、安全性的一致性。
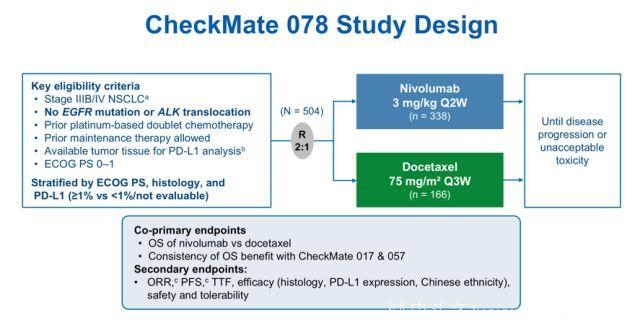
图1. CheckMate 078研究设计

图2. CheckMate 078研究与CheckMate 017/057研究的OS获益
那免疫治疗NSCLC未产生东西方人群差异性的原因是什么呢?我们知道,要考察某一药物对特定人群的疗效和安全性,先要了解药物在该人群中的药代动力学/药效学(PK/PD)特征。PK与PD是药理学研究的两个重要方面,前者探讨药物进入机体后的命运,即药物的吸收、分布、代谢与排泄规律;后者研究药物作用机制与效能。药物发挥药理作用,必须作用于机体特定部位(如受体、酶),这种特异结合的强度与持续时间和药物性质及浓度有关,PK过程影响药效发挥,PK与PD是相互关联的两个方面[6]。
药动学和药效学之间的定量关系称为PK/PD参数。与抗肿瘤药物有关的主要PK/PD参数包括:峰浓度(Cmax)、血药浓度—时间曲线下面积(AUC)、达峰时间(Tmax)、生物利用度、清除率(CL)、表观分布容积(Vd)、半衰期(tl/2)等。药物的PK/PD相关参数能够指示药物体内代谢途径、毒副作用的靶器官、给药间隔及剂量、疗效强弱等。例如:Cmax可以体现药物的吸收程度;AUC与抗肿瘤药物的疗效和毒性有关;生物利用度是评价药物制剂质量的重要指标,也是选择给药途径的依据之一;对于抗肿瘤药物而言,Vd越大可能其抗瘤的疗效越强,它还可以指导药物剂量的调整;tl/2可以反映机体消除药物的能力和消除药物的快慢程度。除此之外,还可根据PK/PD参数进行种属间推定,基于小鼠的PK/PD模型建立并计算人类中的PK/PD参数,为临床试验提供有价值的数据。PK/PD研究及应用还是新药上市申报的关键步骤[7],在健康志愿者样本中进行的药代动力学研究,可对药物临床的基本特性做出最初的描述,估计药物安全剂量、人体对新药的耐受程度等,为下一步效力作用研究提供基础。需要指出的是,在美国,动物体内开展的临床前药效/药理/安全性评价、PK/PD分析和预测、以及药物在人群中开展的安全性评价的临床试验是每个药品上市前的重要环节。
药物的疗效、安全性与PK/PD密切相关,PK/PD的差异也可能会引起疗效和副作用的区别。而已经有研究发现,免疫治疗NSCLC东西方人群的PK/PD无明显差异。
在2017年CSCO大会上公开的CheckMate 077研究队列A[8],考察了Nivolumab在中国患者的药代动力学指标,研究纳入9例NSCLC和6例鼻咽癌患者,接受Nivolumab 3mg/kg Q2W治疗。其中8名患者接受了Nivolumab初始剂量评估期的治疗,7名患者接受了序贯队列扩展期治疗。在第1周期和第3周期的第1,2,3,5,8天收集患者血浆样本进行药代动力学研究。中国人群的中位有效半衰期为566小时(约24天),第1周期和第3周期的Cmax分别为57.0μg/mL和132μg/mL,Tmax分别为4h和8h,对比西方患者的结果显示,中国人群中的药代动力学指标(Cmax、AUCtau)和既往美国开展的CA209-003研究类似(图3)。
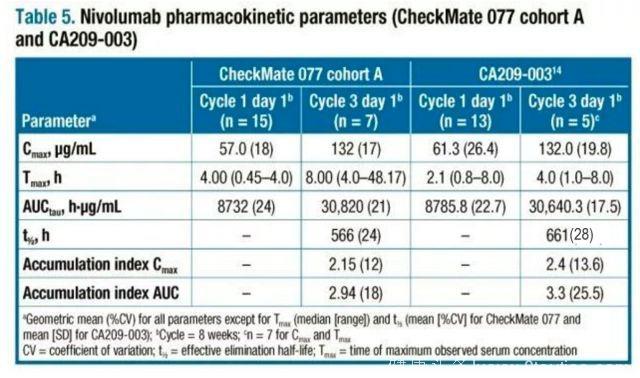
图3. 中国人群研究中的Cmax和AUCtau结果与CA209-003研究类似
在日本晚期实体瘤(包含5例肺腺癌)患者中开展的Nivolumab临床Ⅰ期试验分析了药代动力学数据[9]。17位患者给药剂量分别为1mg/kg(n=3)、3 mg/kg(n=5)、10 mg/kg(n=6)、20mg/kg(n=3)。该研究也未发现日本人群与西方人群的PK特征存在显著差异[10]。
LEE11等也将韩国晚期实体瘤(包括NSCLC)应用Nivolumab的药代动力学、安全性与之前美国、日本类似临床试验进行了比较。患者接受单剂量的Nivolumab(1、3、10 mg/kg),随访3周。符合要求的患者继续给予之前的剂量,每两周一次。每个剂量组纳入6名患者(n=18)。结果显示,Nivolumab的平均消除半衰期为15.0-19.1天,血药浓度-时间曲线特征和安全性指标与之前的研究类似,同样证实,韩国、日本、美国的药代动力学指标无明显差异(图4)。
所以,免疫治疗NSCLC未表现出东西方人群的差异性,可能与免疫治疗NSCLC东西方人群的PK/PD相似有关。
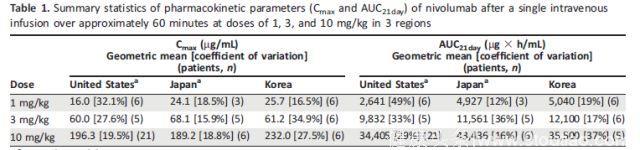
图4. 韩国、日本、美国人群的Nivolumab药代动力学指标相似
总体来说,在肺癌的诊断和治疗中,需要关注患者人群/人种、抽烟状态、性别、生存环境、疾病组织类型、分子靶点分型等的差异,从而制定相对有效的针对性治疗,同时在治疗过程中还要定期监测突变,关注并及时发现耐药性的产生与否,合理调整治疗方案,为肺癌患者带来最大的生存希望;由于肿瘤免疫治疗药物Nivolumab治疗东、西方NSCLC患者的PK/PD特征、疗效、安全性等相似,提示免疫检查点抑制剂药物治疗NSCLC的机制可能具有普适性。因此,合理使用此类抗体能够增强疗效;同时,我们也有理由相信,技术的进步能够进一步推动对肿瘤治疗药物的机制探索,从而指导癌症的个性化用药,推动精准治疗的长足发展。
参考文献:
1. Fang B, Mehran RJ, Heymach JV,et al. Predictive biomarkers in precision medicine and drug development against lung cancer. Chin J Cancer. 2015 Jul 2;34(7):295-309.
2. 张卉,杨新杰,秦娜,等.肺腺癌EGFR与KRAS基因突变状态分析.中国肺癌杂志.2015;11(18):686-690.
3. 高洁,陈佳琦,张力,等. 中国非小细胞肺癌患者表皮生长因子受体和KRAS基因突变与预后的相关性.中华病理学杂志, 2012;41 (10):652-656.
4. 杨宁,郭妹,宋玉兰,等. 430例中国非小细胞肺癌患者EGFR、KRAS、BRAF和PIK3CA基因突变状态及其临床意义.中国肿瘤生物治疗杂志.2015;22 (6):734-739.
5. 陆舜,李子明.肺癌分子靶向治疗-来自亚洲的数据.中国临床肿瘤学大会.2006.
6. Craig WA.Pharmacokinetics/pharmacodynamies parameters:Rationale for antibacterial dosing of mice and men.Clin Infect Dis.1997,26:1.
7. 申华琼,何亚将. 药代动力学在药物申报中的应用.中国临床药理学杂志.2015;31(9):758-761.
8. 2017CSCO.poster.
9. Yamamoto N, Nokihara H, Yamada Y, et al.Phase I study of Nivolumab, an anti-PD-1 antibody, in patients with malignant solid tumors.Invest New Drugs. 2017 Apr;35(2)207-216.
10. Wong AC, Ma B. An update on the pharmacodynamics, pharmacokinetics, safety and clinical efficacy of nivolumab in the treatment of solid cancers. Expert Opin Drug Metab Toxicol. 2016 Oct;12(10):1255-61.
11. Phase I Pharmacokinetic Study of Nivolumab in Korean Patients with Advanced Solid Tumors. The Oncologist 2018; 23: 155-e17.
1.专家访谈丨焦顺昌教授:免疫治疗的特征——应答持久
2.专家访谈 | 白冲教授:鳞状NSCLC二线治疗新标准
3.专家视角丨史美祺教授: CheckMate 078——亚洲人群对IO治疗的安全性与西方人群相似