NEJM研究确认根除幽门螺杆菌能预防异时性胃癌
胃癌的早期发现和治疗对于降低胃癌死亡率具有重要意义。日本、韩国由于广泛开展胃内窥镜筛查使早期胃癌诊断率达到50-70%[1],5年生存率提高到70-80%[2]。早期胃癌治疗以内镜下切除和外科手术为主。然而,临床研究发现在早期胃癌切除后仍有部分患者在胃内其它部位发生新的胃癌,也称为异时性胃癌(metachronous gastric cancer),其原因是胃癌患者胃黏膜多伴有癌前病变发生,因此在切除胃癌后其它部位的癌前病变仍有演变成胃癌的可能。
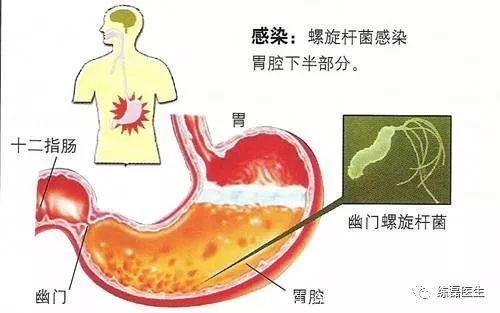
幽门螺杆菌(H. pylori)感染是胃癌发生的重要危险因素,世界卫生组织(WHO)将H.pylori定为I类致癌因子[3]。研究证实,H. pylori感染引起的炎症反应可使胃黏膜发生萎缩、肠上皮化生、异型增生,导致感染人群胃癌发生的几率明显高于非感染人群[4-5]。根除H. pylori感染能有效预防胃癌,使干预人群胃癌发病风险降低39%[6],但是否可以预防异时性胃癌的发生尚无定论。
本期《新英格兰医学杂志》韩国学者发表了一项根除H. pylori感染对早期胃癌切除后异时性胃癌预防作用的随机、双盲、单中心干预研究[7],结果显示根除H. pylori对异时性胃癌的预防具有积极作用。该研究选取了396名经过胃内窥镜切除的早期胃癌患者,采用随机、双盲方法,将其分为抗H.pylori治疗组和安慰剂对照组,经过平均5.9 年的随访观察,比较异时性胃癌发生以及胃黏膜萎缩程度的改变。研究显示,治疗组194例患者中有14例发生了异时性胃癌(7.2%), 显著低于安慰剂组的13.4%(27/202), 风险比(HR)为0.5(95% CI,0.26-0.94)。进一步对H. pylori根除者与未根除者和安慰剂组进行比较,HR为0.32 (95% CI,0.15-0.66)。此外,治疗组有48.4%的患者胃体小弯胃黏膜萎缩程度明显改善,显著高于安慰剂组的15%(P<0.001)。
既往关于根除H. pylori感染是否可以预防异时性胃癌的发生,研究结果不一致[8]。该项研究基于随机、双盲的研究设计,较好地避免了偏倚和混杂因素,研究实行统一评价标准和质量控制,提高了结果的可信度,研究结果对胃癌的防治、特别是异时性胃癌的预防具有很好的借鉴和引领作用。但由于异时性胃癌发生概率低,仍需要更大样本的随机、双盲、多中心研究加以验证。
中国、日本、韩国为胃癌高发国家,仅在中国每年新发胃癌病例约为67.9万[9],占全世界新发胃癌病例的40%以上。中国政府十分重视胃癌的防治,在国家重大公共卫生专项农村癌症早诊早治项目的资助下,在全国部分地区、部分人群中进行了上消化道癌的内窥镜筛查。胃癌筛查自2008年开始,由最初的2个项目点扩大到2017年的188个,每年筛查人数也由2008年的3000人增至2017年的20.75万人。胃癌检出率近年在1.46%左右,早期胃癌占70%左右,其中80-90%患者进行了治疗。韩国学者的这项研究值得我们在早诊早治项目和临床实践中借鉴,应加强对筛查和临床中发现的大量早期胃癌患者手术后进行抗H. pylori治疗,预防异时性胃癌的发生,指导临床实践。
胃癌防治任重道远,其中一级及二级预防是降低胃癌发病率和死亡率的根本途径。今年中国政府工作报告中又一次强调重视对癌症的预防,我们要进一步加强研究和实践,在更大规模的人群中建立包括胃癌在内的癌症预防体系,达到“健康中国2030”中提出降低重大慢性疾病死亡率的长远目标。
参考文献
[1] Sugano K. Screening of gastric cancer in Asia. Best Pract Res Clin Gastroenterol 2015;29:895-905.
[2] Jung KW, Won YJ, Kong HJ, Oh CM, Seo HG, Lee JS. Cancer statistics in Korea: incidence, mortality, survival and prevalence in 2010. Cancer Res Treat 2013;45:1-14.[3] Schistosomes, liver flukes and Helicobacter pylori: IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, Lyon, 7-14 June 1994. IARC MonogrEval Carcinog Risks Hum 1994;61:1-241.
[4] Nomura A, Stemmermann GN, Chyou P-H, Kato I, Perez-Perez GI, Blaser MJ.Helicobacter pylori infection and gastric carcinoma among Japanese Americans in Hawaii. N Engl J Med 1991; 325: 1132-1136.
[5] Parsonnet J, Friedman GD, Vandersteen DP, et al. Helicobacter pylori infection and the risk of gastric carcinoma. N Engl J Med1991; 325:1127-31.
[6] Ma JL, Zhang L, Brown LM, et al.Fifteen-year effects of Helicobacter pylori, garlic, and vitamintreatments on gastric cancer incidence and mortality. J Natl Cancer Inst 2012;104:488-92.
[7] Choi IJ,Kook MC, Kim YI, et al. Helicobacter pylori Therapy for the Prevention of Metachronous Gastric Cancer. N Engl J Med 2018;378:1085-95.
[8] Lee YC, Chiang TH, Chou CK, et al. Association between Helicobacter pylorieradication and gastric cancer incidence: a systematic review and meta-analysis. Gastroenterology 2016;150:1113-1124.e5.
[9] Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015. CA Cancer J Clin. 2016;66:115-32.