结合1例新冠肺炎合并高血压患者病例,探讨ACEI药物的使用!
几天前笔者发表文章“新冠病毒感染的高血压患者,应停用ACEI类降压药物”受到了广泛关注。近些天,有同行对此持不同意见,甚至有人说新冠病毒感染的高血压患者应该用ACEI类药物。
笔者对上述观点不赞同,一个在新冠肺炎中有争议的降压药,为什么要在病人感染期数十天内必须使用,是没有其他替代药物?(一线降压药5大类),还是有证据认为应用有益?
今天,笔者结合近期会诊的一个新冠状病毒感染性肺炎的重症病例,进一步探讨新冠肺炎合并高血压患者停用ACEI药物的理由,目的是给临床一线治疗预警及提供一些新的思考。
介绍一下这个病例:
这是一个53岁女性患者,1月22日左右出现发热,到医院就诊,确诊为“新冠肺炎”,患者既往高血压多年,长期服用“钙拮抗剂、ACEI”药物。
感染早期,患者一般情况尚可,血压控制理想,血常规:大致正常。生化全项:胆固醇略高。
感染第7天左右患者逐渐出现了病情恶化:在100%纯氧吸入的情况下,血氧分压53%,乳酸酸中毒,血压95/45mmHg(多巴胺维持中),白细胞2万多,C反应蛋白高出20多倍,降钙素原正常。CK:4310IU/L,
CKMB:210IU/L,乳酸脱氢酶明显增高。肝衰竭、肾衰竭、急性ARDS、全身炎性反应综合征等,当时请会诊目的是明确是否存在病毒性心肌炎、是否需要生命支持。
由于该医院不能检测肌钙蛋白,患者CKMB/CB不超过6%,不支持心肌损伤,所以我认为不能确诊病毒性心肌炎或心肌损伤,CK、CKMB、乳酸脱氢酶增高可能为骨骼肌损伤、肝脏等其他脏器损伤所致。但患者严重ARDS,在100%纯氧吸入的情况下,血氧分压53%,所以给予了患者ECMO治疗,目前仍在治疗中。
总结该例患者:1、患者高血压长期服用ACEI,并持续应用至发病第3天,后出现休克停用。2、该患者出现ARDS、全身炎性反应、多脏器衰竭,未见明显心肌损害。
支持使用ACEI类降压药物的观点如下:
1、新冠病毒结合ACE2进入肺细胞内,ACE2表达减少。
2、ACE2减少,激活RAS系统导致肺损伤。
3、要抑制激活的 RAS系统所以应该应用ACEI。
而笔者提醒大家对于新冠肺炎应谨慎使用ACEI的观点如下:1、目前研究已证实新冠病毒感染的途径为结合ACE2入侵肺细胞,并劫持表达ACE2细胞,上调细胞内众多病毒复制、转染基因,导致病毒感染能力大幅升高。而ACE2主要表达的细胞为II型肺泡上皮细胞(83%)。当前现有的研究只能确定病毒感染途径。2、持相反观点的同仁认为病毒结合后ACE2下调,激活RAS系统激活,过度刺激AT1受体,导致肺血管通透性增加,从而引起肺损伤加重,此机制来源于SARS-Cov病毒肺炎的研究,而不是新冠病毒肺炎,两者是否有同样作用机制,目前没有数据证实。从笔者的这例病例中不难看出,随着病情进展,患者白细胞、C反应蛋白明显增高,降钙素原正常,这提示发生了炎症反应综合征而非继发感染。推测病毒感染后,机体出现了强免疫反应,巨噬细胞等免疫细胞吞噬病毒结合细胞(II型肺泡上皮细胞),造成严重肺损伤,这也与肺CT表现相符,感染一般为肺的外带、末梢、肺泡部位(图1。新冠病毒CT表现)。如果是RAS系统反射激活导致肺损伤,应该是肺的整体、多段损伤,而不是局部(图2.SARS肺炎CT表现)。另外,如果真是反射RAS激活导致肺损伤,应用ACEI应该损伤明显减轻, 目前来看对于新冠病毒肺炎仍然没有特效药,且上述肺炎患者前期应用ACEI也没能阻止病情进展。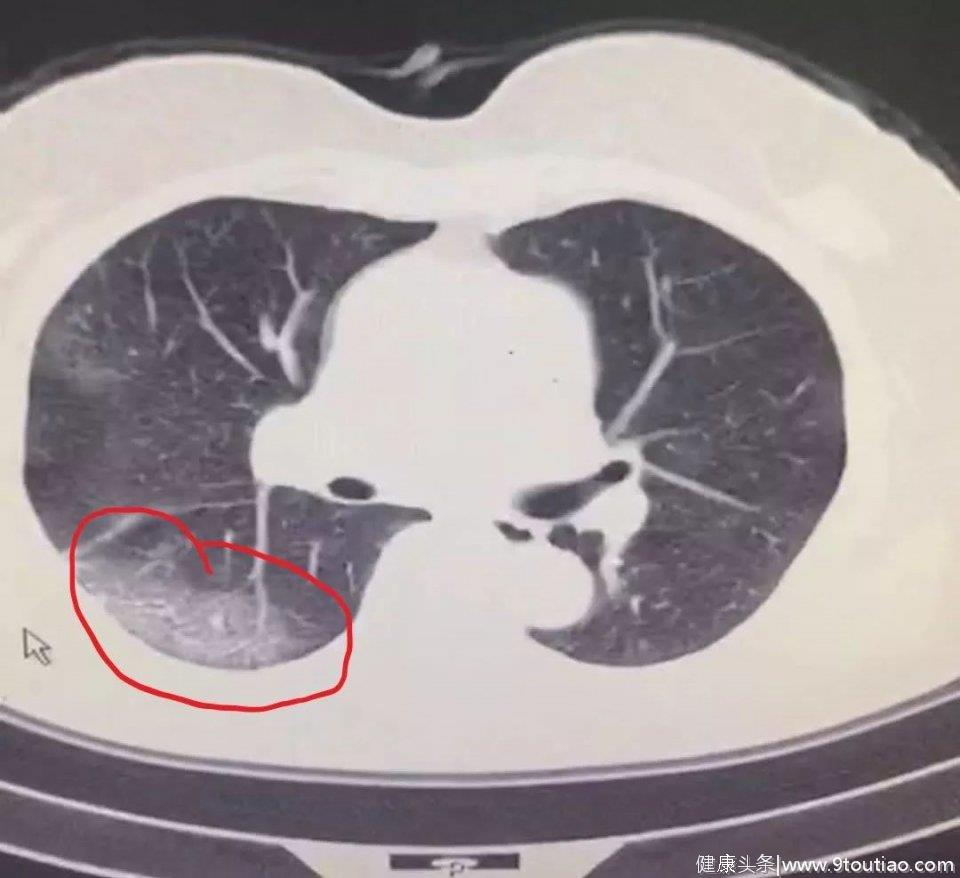 (图1、新冠病毒肺炎CT表现)
(图1、新冠病毒肺炎CT表现)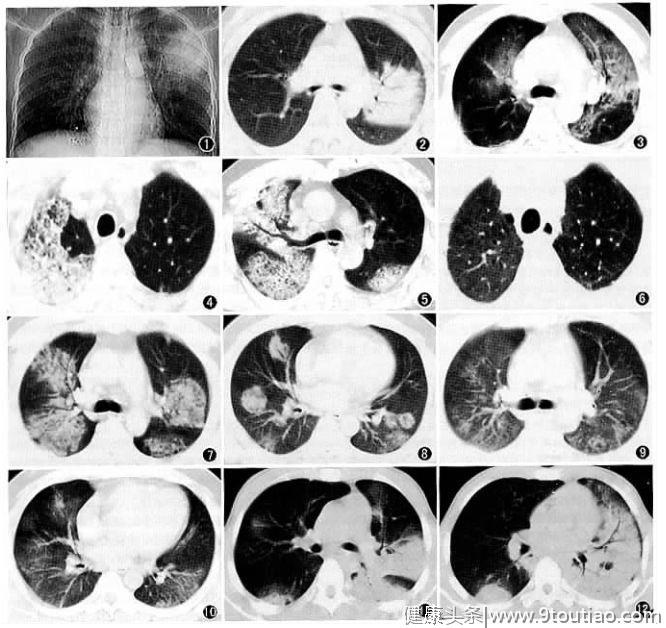
3、Ferrario等发表在Circulation研究显示[1],给大鼠应用ACEI类药物(赖诺普利)后血压下降的同时,ACE2水平增高了4.7倍。所以应用ACEI有升高ACE2的风险,从而导致病毒更容易入侵细胞。
4、2018年发表的一篇论文,回顾性分析了539例病毒性肺炎患者,结果发现入院前给予ACEI和他汀类药物,不能降低病毒性肺炎(非新型冠状病毒肺炎)患者的死亡率及插管率。很可能结果也会出现在新冠肺炎中。

[1]Carlos M. Ferrario,et al. Effect of Angiotensin-Converting Enzyme Inhibition and Angiotensin II Receptor Blockers on Cardiac Angiotensin-Converting Enzyme2.Circulation.Vol. 111, No. 20.
[2].图2来源:唐秉航.中华放射学杂志 2003.37(8):698-700.