拨云见日 突出重围——2型糖尿病合并肥胖或超重患者体重管理探讨【糖话心语第七期】

北京市第三区卫健委提醒糖胖患者:
治疗千万条,减重第一条。
方案不规范,体重两行泪。
本文仅限医疗专业人士阅读

追本溯源 研精究微:探寻肥胖影响T2DM的机制
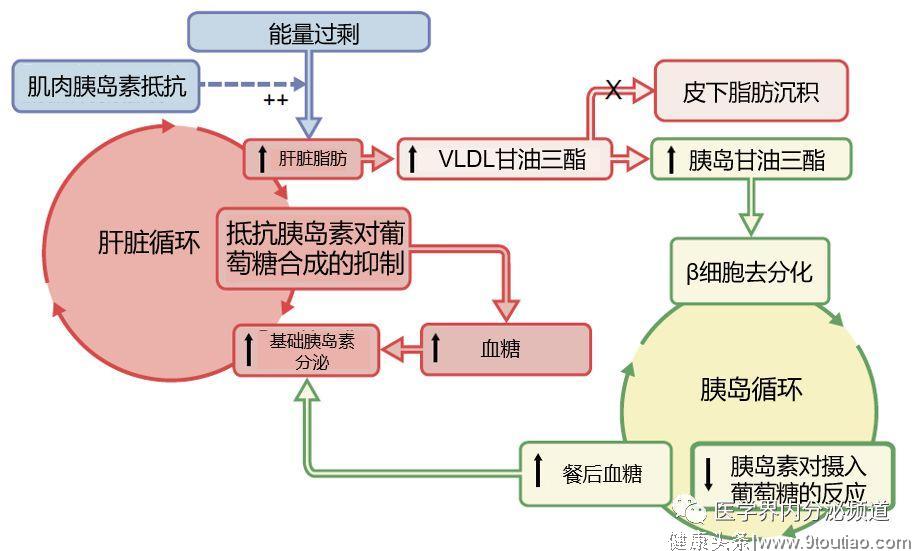
表1 T2DM合并超重和肥胖的治疗选择
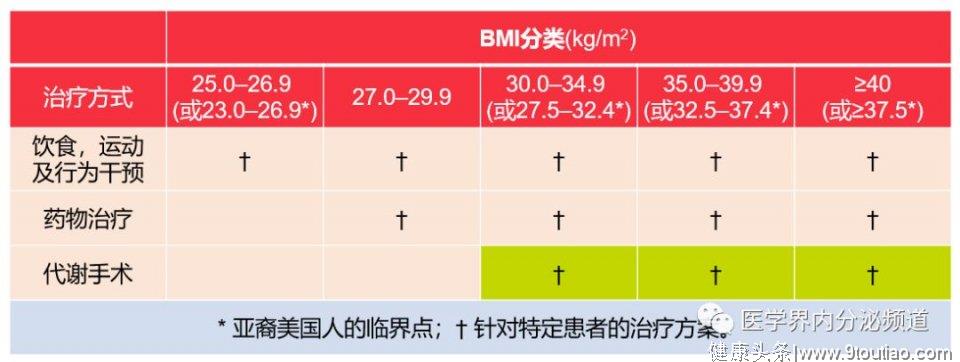
一、生活方式干预
(1)个体化饮食
不同的饮食干预食谱通过限制不同的宏量营养素(碳水化合物、脂肪、蛋白质)减少个体的能量摄入。虽然饮食干预的方式很多,但Meta分析表明不同类型饮食干预对患者的体重影响相似8,9。指南亦推荐,只要能限制相同的热量,各种饮食方式的减重效果都同样有效,可根据患者的健康状况、依从性等选择适合的饮食方式。10,11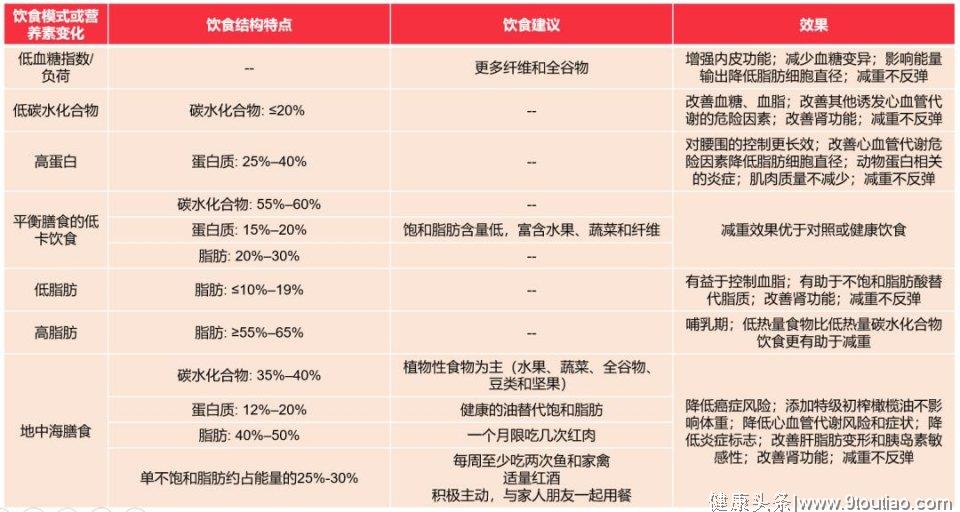
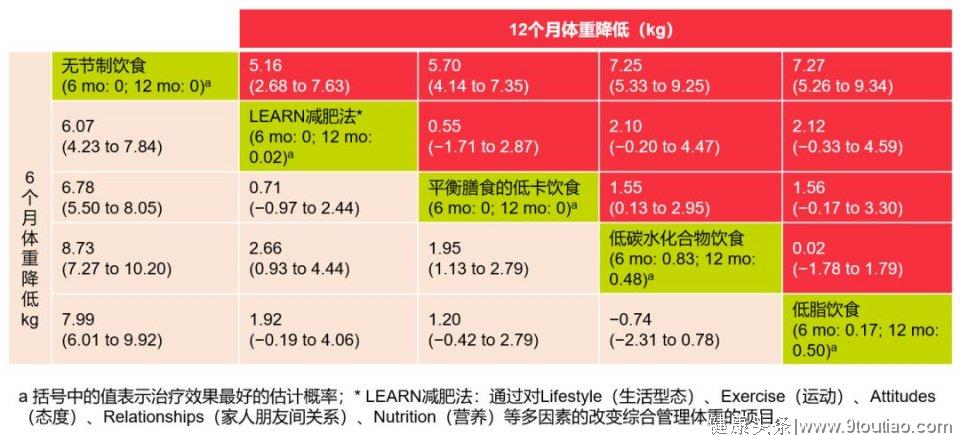
(2)运动治疗
合理运动可改善胰岛素敏感性、改善代谢紊乱。成年T2DM患者每周进行至少150min 中等强度(50%-70%最大心率,运动时有点用力,心跳和呼吸加快但不急促)有氧运动12;对于T2DM合并肥胖的患者,每周应参加中等强度的体力活动200-300min(如快节奏舞蹈,有氧健身操,慢跑,游泳等)(3)行为治疗
行为干预措施可以帮助增加超重或肥胖T2DM患者对于限制饮食、增加体力活动的依从性。具体包括:自我监测体重、食物摄入和体育运动;制定明确且合理的目标;进行肥胖、营养和体育运动的相关教育;与病友面对面或小组交流;刺激控制法;系统化解决问题的处理方法;减少压力;调整认识法,如认知行为治疗、动机性访谈;行为约束;心理咨询;社会支持机构的动员等14。二、药物治疗
对于T2DM患者,仅通过生活方式干预可能无法达到设定的减重及血糖目标。因此,药物治疗也是非常重要的改善代谢的治疗手段。
(1)降糖药物:量与质并存
遵从此原则,应尽量避免使用增加体重的噻唑烷二酮类、磺脲类,格列奈类以及胰岛素;可考虑使用对体重呈中性的DPP-4i或α-糖苷酶抑制剂(中性或降低);以及具有不同程度降低体重效应的二甲双胍(中性或轻度降低)、SGLT-2i以及GLP-1 RA15表4常用降糖药物对血糖、体重及内脏脂肪的作用
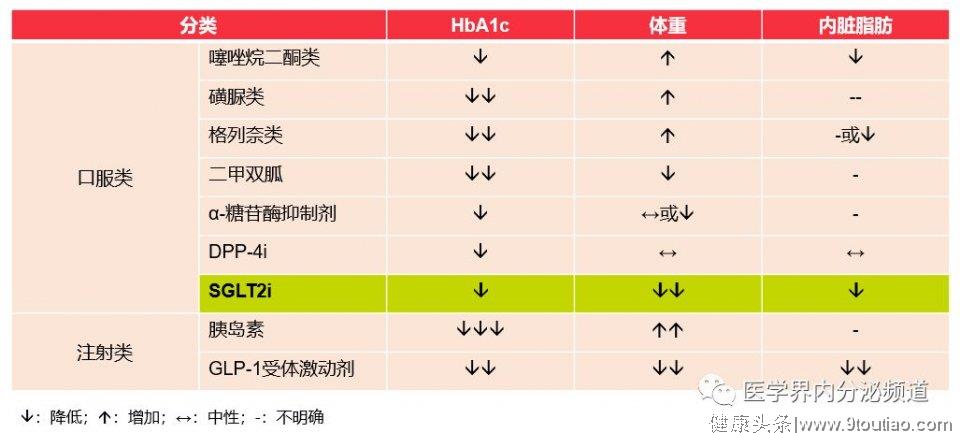
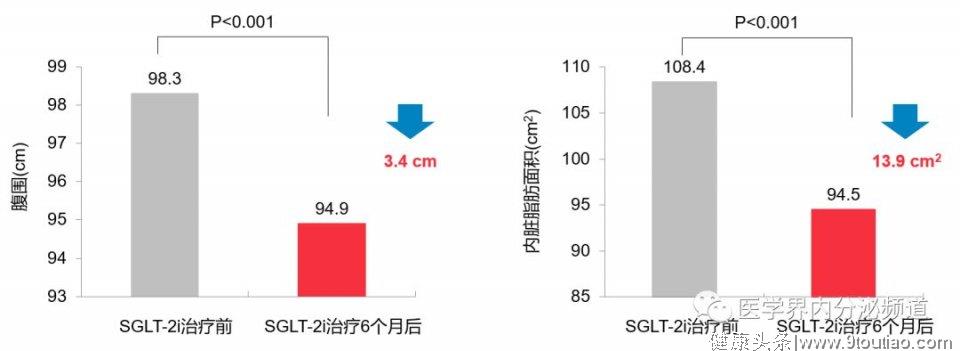
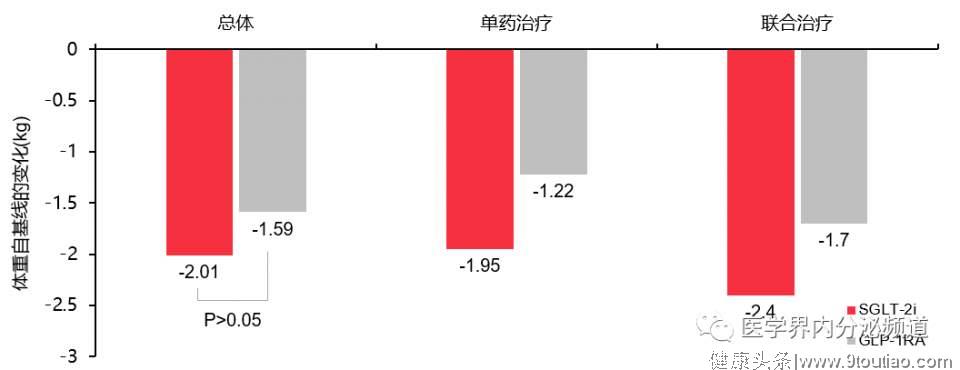

综上,以减重需求为首要考虑的T2DM患者可优选SGLT-2i或GLP-1RA治疗。
(2)减重药物:选择获FDA批准的减重药物
目前,FDA批准6种减重药物用于BMI≥27 kg/m28表5 FDA批准的减重药物:在T2DM合并肥胖患者中的减重和降糖效果8,24-29
三、手术治疗:遵从手术指征
合并肥胖的T2DM患者,如经生活方式和药物干预均不理想,ADA及中国2型糖尿病指南建议此类患者可考虑进行减重手术治疗。
2019年ADA指出对于BMI>40 kg/m2(亚裔美国人BMI>37.5 kg/m2)的成人2型糖尿病患者(无论血糖水平和降糖药物如何)以及BMI 35.0-39.9 kg/m2(亚裔美国人BMI 32.5-37.4 kg/m2)的成人T2DM患者,如通过生活方式和药物治疗血糖仍然控制不佳建议代谢手术。
对于BMI 30.0-34.9 kg/m2(亚裔美国人BMI 27.5-32.4 kg/m2)且通过口服或注射药物治疗(包括胰岛素)血糖仍然控制不佳者,可考虑代谢手术。
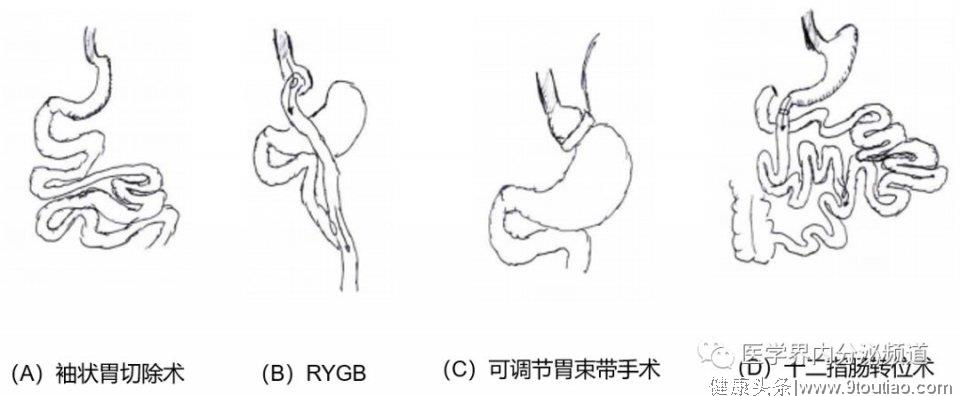
综上所述,无论生活方式干预、药物治疗,亦是代谢手术治疗,均是为了应对呈快速上升趋势的T2DM合并肥胖患者的体重管理。患者可根据自身情况,选择合适的方案,改善及提高生活质量。相信未来也会有更多解决方案,共同抗击这场全球性的公共卫生问题,在减重的道路上一往无前。
[本文仅限医疗专业人士阅读]
参考文献
1. Tian Y,et al. Lancet Diabetes Endocrinol. 2016 Jun;4(6):487-97.
2. Darlene McNaughton, et al. Crit Public Health. 2013 Sep; 23(3): 274–288.
3. Zhou XH, et al. Plos One. 2016, 11(1):e0144179
4. Diabesity - 21st Century Pandemic, We are Still Fighting
5.https://www.healio.com/endocrinology/obesity/news/in-thejournals/%7Bb8a35e07-1d4c-4b42-a52fbe1ab0530a39%7D/increasing-bmi-raises-risks-for-type-2-diabetes-cad
6. Adela Hruby, et al. Pharmacoeconomics. 2015 Jul; 33(7): 673–689.
7. Taylor R, et al. Diabetologia. 2018 Feb;61(2):273-283.
8. Diabetes Care. 2019 Jan;42(Suppl 1):S1-S2.
9. Johnston BC, et al. JAMA. 2014 Sep 3;312(9):923-33.
10. Garvey WT, et al. Endocr Pract. 2016 Jul;22 Suppl 3:1-203.
11. Bray GA, et al. Endocr Rev. 2018 Apr 1;39(2):79-132.
12. 中华医学会糖尿病学分会. 中华糖尿病杂志,2018,10(1) :4-67.
13. AACE. Endocr Pract. 2016 May 24.
14. 陈璐璐. 中国2型糖尿病合并肥胖综合管理专家共识[J]. 糖尿病天地(临床), 2016, 13(10):11-12.
15. JAMES F,et al.Diabetes Care 32:650–657, 2009
16. Taylor R, et al. Diabet Med. 2013 Mar;30(3):267-75.
17. Tchernof A, et al. Physiol Rev. 2013 Jan;93(1):359-404.
18. Neeland IJ, et al. Circulation. 2018 Mar 27;137(13):1391-1406.
19. Tosaki T, et al. Intern Med. 2017;56(6):597-604.
20. Cai X,et al.J Diabetes Investig. 2017 Jul;8(4)_510-517
21. 肖新华. 新诊断超重或肥胖且HbA1c>9%的2型糖尿病患者首选肠促胰素类药物[J]. 医学与哲学, 2015(4):15-18.
22. Cai X,et al.J Diabetes Investig. 2017 Jul;8(4)_510-517.
23. Pereira MJ, et al. Drugs. 2019 Jan 30. doi: 10.1007/s40265-019-1057-0. [Epub ahead of print]
24. 李宁, 牛军平, 陈彬彬, et al. 口服治疗肥胖药物——纳曲酮/安非他酮缓释片[J]. 临床药物治疗杂志, 2016, 14(2):84-88.
25. 秦健, 邹寿涛. 减肥新药——复方苯丁胺/托吡酯缓释剂[J]. 中国药房, 2015, 26(35):5033-5035.
26. 郑宗基, 关美萍, 薛耀明. 新型减肥药盐酸氯卡色林的机制及临床应用[J]. 转化医学电子杂志, 2014(3):168-170.
27. 刘国荣. 是否有能够降低BMI的有效、可行且便宜的药物?[J]. 药品评价, 2010(1):38-38.
28. Franz MJ.Diabetes Spectr. 2017 Aug;30(3):149-153.
29. Mehmet Mihmanli, et al. Springerplus. 2016; 5: 497.
30. Bhasker AG, et al. Obes Surg. 2015 Jul;25(7):1191-7.
31. Adriana Florinela Cătoi, et al. Obes Facts. 2015 Dec; 8(6): 350–363.
32. Donnelly JE, et al. Med Sci Sports Exerc. 2009 Feb;41(2):459-71.