造福癌症患者的免疫疗法
复杂多变的癌症严重地威胁着人们的健康,人类近千年来与之持续搏斗着。回顾征程,人类从抗癌战争发展到现在,出现了三次大革命:第一次是针对癌细胞毒性的放化疗治疗,第二次是针对基因突变的靶向治疗,而近些年进行的第三次革命是针对免疫系统的免疫疗法。2016年初,美国政府已启动攻克癌症的“登月计划”,投入大量资源,主攻的也是免疫疗法。研究表明,患者自身免疫功能低下或失调,是恶性肿瘤之所以发生并扩展的重要原因。因此,提高免疫力,激活免疫系统是癌症治疗过程中亘古不变的真理。与第一代的放化疗和第二代的靶向治疗相比,免疫疗法从免疫系统入手,针对的是免疫细胞而不是癌细胞,目的在于激活免疫系统,让它去抑制癌细胞。免疫疗法的出现,第一次让人们看到了把多数癌症变成慢性病的希望。
免疫疗法指的是利用免疫系统来治疗疾病的方法,总体来说是一个较大的治疗体系。例如,发展抗病毒疫苗、HPV病毒、HSV病毒抗体培养等等。19世纪下半叶,法国生物学家路易·巴斯德在研究治疗鸡的霍乱病时发现,通过把病鸡上的霍乱弧菌减弱其活性制成的减弱疫苗,可以使鸡对霍乱病产生主动免疫力。后来他用同样的方法,先后在1881年和1885年制成了抗炭疽病的减弱疫苗和抗狂犬病毒疫苗。这些就是世界上最早出现的免疫疗法,由于其疗效显著,巴斯德被誉为“细菌斗士”。
1890年,德国微生物学家冯·贝林和在德国工作的日本微生物学家北里柴三郎研制成功抗白喉毒素血清和抗破伤风毒素血清。在20世纪,免疫疗法又有新的进展,特别是卡介苗的发明,有效地预防了结核病。近几年来,科研人员利用免疫疗法在尖锐湿疣、生殖器疱疹等疾病上利用自身感染组织培养抗体,在医学界引起了轰动。
激活人体自身免疫系统来对抗癌症,是一个存在了上千年的猜想。从理论上说,免疫药物相对别的药物来说有三大优势:一是不直接损伤,反而增强免疫系统;二是同一种药物可以治疗多种癌症,对很多患者都会有效;三是可以抑制癌细胞进化,降低复发率。
2016年,随着新技术革命的到来,癌症治疗出现了有史以来的第三次革命。科研人员研究出两种肿瘤免疫治疗方法,通过不同的途径来加强T细胞的威力。T细胞是T淋巴细胞的简称,来源于骨髓的多能干细胞(胚胎期则来源于卵黄囊和肝)。在人体胚胎期和初生期,骨髓中的一部分多能干细胞或前T细胞迁移到胸腺内,在胸腺激素的诱导下分化成熟,成为具有免疫活性的T细胞。成熟的T细胞经血流分布至外周免疫器官的胸腺依赖区定居,并且可以经过淋巴管、外周血和组织液等进行再循环,发挥细胞免疫及免疫调节等功能。T细胞的再循环有利于广泛接触进入体内的抗原物质,加强免疫应答,较长期保持免疫记忆。T细胞的细胞膜上有许多不同的标志,主要是表面抗原和表面受体,这些表面标志都是结合在细胞膜上的巨蛋白分子。作为抗击肿瘤细胞的先锋,T细胞能够在肿瘤细胞表面打孔,再把一些特定的酶通过孔道注入癌细胞,最终将癌细胞整个消灭。
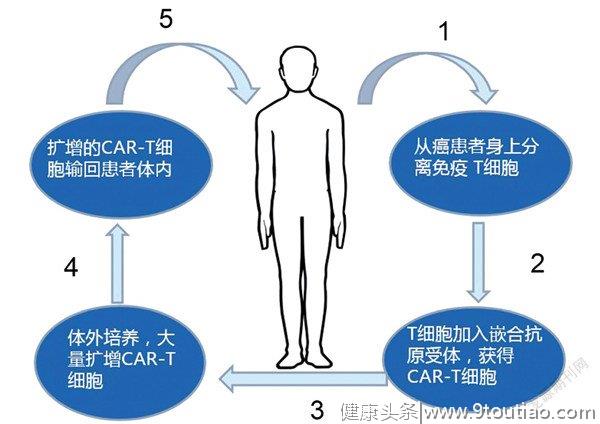
两种免疫治疗法T细胞的改造使用是第一种肿瘤免疫治疗方法,主要有以下6个步骤:1.将癌症患者的免疫T细胞从外周血中分离出来,在体外培养。2.利用基因工程技术给T细胞加入一个能识别肿瘤的细胞,并且同时激活T细胞杀死肿瘤细胞的嵌合抗体。T细胞变成CAR-T细胞后,不再是一个普通的T细胞,能同时承担识别、锁定、杀伤癌细胞这些任务,提升效率,增强威力。3.CAR-T细胞在体外大量增殖,一般一个癌症患者需要几十亿,乃至上百亿个CAR-T细胞。患者体型越大,需要的细胞就越多。4.在T细胞回输之前,对患者进行化疗预处理。5.把扩增好的CAR-T细胞注射回患者体内,进而对表达这些抗原的癌细胞进行攻击。6.严密监护患者,尤其是控制住前几天身体出现的剧烈反应。这种方法用于治疗白血病这样的血液肿瘤效果显著,接受治疗的患者中90%没有出现复发。
这种肿瘤免疫治疗方法用于临床才两年左右时间,对一些特定的癌症患者展示出了一定的效果。但目前它还处于临床试验的阶段,是不是能彻底治愈癌症现在下结论还为时太早。而且CAR-T也不是完美的,病人接受这种疗法有巨大的临床风险。由于CAR-T杀癌细胞实在是太快太有效了,能够瞬间在局部产生出超大量的细胞因子,引起惊人的免疫反应,这就是细胞因子风暴。临床表现是病人高烧不退,如果不控制好,很有可能就救不过来了。当然现在临床上经验已经丰富了很多,对细胞因子风暴有了提前准备,它带来的风险也都完全可以被控制住。
作为CAR-T疗法的先驱,卡尔·琼教授1999年来到美國费城的宾夕法尼亚大学进行癌症研究。2009年,宾夕法尼亚大学批准卡尔·琼研究团队启动表达抗-CD19嵌合抗原受体(CAR-T19)的自体T细胞治疗的试验性临床研究。在2017年3月公布的数据中,美国食品药品监督管理局(FDA)宣布他们一共收到了105份CAR-T的调查性新药申请。这意味着未来将有更多的临床试验,势必会推动这项疗法持续开展。卡尔·琼博士将改造后的T细胞称为“连环杀手”,仅一个改造后的T细胞就可以杀死10万个癌细胞。
CAR-T疗法的出现给癌症的治疗带来了新的曙光,随着越来越多的企业加入到这一领域的研发以及相关产业政策的利好,未来这一技术的发展成果将造福于广大的患者,并为人类最终战胜癌症提供强有力的支持。以CAR-T为代表的免疫细胞治疗技术,在2013年被《科学》杂志评为“十大科技突破”之首。
CAR-T无疑是肿瘤临床治疗的利器,然而制备过程却相当繁琐,从取血到最终回输给患者可能需要长达数周的时间。于是,科学家设想能否直接在体内操作T细胞,使它获得足够的功能。美国西雅图弗雷德·哈金森癌症研究中心的研究人员最近就开发了一种基于纳米技术的体内CAR-T制备方案,使得CAR-T制备的过程大大简化。其工作原理如下:纳米颗粒通过靶向分子找到T细胞,并携带内部包载的DNA一起进入T细胞;接着DNA在T细胞内释放,并转录翻译成蛋白质,使T细胞被改造成具有针对肿瘤的CAR结构;最后普通的T细胞就在体内被改造成了临床治疗所需的CAR-T细胞。实验结果表明,连续注射5天纳米颗粒后,动物体内的CAR-T细胞数量就开始急速增加,并高效识别杀死肿瘤细胞。随后CAR-T细胞逐渐凋亡,效应消失,大大缓解了严重的副作用。
CAR-T细胞疗法在血液癌的治疗中已经取得惊人的效果,尤其是针对B细胞型急性淋巴细胞白血病患者的初期缓解率可以达到90%左右。国际上第一批尝试免疫疗法的晚期黑色素瘤患者中,已经有人存活了15年。目前,研究人员正在积极设计开发新型的CAR-T疗法,期望在其他血液肿瘤以及实体瘤中发挥类似疗效。CAR-T疗法在治疗肝癌、肺癌、前列腺癌等一系列的针对实体瘤及其他血液肿瘤的临床试验正在进行。随着研究的不断加速,科学家们将开发出更加安全以及有效的CAR-T疗法,为更多患者带去生存的希望。
第二种肿瘤免疫治疗方法是检查点阻断,是让T细胞恢复对肿瘤细胞的杀伤。这类疗法中的药物被称为“免疫检查点抑制剂”。在人体内,一些小分子往往能与免疫T细胞上的受体结合,抑制它们的活性。这在一般的情况下能够避免T细胞攻击人体的正常细胞,避免自身免疫疾病。但不幸的是,肿瘤细胞也会利用这一点,逃过T细胞的攻击。一些肿瘤细胞会分泌一种叫做PD-L1的配体,当它与T细胞上的PD-1受体结合后,会抑制T细胞的活性,让它们进入“沉睡”状态。
而现在的一些免疫检查点抑制剂能够阻断PD-1与PD-L1之间的交流,它们都是人源化的单克隆抗体,可以与PD-1或者PD-L1结合。这能让T细胞表面的PD-1无法与肿瘤细胞的PD-L1结合,让T细胞不至于被麻痹,也可以直接与肿瘤细胞分泌的PD-L1结合,不让它们靠近T细胞的PD-1受体。总之,这类药物阻断了肿瘤细胞对T细胞的“欺骗”渠道,让T细胞能够保持活性,对肿瘤细胞产生杀伤。
目前,证明有效的肺癌的免疫治疗法是“免疫检查点抑制剂治疗机制”。免疫检查点是通过调节免疫系统反应来维持自身耐受并保护周围组织的免疫抑制性通路,肿瘤细胞会利用这一特性逃避免疫细胞的攻击。肺癌中研究最受关注的两个免疫检查靶点是细胞毒性T淋巴细胞相关抗原4(CTLA-4)和程序性死亡(PD-1)受体。其他免疫疗法,包括在其他癌种里展现效果的CAR-T等,对肺癌都还没有证明其疗效。目前,FDA针对肺癌批准上市的免疫药物有3种:PD-1抑制剂Nivolumab、PD-1抑制剂Pembrolizumab和PD-L1抑制剂Atezolizumab。
對于疾病,特别是癌症,每个个体的独特性是很鲜明的。一种药物或治疗手段在某个人身上有效,并不意味着在其他患者身上也同样有效;在同一类癌症中有效,并不表示在另外一种癌症中也有同样的效果。这些困难和局限性,仍需要科学家们长期深入研究。总之,免疫治疗作为新兴疗法,在癌症临床实践中还有很多“未解之谜”。人们完全有理由相信,随着免疫治疗相关研究的不断开展,数据的不断丰富,被认为“绝症”的癌症有望逐渐成为可控可治的慢性病,造福更多的癌症患者。