不讲武德?用广谱抗癌方案一招击溃13种晚期癌症
仑伐替尼是一种多靶点酪氨酸激酶受体抑制剂,可抑制血管内皮生长因子(VEGF)受体VEGFR1(FLT1)、VEGFR2(KDR)和VEGFR3(FLT4)的激酶活性。除正常细胞功能外,LENVIMA还可抑制与致病性血管生成、肿瘤生长和癌症进展相关的其他激酶,包括成纤维细胞生长因子(FGF)受体FGFR1-4、血小板衍生生长因子受体α(PDGFRα)、KIT和RET。
帕博利珠单抗是一种抗PD-1治疗药物,通过提高人体免疫系统帮助发现和抗击肿瘤细胞的能力发挥作用。KEYTRUDA是一种人源化单克隆抗体,可阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,从而激活可能影响肿瘤细胞和健康细胞的T淋巴细胞。
仑伐替尼具有免疫调节活性,与抗PD-1单抗联合使用具有协同作用,会增加抗PD-1单抗的疗效。仑伐替尼联合帕博利珠单抗,正在13种肿瘤类型(子宫内膜癌、肝细胞癌、黑色素瘤、非小细胞肺癌、肾细胞癌、头颈部鳞癌、尿路上皮癌、胆道癌、结直肠癌、胃癌、胶质母细胞瘤、卵巢癌和三阴性乳腺癌)中该联合用药进行评价。

子宫内膜癌
仑伐替尼联合帕博利珠单抗治疗经治晚期子宫内膜癌的中期分析结果显示,24周时联合方案ORR达38.0%,其中,微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)亚组ORR高达63.6%。
基于该结果,仑伐替尼联合帕博利珠单抗已获FDA加速批准用于经系统性治疗后进展、但不适合进行根治性手术或放疗的非MSI-H/ dMMR型晚期子宫内膜癌患者。
胃癌

《柳叶刀·肿瘤学》发表了临床II期EPOC1706试验的数据,结果显示,帕博利珠单抗联合仑伐替尼在一二线治疗胃癌中,客观缓解率达到69%。
研究共入组了29例复发或转移性胃癌患者(27例MSS,2例MSI;14例为一线治疗,15例为二线治疗)。中位随访时间为12.6个月(IQR 10·5-14·3),29例中有20例患者(69%,95%CI 49-85)获得了缓解。排除两例错配修复缺陷患者,剩余27名患者的ORR仍然达到了70%。接受一线和二线治疗患者的ORR相似,疾病控制率(DCR)达100%。中位无进展生存期为7.1个月(95%CI 5·4-13·7),中位总生存期尚未达到。
探索性分析显示,在PD-L1阳性患者中,ORR达到84%,在PD-L1 CPS<1的患者中,ORR也达到了40% (4/10)。有21名患者的肿瘤突变负荷(TMB)可以被评估,在高TMB患者中(TMB>10),ORR达到82%,在低TMB患者中,ORR为60%。
肝癌
JCO公布了帕博利珠单抗联合仑伐替尼治疗不可切除肝细胞癌的数据,共104例患者入组,100例纳入一线分析,ORR高达46%,中位OS延长至22个月,中位PFS 9.3个月,6个月生存率为81%,1年生存率为67.5%。
2020年美国临床肿瘤学会胃肠肿瘤研讨会上,仑伐替尼联合纳武利尤单抗一线治疗不可切除肝细胞的Ⅰb期临床研究也令人瞩目:ORR为76.7%,完全缓解(CR)为10%,疾病控制率(DCR)为96.7%。
黑色素瘤
LEAP-004是一项在12周内接受抗PD-1/PD-L1治疗后出现疾病进展的不可切除或晚期黑色素瘤患者中评价仑伐替尼联合帕博利珠单抗的II期、单臂、开放性试验。患者口服仑伐替尼 20 mg,每日一次,同时静脉输注帕博利珠单抗 200 mg,每3周一次,持续35个周期(约2年),直至出现不可耐受的毒性或疾病进展。主要终点为ORR。次要终点包括无进展生存期(PFS)和缓解持续时间(DOR)、总生存期(OS)以及安全性。
截至数据截止日期(2020年6月10日),共有103例患者入组并接受治疗。中位随访持续时间为12个月(范围:8.7-15.6),仑伐替尼联合帕博利珠单抗的总体ORR为21.4%(n=22),完全缓解率为1.9%(n=2),部分缓解率为19.4%(n=20)。在总体研究人群中,中位DOR为6.3个月(范围:2.1+至11.1+),72.6%的患者缓解持续至少6个月。中位PFS为4.2个月,73.8%的患者出现疾病进展或死亡,9个月PFS率为26.2%。中位OS为13.9个月(95% CI:10.8-未达到[NR]),44.7%的患者死亡,9个月OS率为65.4%。
探索性分析表明,在接受抗PD-1/L1治疗+抗CTLA-4治疗后出现疾病进展的29例患者中,ORR为31%(95% CI:15.3-50.8),完全缓解率为3.4%(n=1),部分缓解率为27.6%(n=8)。在这些患者中,疾病控制率(DCR)为62.1%。在总体研究人群中,DCR为65%。
肾癌
来自KEYNOTE-146/Study 111 研究II期部分肾细胞癌队列结果:入组患者每三周静脉输注200mg帕博利珠单抗,同时每日口服一次仑伐替尼20mg。
第24周时ORR为51%;总体ORR为55%,PR率为55%;mDOR为12个月(95%CI:9-18);mPFS达到11.7个月(95%CI:9.4-17.7),12个月PFS率为45%;mOS尚未达到(95%CI:16.7-NR),12个月OS率为77%。
肺癌、头颈鳞癌等
2020年一项帕博利珠单抗联合仑伐替尼组合治疗实体瘤的Ib/II期多中心研究结果在JCO杂志上发布,此项研究共纳入了137例晚期实体瘤患者,包括30例肾癌、23例子宫内膜癌、22例头颈鳞癌、21例黑色素瘤、21例非小细胞肺癌及20例尿路上皮癌患者,大部分患者(75%)既往都接受过系统治疗。
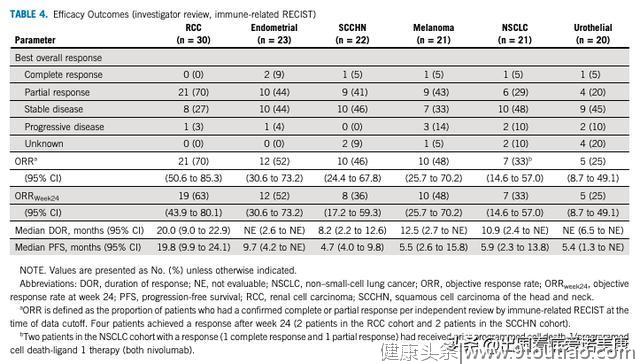
结果显示:非小细胞肺癌总ORR为33%,24周ORR为33%,其中有1例CR,DCR为81%,mDOR为10.9个月,mPFS为5.9个月;头颈鳞癌总ORR为46%,24周ORR为36%,DCR为91%,mDOR为8.2个月,mPFS为4.7个月;尿路上皮癌总ORR为25%,24周ORR也为25%,DCR为70%,mPFS为5.4个月。
多种实体瘤
LEAP-005是一项在选定既往经治晚期实体瘤患者中评价LENVIMA联合KEYTRUDA的II期、单臂、开放性试验。研究队列为三阴性乳腺癌(TNBC)、卵巢癌、胃癌、结直肠癌(非MSI-H/pMMR)、多形性胶质母细胞瘤(GBM)和胆管癌(BTC)患者。患者口服LENVIMA 20 mg,每日一次,同时静脉输注KEYTRUDA 200 mg,每3周一次,持续35个周期(约2年),直至出现不可耐受的毒性或疾病进展。主要终点为ORR和安全性。次要终点包括DCR、DOR、PFS以及OS。
截至数据截止日期(2020年4月10日),共有187例患者入组并接受治疗。中位随访持续时间为8.6个月(范围:1.9-13.1)时,6种不同肿瘤类型证实的ORR以及有效性和安全性结果:
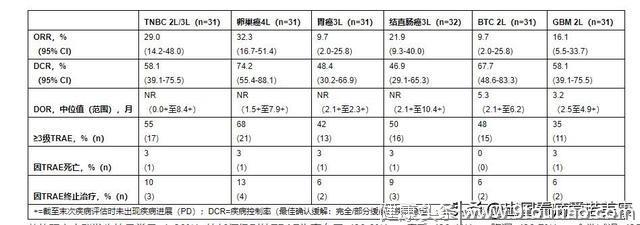
在II期LEAP-005试验中,用于既往经治的三阴性乳腺癌(TNBC)、卵巢癌、胃癌、结直肠癌(非微卫星高度不稳定性[非MSI-H]/错配修复基因正常[pMMR])、多形性胶质母细胞瘤(GBM)和胆管癌(BTC)患者中,仑伐替尼联合帕博利珠单抗的ORR范围为9.7-32.3%。
以上这些数据表明,仑伐替尼联合帕博利珠单抗在多种侵袭性癌症类型中表现出鼓舞人心的抗肿瘤活性,这将帮助更多患有这些癌症的患者,中晚期癌症治疗也将逐渐进入“靶向+免疫”的联合治疗时代。