2017 ESMO世界胃肠癌大会 中晚期胰腺癌免疫治疗的最新临床数据
——在AM0010治疗与FOLFOX联合治疗进展期1 / 1b期试验期间,观察到晚期胰腺癌患者的具有10.2个月平均生存期和47%一年生存率。

在2017年6月28日至7月1日在西班牙巴塞罗那举行的ESMO第19界世界胃肠癌大会上宣布了一项领先研究性免疫肿瘤药物AM0010临床数据(pegilodecakin,聚乙二醇化白细胞介素10 )。AM0010正在进行一项1/1b临床试验的评估,该临床试验已经登记了352名晚期癌症患者,以及正在接受晚期胰腺癌患者的第三阶段临床试验。
“在正在进行的1期/ 1b期临床试验中,AM0010与FOLFOX(亚叶酸,5-氟尿嘧啶和奥沙利铂)联合化疗已经证明了迄今为止在晚期胰腺癌患者中非常有希望的功效和安全性数据,”加州洛杉矶加州大学洛杉矶分校的大卫格芬医学院以及第三期临床试验的调查员,J.Randolph Hecht博士说。“这项研究的中位随访是14.2个月(范围6.8-18.9个月),21个患者中有10例(47%)在一年以上仍然存活。
Van Vlasselaer博士说:“我们很受鼓舞,我们继续在这个试验中看到这样的有前景的数据趋势。”“这些阶段1/1b的数据提供了我们正在进行的关键阶段3临床试验的基本理论,同时将FOLFOX作为晚期转移性胰腺癌的二线治疗。”
晚期胰腺癌的1期/ 1b期临床试验结果
在本次正在进行的1期/ 1b期临床试验中,47例晚期胰腺导管腺癌(PDAC)患者已经用单独的AM0010或AM0010与FOLFOX化疗联合治疗。22名患有PDAC的患者接受AM0010单药治疗,21名尚未接受以前含铂治疗方案的PDAC患者接受AM0010联合FOLFOX治疗。单独或与FOLFOX组合,PDAC患者AM0010治疗耐受性良好。
与每日给药的AM0010相关的3/4级治疗相关不良事件包括血小板减少症,贫血和中性粒细胞减少症是短暂的和可逆的。AM0010加上FOLFOX与修订的AM0010剂量计划(5天,2天休)测试无3/4级血液不良事件。正在进行的3期临床试验中正在使用该修改的剂量计划。
截至2017年5月1日,PDAC患者参加了1期/ 1b期临床试验的结果如下:
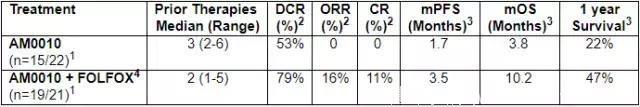
(1)n =可评估患者人数/入组人数
(2)疾病控制率(DCR),客观反应率(ORR)和完全缓解率(CR)均基于可评估患者
(3)中位无病生存期(mPFS)和中位总生存(mOS)是基于治疗患者的意图
(4)进行中的研究,数据截至2017年5月1日。中位随访14.2个月(范围6.8-18.9个月)
AM0010与FOLFOX联合增加患者血清中的免疫刺激细胞因子,并增加患者以前未检测到的新T细胞克隆。新T细胞克隆的扩增使患者的总体生存期更长。
咨询更多抗癌技术及权威专家,请致电或登录全球肿瘤医生网。
全球肿瘤医生网是由医生组建的专业抗癌技术服务平台,与国内外医院保持密切的会诊和转诊合作关系,可以帮助患者在全球范围内选择最适合的医院、技术、药物、临床实验进行治疗,可以为患者提供终身的抗癌追踪和治疗服务。国内患者可以通过全球肿瘤医生网接受权威癌症专家的会诊,通过平台直接预约前往美国医院治疗,也可以通过平台接受最新抗癌技术评估和治疗。