肝硬化丙肝患者遭遇药物不良反应,雪上加霜的困境该如何破解?

药物不良反应是临床实践中的一大难题,将严重影响患者治疗效果,而攻克这一难题,我们一直在路上……
来源丨医学界消化肝病频道
病毒感染20年后,慢性丙型病毒性肝炎(CHC)患者群体的肝硬化年发生率为5%-15%[1]。由于发病隐匿,部分患者在确诊CHC时,已处于肝硬化期,甚至已发展为肝癌。当肝硬化患者出现肝功损害时,抗病毒治疗尤为迫切,但肝功损害也为治疗带来了高难度的挑战。今天,我们向大家介绍一例处于肝硬化代偿期的GT1b型CHC病例[2],他同时遭遇了独特的药物不良反应,但是最终抗丙肝治疗成功。
患者是一位49岁的日本男性,GT1b型CHC病史10年,我们先来看一下他的治疗难点:
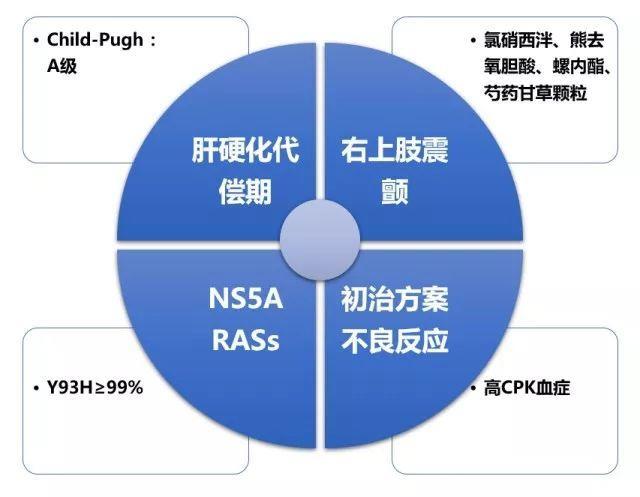
图1 病例治疗难点
患者的转氨酶、肝脏硬度、血小板计数、凝血酶原活动度均异常,具体情况见表1:
表1 病例基线检测结果
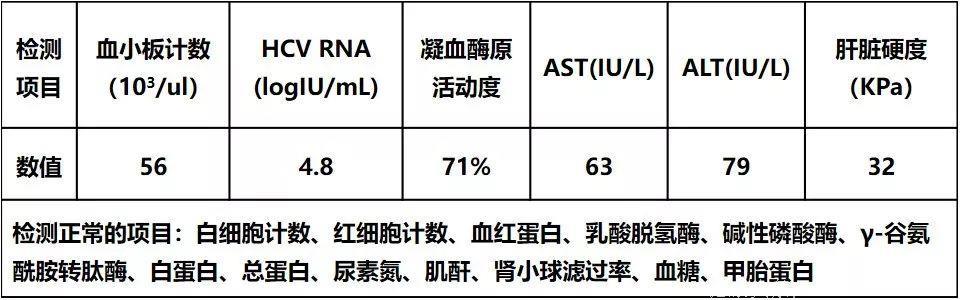
从患者的检测结果可以看出,患者已处于肝硬化代偿期,不适用聚乙二醇干扰素+利巴韦林方案,治疗者为患者使用了Ledipasvir(90 mg/日)+sofosbuvir(400 mg/日)的初治方案。患者在用药14天后出现了药物并发症——高肌酸磷酸激酶(CPK)血症(CPK:2194 IU/L)。
此时治疗者只能放弃初治方案,但是却不能放弃对患者的治疗。治疗者为患者选择了择必达(Zepatier,Grazoprevir/elbasvir)作为新的治疗方案,其原因为:
多项临床试验证实,Zepatier药物毒副反应少,药物安全性良好,可安全应用于肝硬化代偿期及慢性肾功能不全(CKD)患者;
Zepatier治疗GT1b型CHC患者,初治肝硬化人群的SVR12率高达99%[3,4],可谓疗效显著;
美国肝病研究组织CHC治疗指南[5]建议:由于NS5A RAS(相关靶点有:M28T,Q30E/H/R,L31M,H58D,Y93H/N等)不影响Zepatier对GT1b型CHC患者的疗效,无需对使用Zepatier治疗的GT1b型感染者进行RAS检测;
Zepatier具有药物相互作用少的优势,当CHC患者应用多种药物治疗伴随疾病时,应优先考虑使用Zepatier。
Zepatier的这些特点在治疗中得到了体现,在治疗4周后,患者的HCV RNA 转为阴性,获得快速病毒学应答(RVR),在治疗12周后检测HCV RNA显示,获得持续病毒学应答(SVR);在治疗过程中,患者的谷丙转氨酶(ALT)出现明显下降,最终稳定在正常水平(两者动态变化过程见图2)。
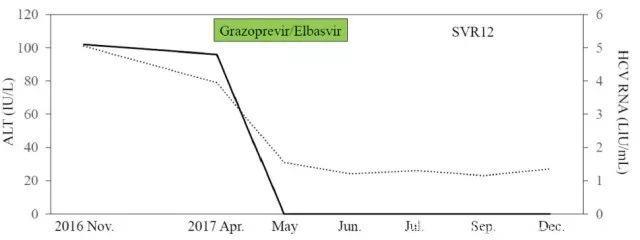
图2 病例在治疗过程中的ALT和HCV RNA
动态变化过程
注:实线:HCV RNA;虚线:ALT
临床启示
这一病例再次向我们证实了Zepatier的高效性和安全性:
1. Zepatier治疗GT1b型CHC患者,疗效显著:既往多项研究[3,4,6-10]证实,Zepatier治疗GT 1b型CHC患者,包括肝硬化、HIV感染、遗传性血液疾病、CKD、阿片类兴奋剂使用者等特殊患者,SVR12高达95%~99%以上,并且无需进行RAS检测。
2. Zepatier安全性良好,可以应用于肝硬化代偿期患者和CKD患者:美国肝病研究组织CHC治疗指南[5]推荐Zepatier可安全地用于肝硬化代偿期患者、CKD患者和血液透析患者,无需调整剂量。
3. Zepatier的其它不良反应少:在多项临床试验[3,4,6-10]中,Zepatier均展现出了良好的药物安全性。某些DAA药物可能导致严重的心律失常,比如sofosbuvir或Harvoni与胺碘酮同时使用可能导致严重的心率减慢,但Zepatier可以用于使用胺碘酮的患者。本例患者在使用sofosbuvir/ Ledipasvir后出现高CPK血症,换用Zepatier后未出现高CPK血症,值得我们借鉴。
由此可见,对于肝硬化代偿期的GT1b型CHC患者以及合并多种疾病、使用多种药物治疗者,Zepatier可以作为优选使用药物。相信随着Zepatier在中国的上市使用,更多的国内丙肝患者,尤其是病情复杂的丙肝患者,将得到显著获益。
参考文献:
[1] 中华医学会肝病学分会,中华医学会感染病学分会. 丙型肝炎防治指南( 2015 年更新版).
[2] Kanda T, Yasui S, Nakamura M, et al. Successful retreatment with grazoprevir and elbasvir for patients infected with hepatitis C virusgenotype 1b, who discontinued prior treatment with NS5A inhibitor-including regimens due to adverse events. Oncotarget. 2018;9(22):16263-16270.
[3] Zeuzem S, Ghalib R, Reddy KR, et al.Grazoprevir-elbasvir combination therapy for treatment-naive cirrhotic andnoncirrhotic patients with chronic hepatitis C virus genotype 1, 4, or 6Infection: a randomized trial. Ann Intern Med. 2015;163(1):1–13.
[4] George J, Burnevich E, Sheen I, et al.Efficacy and safety of elbasvir/grazoprevir in treatment-naive subjects withchronic HCV GT 1, GT 4 and GT 6 infection (C-CORAL): a phase III randomizedmultinational clinical trial [abstract no. 76 plus conference report].Hepatology. 2016;64(Suppl 1):41A.
[5] https://www.hcvguidelines.org/evaluate/resistance.
[6] Kwo PY, Gane E, Peng C-Y, et al.Effectiveness of elbasvir and grazoprevir combination, with or withoutribavirin, for treatment experienced patients with chronic hepatitis Cinfection. Gastroenterology.2017;152(1):164–75.
[7] Rockstroh JK, Nelson M, Katlama C, etal. Efficacy and safety of grazoprevir (MK-5172) and elbasvir (MK-8742) inpatients with hepatitis C virus and HIV co-infection (C-EDGE CO-INFECTION): anon-randomised, open-label trial. Lancet HIV. 2015;2(8):e319–27.
[8] Hezode C, Colombo M, Bourliere M, etal. Elbasvir/grazoprevir for patients with hepatitis C virus infection andinherited blood disorders: a phase III study. Hepatology. 2017;66(3):736-745.
[9] Kumada H, Suzuki F, Karino Y, et al.The combination of elbasvir and grazoprevir for the treatment of chronic HCVinfection in Japanese patients: a randomized phase II/III study. JGastroenterol. 2017;52(4):520–33.
[10] Sperl J, Horvath G, Halota W, et al.Efficacy and safety of elbasvir/grazoprevir and sofosbuvir/pegylatedinterferon/ribavirin; a phase III randomized controlled trial. JHepatol.2016;65(6):1112–9.