糖尿病长胖或变瘦,可能和这些隆糖药有关
北京大学第一医院 张俊清
2型糖尿病患者多伴有超重和肥胖,CCMR-3B研究纳入我国25817例2型糖尿病患者,研究显示糖尿病合并CV危险因素越多,高BMI患者比例越高[1]。超重和肥胖的2型糖尿病患者体重每增加5Kg,心血管风险增加13%,卒中风险增加11%,全因死亡风险增加27%[2]。体重增加还会增加胰岛素抵抗,影响患者对药物治疗的依从性和生活质量。因此,2018 AACE/ACE 2型糖尿病综合管理策略和2018 ADA/EASD 2型糖尿病患者高血糖管理共识[3]都指出在糖尿病治疗药物选择中应综合考虑药物的降糖疗效、对体重的影响和心血管安全性。本文将梳理降糖药物对体重的影响。
导致体重增加的降糖药
导致体重增加的药物包括胰岛素、胰岛素促泌剂(磺脲类和格列奈类降糖药)以及噻唑烷二酮(TZD)类降糖药。系统分析显示,这些药物带来的平均体重增加TZD为5.0kg/年,胰岛素为3.3kg/年、胰岛素促泌剂为1.8kg/年[4] (图1)。
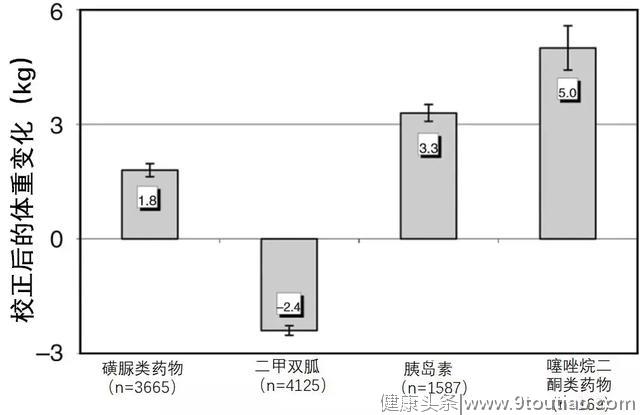
图1. 校正后的12个月体重变化
胰岛素治疗导致体重增加的机制主要是:胰岛素促进肌肉及脂肪组织的蛋白质合成,中心性肥胖及血脂紊乱加重,为纠正或避免低血糖导致进食增加,过度依赖胰岛素导致饮食放纵,尿糖得到纠正导致能量丢失减少等[5]。Holman 发现基础胰岛素使体重增加 3.6±0.5 kg,双相预混胰岛素体重增加5.7±0.5 kg,餐时胰岛素增加体重6.4±0.5 kg[6]。体重增加虽然是导致不良心血管结局的重要因素,但多项大型临床研究结果显示,胰岛素强化治疗通过纠正血糖、改善脂代谢紊乱,能够使患者得到长期获益,改善长期的心血管结局。
胰岛素促泌剂的作用机制是刺激胰岛β细胞分泌更多量胰岛素,因而其导致体重增加的机制理论上与胰岛素类似,主要通过增多的胰岛素发挥对体重的影响作用。UKPDS研究结果显示,传统的胰岛素促泌剂(氯磺丙脲和格列本脲)可使患者体重平均增加3.5-4.8 kg[7]。目前临床广泛应用的新型磺脲类降糖药通过技术创新减轻了体重增加和低血糖的不良反应。多项大型研究均证实,在不增加体重的情况下,新型磺脲类药物可获得很好的降糖效果和远期减少糖尿病微血管并发症的获益。此外,剂型的改变也使磺脲类药物(如格列齐特缓释片)在有效降糖的同时不增加体重[8]。格列奈类降糖药能够与β细胞受体快速结合,快速解离,不会持续过度刺激胰岛素分泌,因此,增加体重的作用弱于磺脲类药物。
噻唑烷二酮类降糖药属于胰岛素增敏剂,适用于以胰岛素抵抗为主的2 型糖尿病患者,降糖作用明显并持久。其常见副作用为体重增加和水肿,还可能会增加骨折和心衰风险[9],在我国及其他一些国家,已经被严格限制使用。TZD可能通过多种途径导致体重增加[10]:增加胰岛素对血糖的敏感性,使尿糖减少,能量在体内堆积;激活过氧化物酶增殖物激活受体(PPAR)-γ,有效抑制脂肪分解,促进皮下脂肪细胞分化和脂肪生成;动物实验和临床试验均证实,TZD可以通过降低瘦素水平而导致体重增加。ADOPT研究证实罗格列酮治疗5年后患者的体重增加4.8 Kg[11]。吡格列酮同样也会增加体重。
可以减轻体重的降糖药
降低体重的降糖药物包括二甲双胍、钠-葡萄糖共转运蛋白2(sodium glucose cotransporter 2, SGLT2)抑制剂和胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂。降低体重可以明显降低T2DM患者心血管疾病危险因素,在2016年《中国2型糖尿病合并肥胖综合管理专家共识》[12]中指出,对于超重/肥胖的患者应优先选择有利于减轻体重或对体重中性影响的药物。2018 ADA/EASD 2型糖尿病患者高血糖管理共识[13]推荐对于迫切需要减少体重增加或减重的患者,降糖药物应首选二甲双胍,如果HbA1c不达标,应该联合减重效果好的GLP-1受体激动剂或SGLT2抑制剂。
二甲双胍有60年的临床应用经验,国内外主要糖尿病指南均建议,除非存在禁忌证或无法耐受,2型糖尿病患者都应从一开始就使用二甲双胍治疗,且应该成为联合治疗的基础,充分体现了其在糖尿病治疗中的重要地位。荟萃分析显示,二甲双胍可使体重降低1.1 kg[14]。二甲双胍减轻体重的机制可能包括:抑制食欲,减少热量摄入;改善高胰岛素血症,降低基础胰岛素和负荷后胰岛素水平;增加瘦素敏感性[15]等。
高选择性SGLT2 抑制剂是一种新型的口服抗糖尿病药物,通过抑制近端肾小管上皮细胞中的SGLT2,减少肾小球滤液中90%的葡萄糖重吸收,促进尿葡萄糖的排泄,起到降低血糖和减轻体重的作用。在合并确诊的ASCVD或者ASCVD高危患者中,恩格列净和卡格列净能带来心脏和肾脏获益。在一项89%受试者为中国患者的III期多中心、双盲、平行、对照研究中,初始治疗的2型糖尿病患者24周时安慰剂、达格列净 5 mg和10 mg组体重分别减少0.27kg、1.64 kg和2.25 kg[16]。另一项比较恩格列净联合二甲双胍与格列美脲联合二甲双胍用于治疗血糖控制不佳的T2D患者(EMPA-REG H2H-SU)的研究中,恩格列净25 mg QD组与基线相比体重降低3.2 kg,格列美脲组体重增加1.6 kg,104周时情况类似[17]。
GLP-1受体激动剂是一类注射给药的新型降糖药物,能够以葡萄糖依赖的方式刺激胰岛素分泌,抑制胰高糖素分泌,降低血糖,同时能够增加饱腹感,减轻体重。在约30周的治疗期间,GLP-1受体激动剂可使体重下降1.5-6.0 kg[18]。有研究显示利拉鲁肽和semaglutide能改善心血管结局,有良好的心血管保护作用。AWARD-5研究中,度拉糖肽1.5 mg治疗52周平均体重下降3.03 kg,治疗104周后,依然能够保持2.8~8 kg的降幅[19]。LEADER研究显示,利拉鲁肽组体重显著减轻2-9 kg[20]。基线不同体重指数的患者使用利拉鲁肽,均能获得体重的降低[21]。GLP-1RA潜在的减重机制包括:独特的中枢作用,可以促进饱腹感、降低食欲、加快能量消耗和减少脂肪合成;通过迷走神经通路减缓胃排空[22] (图2)。
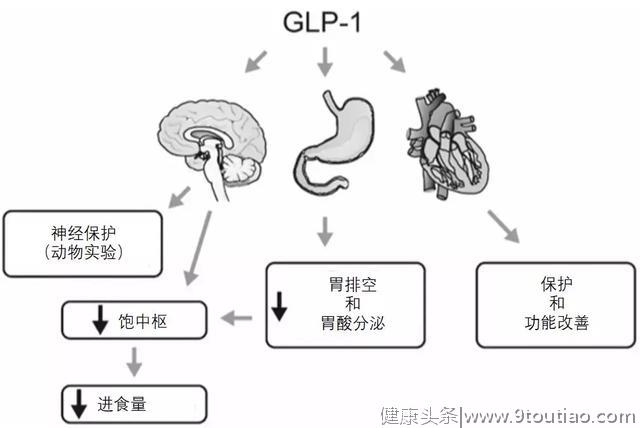
图2. GLP-1受体激动剂潜在的减重机制
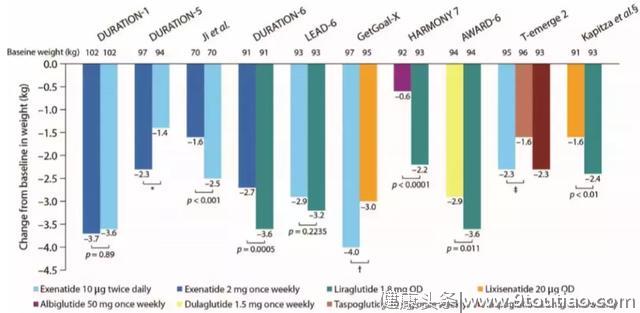
图3. 不同GLP-1RA的对体重影响差异[23]
SGLT-2抑制剂和GLP-1受体激动剂两类新型降糖药极少低血糖反应,能明显降低体重,且对心血管有保护作用,有助于改善2型糖尿病伴或不伴心脑血管事件危险因素的患者的预后。
对体重影响较少的降糖药物
二肽基肽酶-4(dipeptidyl peptidase-4,DPP-4)抑制剂是新型肠促胰岛素类降糖药物,以葡萄糖依赖方式增加胰岛素分泌、减少胰高糖素分泌,有中等降糖作用,对体重无影响。一项在11个国家100家中心进行的临床研究共入选1055例患者,在原来稳定的二甲双胍和磺脲类联合治疗基础上,加用利格列汀5 mg/d或安慰剂治疗24周,与基线相比,利格列汀组体重增加0.40 kg,安慰剂组增加0.30 kg,两组无统计学差异[24]。《基于肠促胰素的治疗药物临床应用快速建议指南》[25]建议DPP-4抑制剂可用于超重/肥胖T2DM患者的降糖治疗。
ɑ-糖苷酶抑制剂通过抑制碳水化合物在小肠上部的吸收而降低餐后血糖,进而影响空腹血糖的控制效果,在降糖的同时,不影响体重,是肥胖性2型糖尿病患者单用或联合治疗的选择之一。但是,研究显示阿卡波糖300 mg/天有减轻体重的作用[26]。一项纳入601例亚洲患者、60例欧洲患者的平行对照研究显示,对于新诊断的糖尿病患者,阿卡波糖(300 mg/d)体重降低优于DPP-4抑制剂(100 mg/d)[27]。我国11家糖尿病中心入选788例新诊断的2型糖尿病患者,随机给予二甲双胍1500 mg/天和阿卡波糖300mg/天治疗24周,阿卡波糖治疗组平均体重下降2.55 kg,优于二甲双胍治疗组(糖尿病平均下降1.88 kg)。阿卡波糖减重的可能机制包括:改善糖脂代谢紊乱;改善胰岛素抵抗,节约内源性胰岛素分泌;延缓肠道对碳水化合物的吸收,刺激L细胞分泌GLP-1;调节肠道菌群,降低炎症反应等多种机制。

专家简介

张俊清教授 北京大学第一医院
北京大学第一医院内分泌科主任、主任医师、研究生导师。长期从事内分泌代谢疾病临床和科研工作,主要研究方向为胰岛素信号传导、糖尿病及其并发症发病机制。
学术兼职:中华医学会内分泌学分会常委,中国医师协会内分泌代谢病学分会常委兼副总干事,北京医学会内分泌代谢学分会副主任委员,北京医师协会内分泌代谢学分会常务理事,中国老年保健医学研究会老年内分泌与代谢病分会常委,中华预防医学会糖尿病预防与控制专业委员会常委,中国女医师协会糖尿病专业委员会常委兼秘书,全国卫生产业企业管理协会—慢病防治分会常委。《中国糖尿病杂志》、《中国医学前沿杂志(电子版)》、《国际糖尿病》等杂志编委。
参考文献
(上下滑动可查看)
1.Am J Med. 2013 Oct;126(10):925.e11-22.
2.Postgrad Med.Diabetologia. 2009 Jan;52(1):65-73.
3.Diabetologia. 2018an;61:2461-2498.
4.Diabetes Obes Metab. 2007 Jan;9(1):96-102.
5.J Clin Hypertens (Greenwich). 2009 Oct;11(10):601-7.
6.N Engl J Med. 2007 Oct 25;357(17):1716-30.
7.BMJ. 1995 Jan 14;310(6972):83-8.
8.N Engl J Med. 2008 Jun 12;358(24):2560-72.
9.Acta Pharmacol Sin. 2010 Aug;31(8):1005-12.
10.邢小燕, 杨文英. 噻唑烷二酮类药物治疗2型糖尿病的有效性及安全性[J]. 中国药物警戒, 2005, 2(2):72-75.
11.N Engl J Med. 2006 Dec 7;355(23):2427-43.
12.中国2型糖尿病合并肥胖综合管理专家共识[J].中华糖尿病杂志, 2016, 8(11): 662-666.
13.Diabetologia. 2018an;61:2461-2498.
14.J Clin Endocrinol Metab. 2015 Feb;100(2):363-70.
15.Diabetes. 2006 Mar;55(3):716-24.
16.Clin Ther. 2014 Jan 1;36(1):84-100.e9.
17.Lancet Diabetes Endocrinol. 2014 Sep;2(9):691-700.
18.Am J Med.2017,130:S4-S17.Diabetes Obes Metab.2018,20:2255-2263.
19.Diabetes Care. 2014 Aug;37(8):2149-58.
20.Diabetes Ther. 2016 Sep;7(3):411-38.
21.Diabetes Obes Metab. 2013 Jan;15(1):42-54.
22.Diabetes Obes Metab. 2014 Aug;16(8):673-88.
23.Diabetes Obesity & Metabolism, 2016, 18(4):317-332
24.Curr Med Res Opin. 2013 Aug;29(8):921-9.
25.中华内分泌代谢杂志, 2016,32(6 ): 448-454.
26.Diabetes Care. 1998 Jul;21(7):1058-61.
27.潘长玉等,中华内分泌代谢杂志,2009; 25(4):386-90.
来源:《国际糖尿病》