【审评】昆药集团长效降糖药苏帕鲁肽注射液获批临床
精彩内容
6月14日,昆药集团发布公告,称控股公司上海银诺医药技术有限公司、昆明银诺医药技术有限公司收到国家药品监督管理局核准签发的《药物临床试验批件》,并将于近期开展苏帕鲁肽注射液的Ⅰ期临床试验。
药品基本情况
药品名称:苏帕鲁肽注射液
受理号:CXSL1700186
批件号:2018L02556
剂型:注射剂
注册分类:治疗用生物制品
规格:1ml:3mg
申请人:上海银诺医药技术有限公司,昆明银诺医药技术有限公司
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品进行临床试验。
该新药的研究情况
GLP-1是一种重要的肠促胰岛素激素,可以通过促进胰岛素分泌,抑制胰高血糖素的释放,抑制食欲及减缓胃排空等途径降低血糖。但天然的GLP-1的半衰期很短(1-2分钟),无法成为有效的临床治疗手段,研发长效GLP-1 类似物或GLP-1受体激动剂成为了近年来医药学术界的重要方向。
苏帕鲁肽是银诺医药开发的具有自主知识产权的人源GLP-1受体激动剂,其临床前研究结果显示,苏帕鲁肽相比天然GLP-1具有较长的半衰期。苏帕鲁肽能通过激活GLP-1受体以血糖依赖方式刺激胰岛素分泌,同时,抑制胰高血糖素释放。用糖尿病小鼠动物模型和灵长类动物恒河猴糖尿病模型做的临床前药效结果显示,苏帕鲁肽的降糖效果显著,作用持久,并且具有降低肥胖小鼠的体重,增加胰岛素敏感性,提升血糖耐受,改善肥胖小鼠机体的糖脂代谢的作用。
数据显示,GLP-1受体激动剂2016年全球市场销售额达69.22亿美元,占据糖尿病用药整体市场近10%的份额,2012-2016复合增长率达29.78%,远高于糖尿病用药市场14.67%的整体增速。其中,一周一次的长效GLP-1制剂凭借其更优的临床应用性与患者依从性,在整个GLP-1激动剂的市场份额占比由2011年的31%提升到2016年的42%,显示出良好的市场潜力。
全球在申报及已上市的长效GLP-1受体激动剂制剂主要有索玛鲁肽、度拉鲁肽、苏帕鲁肽及长效艾塞那肽,GLP-1长效制剂因其用药方便性,患者的依从性更好,较短效GLP-1制剂更具优势,度拉鲁肽全球上市后的优秀表现、索玛鲁肽优异的临床研究结果,预示着长效GLP-1市场迎来了快速增长期。
2013-2017年中国公立医疗机构终端利拉鲁肽的销售情况 (单位:万元)
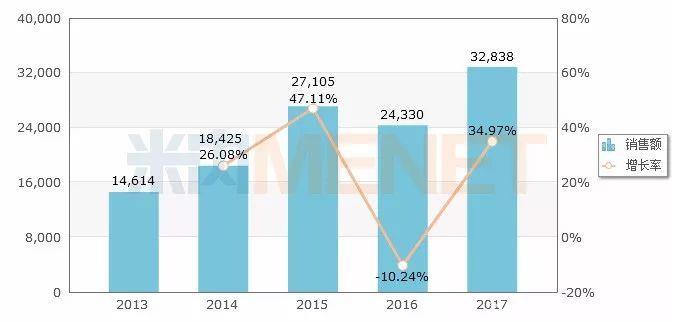
(来源:中国公立医疗机构终端竞争格局)
2017年7月,诺和诺德的利拉鲁肽(短效GLP-1制剂)进入了我国的医保谈判目录,意味着GLP-1制剂的作用和疗效价值得到了国家方面的认可。据米内网数据显示,2017年在中国城市公立医院、县级公立医院、城市社区中心及乡镇卫生院(简称中国公立医疗机构)终端利拉鲁肽的销售额超过3.28亿元,增长率为34.97%。
在中国,沈阳三生的长效艾塞那肽注射液于2018年1月获批上市,诺和诺德的索玛鲁肽注射液处于临床研究阶段、礼来的度拉鲁肽注射液处于临床试验批件申请阶段。银诺医药拥有自主知识产权的苏帕鲁肽作为又一个在中国进入临床阶段的7天周期注射用降糖药,鉴于苏帕鲁肽与艾塞那肽相比具有更高的人类同源性,其肝肾毒性和胰腺炎风险相对较低,具有更优的临床适用性,且与其他进口制剂相比,苏帕鲁肽将具有中国本地化生产的成本优势。苏帕鲁肽如获准上市,将在GLP-1制剂总体呈快速增长的情况下,获得可观的市场收益。
此研发项目是公司慢病领域战略布局的重要一环,也是公司向生物制药领域的开拓性探索,项目的实施使公司的创新能力进一步提升。如苏帕鲁肽成功上市,将成为公司又一重点产品,为公司的持续发展带来新动力。公司在收到上述药物临床试验批件后,将着手启动药物的临床研究相关工作,待完成临床研究后,递交临床试验数据及相关资料,申报生产上市。
来源:上市公司公告、米内网数据库