全脑放疗的新搭档,安罗替尼联合方案入选ESMO年会!—抗癌管家
抗癌管家-康爱管家提示:2020年的欧洲肿瘤学会(ESMO)年会上,安罗替尼联合全脑放疗治疗晚期非小细胞肺癌脑转移患者的II期临床研究入选年会壁报[1]。
研究结果相当可观,颅内客观缓解率和疾病控制率分别为60%和90%,且不良反应可控,为非小细胞肺癌多发脑转移的患者提供了一个极具前景的治疗选择。
放疗仍存在诸多不足,
联合抗血管生成治疗可起到协同作用
抗血管生成治疗与放疗的联合一直是肿瘤治疗的研究热点。
放疗是癌症局部治疗的重要手段之一,临床上,约70%的肿瘤患者需要接受放疗[2]。尽管立体定向放疗使得放疗进入了“精确放疗时代”[3],但放疗的有效率和安全性仍需改进。抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。大剂量的放疗会引起邻近组织的损伤,可能导致严重的炎性疼痛、功能障碍、放射性肺炎、放射性胃炎、食管炎、结肠炎、肝功能衰竭和颅内放射性坏死等[4]。
除了不良反应,肿瘤对放疗的抵抗同样是一大问题,表现为放疗响应不佳,疗效差。血管生成因子恰恰是在这个过程中起到了关键的作用[5]。
最早在1953年,Oliver Scott和他的同事们发现,增加氧气的吸入可以增强小鼠肿瘤对放射线的敏感程度[6,7]。这是因为放疗辐射通过诱导DNA双链断裂,触发细胞周期阻滞和细胞凋亡,而氧是其有效的放射增敏剂,对辐射诱导DNA损伤至关重要[5]。
1971年,Folkman教授首次提出肿瘤生长依赖于血管生成。肿瘤血管生成是指血管内皮细胞从所在血管系统中分化、迁移并形成新的微血管的复杂生物学过程,也是促血管生成因子和抗血管生成因子失衡的结果[5]。
其中,血管内皮生长因子(VEGF)是肿瘤血管生成最重要的刺激因子,能够维持内皮细胞存活,诱导其增殖、迁移和血管形成,增强血管通透性等,因此VEGF及其受体是抗血管生成治疗最重要靶点之一[5]。于是,越来越多以VEGF为靶点抗血管生成药物被开发出来,通过与其他治疗手段的联合,增强抗癌疗效[6]。
20世纪90年代,Teicher等人首先发现了抗血管生成治疗联合放疗的潜力[6]。
肿瘤血管在结构和功能上和正常血管是非常不同的,肿瘤血管高度无序、迂曲、膨胀、分支多,并且血管壁通透性增加,这些都会导致氧气的输送受阻[5]。Teicher等人发现,抗血管生成药物可以增加肿瘤处的氧气浓度,从而增强肿瘤对放射的响应[6]。这才开启了抗血管生成治疗和放疗联合的篇章。
除了改善肿瘤乏氧,近些年的研究还发现,某些肿瘤干细胞对放疗的抵抗作用,正是依赖于血管发生因子,抑制血管发生因子可增强放疗敏感度[5,6]。
安罗替尼联合全脑放疗
显著改善脑转移患者响应率
安罗替尼是一种国产新型多靶点酪氨酸激酶抑制剂(TKI),作用于血管内皮细胞生长因子受体(VEGFR)、血小板衍生生长因子受体(PDGFR)、成纤维生长因子受体(FGFR)、干细胞生长因子(c-Kit)等位点,不但可以抑制肿瘤细胞的增殖,也可以抑制肿瘤血管生成。
ALTER1202研究结果表明,相比安慰剂,安罗替尼将小细胞肺癌患者中位无进展生存期延长了3.4个月(4.1个月 vs 0.7个月),中位总生存期延长了2.4个月(7.3个月 vs 4.9个月)。相对于安慰剂组,安罗替尼组显著延长了中位无进展生存期[8]。
表1:ALTER1202的主要有效性结果
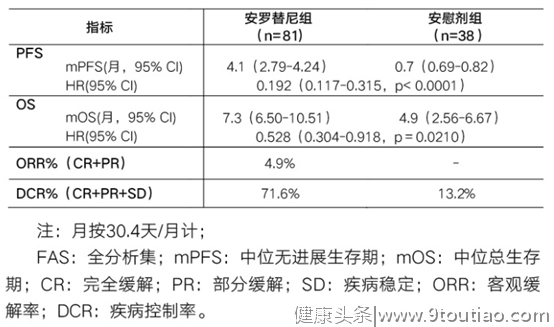
安罗替尼作为首个在国内获批小细胞肺癌后线治疗的小分子多靶点受体酪氨酸激酶抑制剂,打破了小细胞肺癌后线无药可治的僵局,很好地填补了临床空白,造福更多的小细胞肺癌患者。
除了小细胞肺癌,2018年发表于JAMA Oncology的名为ALTER0303的随机、双盲、多中心临床试验数据显示,与安慰剂相比,安罗替尼可将接受过两次化疗之后的晚期非小细胞肺癌的中位无进展生存期延长4.0个月(5.4个月vs 1.4个月),抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。中位总生存期延长3.3个月(9.6个月vs 6.3个月)。基于此,安罗替尼获得国家药品监督管理局(NMPA)批准用于治疗晚期非小细胞肺癌[9]。
近期,安罗替尼联合全脑放疗治疗晚期非小细胞肺癌脑转移患者的II期临床研究取得了可观的效果,结果已经纳入2020年欧洲肿瘤学会(ESMO)壁报。
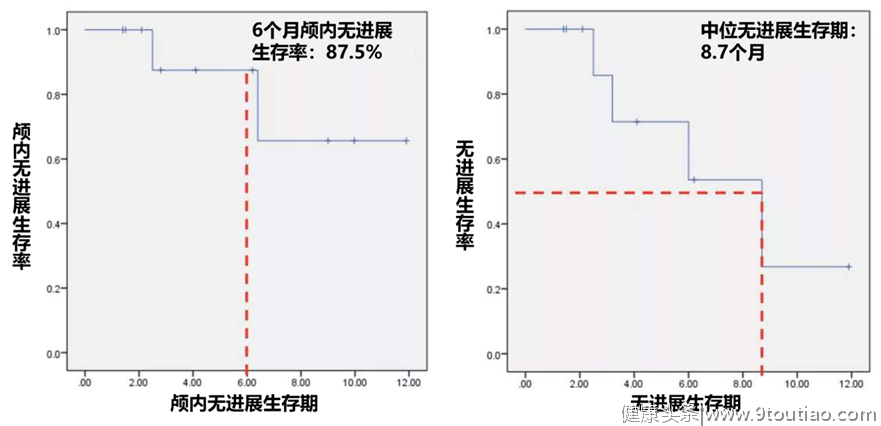
图1:颅内无进展生存期和中位无进展生存期
截止2020年4月30日,总共入组患者20例,10例可评估疗效。在晚期非小细胞肺癌多发脑转移患者中,安罗替尼联合全脑放疗组6个月颅内疾病无进展生存(PFS)率为87.5%,颅外中位PFS为8.7个月。颅内客观缓解率(ORR)和疾病控制率(DCR)分别为60%和90%,颅外ORR和DCR分别为10%和90%,且不良反应可控[1]。可见,安罗替尼联合放疗可行可期。
抗血管生成治疗联合放疗既可发挥抗血管生成治疗的靶向优点,又能提高放疗敏感度。目前,安罗替尼也在同步放化疗后未进展的局部晚期非小细胞肺癌患者中开展了相关前瞻性多中心研究,我们期望这一研究能够让患者在减轻经济负担的同时,也能够获得生存获益。
联合治疗的不良反应仍需注意
一般来说,抗血管生成治疗联合立体定向放疗的疗效要比联合常规分割放疗更好,但联合常规分割放疗的严重不良反应发生率很低,联合立体定向放疗的严重不良反应发生率则高很多。这些不良反应在单独进行立体定向放疗或抗血管生成治疗时也会发生,特别是放射性脑坏死、放射性肺炎、高血压、手足皮肤反应和蛋白尿等[4,10]。
常规分割放疗或立体定向放疗均可能引起放射性脑坏死,通常发生在放疗后6~47个月内[11,12]。常见症状为头痛、疲劳、恶心、身体不稳、四肢无力,甚至为意识模糊等[12],患者及家属需密切关注患者状态变化,并及时告知主治医生。
放射性肺炎需要进行有效抗炎治疗,否则可能发展为肺纤维化[4]。
高血压是抗血管生成类药物的常见不良反应。家属及患者应注意[10]:
- 在使用抗血管生成药物的过程中需动态监测血压,并配合清淡饮食及适当运动。
- 如发生高血压,推荐在医生的指导下使用降压药控制血压。
手足皮肤反应主要表现为手及足底部红斑和感觉异常,抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。用患者的话来描述便是“烂手烂脚”。在使用盐酸安罗替尼治疗期间,若出现手掌或足底等腺体较丰富区域的局部组织损伤,对不同症状,医生可能会建议您使用[13]:
- 润肤霜或润滑剂,或局部使用含尿素和皮质类固醇成分的乳液或润滑剂。
- 必要时局部使用抗真菌或抗生素药物。
若小便时发现有小气泡,别大意,家属及患者应赶紧去医院查查尿常规,如果检查发现尿蛋白有加号:“+”“++”等,即是蛋白尿。建议每6周检查尿常规,对连续2次尿蛋白≥++者需进行 24小时尿蛋白测定[10,13]。
- 蛋白尿+或24小时尿蛋白小于1.0g一般无须担心。
- 若蛋白尿++,请立即联系医生寻求帮助。
虽然抗血管生成治疗存在一定的不良反应,但不良反应一般可控。抗血管生成治疗联合放疗既可发挥抗血管生成治疗的靶向优点,又能提高放疗敏感度,两者的联合为非小细胞肺癌多发脑转移的患者提供了新的治疗选择。
本文转自肺癌康复圈(由“抗癌管家网站-康爱管家”转载分享)