降低30%死亡风险,PD-L1将成小细胞肺癌一线标准治疗方案
今天,美国批准PD-L1药物阿特珠单抗联合卡铂和依托泊苷一线治疗广泛期小细胞肺癌。这是20年来,广泛期小细胞肺癌的一线治疗方案首次被改写。

本项批准是基于一项名为IMpower133的大型III期临床研究,该研究显示出在标准化疗方案(卡铂和依托泊苷)基础上增加阿特珠单抗使用可以显著改善广泛期小细胞肺癌的患者总生存期。

基因泰克(罗氏)全球产品研发部门首席医学官 Sandra Horning医学博士在采访时提到,这是肿瘤免疫治疗首次被批准应用于广泛期小细胞肺癌的一线治疗。直到今天,我们针对小细胞肺癌的治疗依然有限,现在我们很兴奋看到,相比传统化疗方案,PD-L1与化疗联用将改善患者的总生存期。
该IMpower133研究结果曾在世界肺癌大会2018(WCLC2018)和知名医学杂志NEJM上同时发表。这是一项国际、多中心、随机对照的III期临床试验,一共招募了403名刚确诊为广泛期小细胞肺癌的患者,然后按照1:1的比例分组:
标准化疗组
卡铂和依托泊苷
PD-L1联合组
PD-L1药物阿特珠单抗联合标准化疗
在中位随访13.9个月后,研究人员发现,相比标准化疗方案,PD-L1联合标准化疗降低了30%的死亡风险(HR, 0.70; P=0.0069)。
中位总生存时间:PD-L1联合组为12.3个月,标准化疗组为10.3个月。
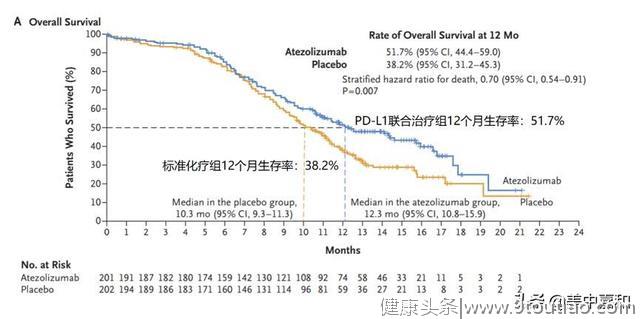
另外,数据显示在12个月疾病无进展生存率,PD-L1联合组也优于标准化疗组(12个月PFS : 12.6% vs 5.4%)。
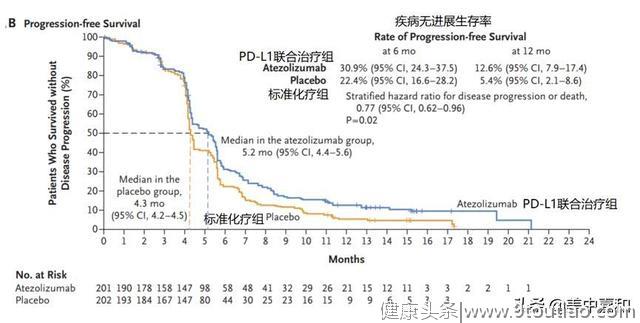
而在药物安全性上来看,PD-L1联合组的不良反应事件与之前研究一致,常见的不良反应为乏力/虚弱(39%),恶心(38%),脱发(37%),食欲减退(27%),便秘(26%)和呕吐(20%)。
写在最后
正因为IMpower133临床试验数据显示出PD-L1联合化疗在小细胞肺癌治疗的优势,美国FDA批准了这一联用方案,这是20年来的一小步,但也为后续免疫治疗在广泛期小细胞肺癌的应用打下坚实的基础。
后续随着临床研究人员对小细胞肺癌研究的深入、免疫治疗策略的优化,2个月、1年、3年,对于小细胞肺癌,未来将有更多选择……
参考文献
[1] Horn L et al. First-line atezolizumab plus chemotherapy in extensive-stage small-cell lung cancer. N Engl J Med. 2018; DOI: 10.1056/NEJMoa1809064.
[2] https://www.roche.com/media/releases/med-cor-2019-03-19.htm