类风湿关节炎治疗现实受阻,如何助力RA患者找到“小欢喜” ?
不想错过界妹的推送?
并点击右上角“···”菜单,选择“设为星标”

当传统合成改善病情抗风湿药(csDMARDs)治疗类风湿关节炎患者遭遇现实瓶颈,生物制剂是否能为我们带来更多样化的选择?
病例简述
患者为52岁女性,7月前无明显诱因下出现左肩疼痛,右腕关节肿痛,右手中指僵硬感,左颞颌关节疼痛,伴口干,外院诊断为“关节炎”,予以抗炎止痛治疗后症状缓解不明显。5月前再次出现右膝关节疼痛,右肩关节疼痛,关节活动受限,诊断为“类风湿关节炎、骨质疏松症”,予以甲氨蝶呤、羟氯喹及其他辅助药物治疗,疼痛略缓解,但仍有关节肿胀,活动受限等症状。
入院查体:生命体征平稳。左肩压痛,右腕关节肿胀压痛,右腕强直,右膝活动时有骨擦感,双“4”字试验(+)。
辅助检查: 红细胞沉降率(ESR):92mm/h;肝功能:天门冬氨酸氨基转移酶(AST) 51U/L,谷氨酸氨基转移酶(ALT)正常,白蛋白 34.1g/L。
入院诊断:1、类风湿关节炎;2、骨关节炎;3、骨质疏松
入院后予以csDMARDs联合辅助药物治疗:甲氨蝶呤 12.5mg每周1次;羟氯喹片0.2g每日2次,均于3天后停用。
停用原因:服药后白细胞减少。
2018年5月12日起患者开始使用IL-6通路抑制剂静脉注射治疗。
2018年5月14日辅助检查示:C反应蛋白(CRP)<3.13mg/L;类风湿因子(RF)阴性;ESR:46mm/h;中性粒细胞 1.77g/L,红细胞(RBC) 2.91T/L,血红蛋白(Hb) 90g/L。
患者继续每月静脉注射IL-6通道抑制剂一次,四个月后,改为每两月注射一次,持续至今。
42018年7月复查:CRP、ESR均正常,关节肿胀、疼痛消失。
52019年4月复查:抗角蛋白抗体(AKA)阴性、RF(-),抗环瓜氨酸肽(CCP)抗体>200RU/ml ;ESR 16mm/h;CRP<3.02mg/L;ALT/AST/白蛋白均正常;中性粒细胞 2.26g/L,RBC 3.67T/L,Hb 121g/L。
“一线”≠“一刀切”
部分患者csDMARDs耐受欠佳
类风湿关节炎(RA)治疗的总原则是达标治疗。csDMARDs是RA治疗的基石,亦是国内外指南共同认可的一线药物[1]。《2018中国类风湿关节炎诊疗指南》[2](以下简称“指南”)推荐RA患者一经确诊,应尽早开始csDMARDs治疗。其中甲氨蝶呤(MTX)为RA治疗的锚定药物。存在MTX禁忌时,考虑单用来氟米特或柳氮磺吡啶。一般情况下,2/3的RA患者单用MTX或与其他csDMARDs联用即可达到治疗目标。当单一csDMARDs治疗未达标时,指南建议联合另一种或两种csDMARDs进行治疗,或联合一种生物制剂DMARDs/靶向合成DMARDs(tsDMARDs)进行治疗。理想很丰满,现实却很骨感。在真实世界临床实践中,除了应答欠佳,部分RA患者还存在csDMARDs难以耐受、服用依从性差的情况,以csDMARDs为基础的初始治疗难以满足所有的临床需求。一项1,500例RA患者的在线问卷显示,45%的患者承认未告知医生并自行停用MTX[3]。纳入1125例RA患者的REAL研究提示患者csDMARDs停药的原因中不良临床事件占36.1%,疗效(原发/继发失效)占53.7%,不良实验室指标占10.2%。另有数据显示真实世界中3-12.7年治疗时间,有10%-77%使用MTX的患者由于不良临床事件(AEs)停药[4]。2016年EULAR 推荐[1],临床上对于经csDMARDs治疗未达标的RA患者,可与bDMARDs和靶向合成DMARDs(tsDMARDs)联合使用。而对于无法联合使用csDMARDs的患者,白介素6(IL-6)通路抑制剂与tsDMARDs较其他bDMARDs具有一定优势。真实世界数据也显示大约有1/3的RA患者正在使用生物制剂单药治疗。机制自成一派
蓄势待发去“打怪”
RA发病机制是由多种细胞因子和免疫细胞参与的复杂过程。在细胞因子中,IL-6、肿瘤坏死因子(TNF)和IL-1对炎症的贡献最为突出,其中由多种细胞产生的IL-6在RA发病中发挥重要作用。
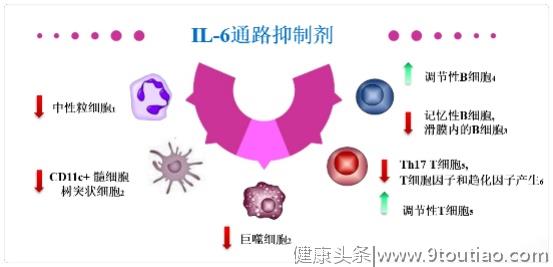
图1 IL-6通路抑制剂的作用机制
IL-6参与调控固有免疫和获得性免疫。一方面,IL-6通路抑制剂阻断IL-6对中性粒细胞、树突状细胞和单核/巨噬细胞等增殖、募集等作用;另一方面,IL-6通路抑制剂影响IL-6对B细胞和T细胞的激活、募集以及效应细胞因子的产生,从而打破RA的恶性炎症循环;且由于IL-6通路抑制剂对B细胞的抑制作用,抗药抗体发生率降低,可一定程度降低类风湿因子[5]。IL-6通路抑制剂通过阻断IL-6信号转导的两种模式――经典膜信号转导和跨越式信号转导,由IL-6、IL-6受体、gp130形成功能性IL-6受体复合物而发挥作用。JAK抑制剂(tsDMARDs)则通过抑制细胞内 JAK 信号通路传导,抑制免疫细胞活化及促炎症细胞因子的释放,从而达到治疗目的。研究发现,在MTX-IRRA患者中,IL-6通路抑制剂单药使用与其联合MTX疗效相当[6]。一项为期3年的双盲研究,旨在评估IL-6通路抑制剂单药与其联合甲氨蝶呤治疗RA 2年以上的疗效和安全性,采用达标治疗方法,自24周开始,若患者DAS28-ESR>3.2,则患者增加csDMARDs(除了MTX)。自52至104周,持续临床缓解的患者中止IL-6通路抑制剂治疗,每4周对患者随访1次,随访长达1年 。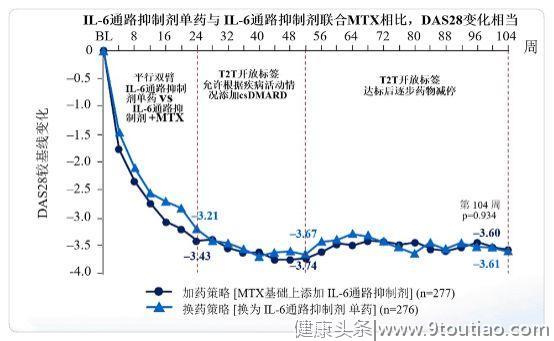
图2 IL-6通路抑制剂单药与其联合MTX相比,2年有效控制疾病活动度DAS28变化相当
结果显示IL-6通路抑制剂与其联合MTX相比,2年有效控制疾病活动度DAS28变化相当。在安全性方面,联合组肝酶升高患者数量高于单药组。该研究提示我们IL-6通路抑制剂在RA的单药治疗中有一定的优越性,不失为RA患者个体化治疗新选择之一[6]。小 结
RA属于终身疾病,早期诊治及治疗方案的选择至关重要。csDMARDs尤其是MTX仍然是RA治疗的锚定药物。对于csDMARDs难以耐受、应答欠佳的患者, b/ts DMARDs单药治疗也是一种有价值的治疗策略。
IL-6通路抑制剂以其独特的作用机制,在RA的单药治疗中展现其一定的优势,为RA患者的个体化治疗提供新的选择。
参考文献:
[1]Smolen JS, et al. Ann Rheum Dis. 2017;76(6)960-977.
[2]中华医学会风湿病学分会.2018中国类风湿关节炎诊疗指南[J].中华内科杂志,2018,57(4):242-251.DOI:10.3760/cma.j.issn.0578-1426.2018.04.004.
[3]Ilar A , Alfredsson L , Wiebert P , et al. Occupation and Risk of Developing Rheumatoid Arthritis: Results From a Population-Based Case-Control Study[J]. Arthritis Care & Research, 2017.
[4]Tanja SchjødtJørgensen,et al.Rheumatology2015;54:2156-2165
[5]Hunter C A , Jones S A . IL-6 as a keystone cytokine in health and disease[J]. Nature Immunology, 2015, 16(5):448-457.
[6]Huizinga T W J , Conaghan P G , Martin-Mola E , et al. Clinical and radiographic outcomes at 2 years and the effect of tocilizumab discontinuation following sustained remission in the second and third year of the ACT-RAY study[J]. Annals of the Rheumatic Diseases, 2015, 74(1):35-43.

黄安斌 教授

梅春丽 主治医师