与肥胖、慢病「神同步」:精炼种子油深度解析 | 野兽生活
其实,过量精炼种子油的潜在危害,不止在于发胖,还可能是各种现代慢性疾病的根源。
今天,我们继续向大家介绍,为什么精炼种子油吃太多容易让人生病。
01
精炼种子油
与现代慢病神同步
在世界上几乎所有国家和地区,精炼种子油的大量食用都与肥胖、慢病出现「神同步」。不论是美国、日本冲绳、以色列,还是中国,都出现了类似的趋势。
从具体病症来说,精炼种子油与它们的「神同步」更是让人触目惊心。
(注意:下面的「神同步」只是相关性,并不直接代表因果关系。)
肥胖
从肥胖来说,曾经,美国人每天的种子油摄入量仅有2克。到2010年,美国人平均每天摄入80克的精炼种子油。
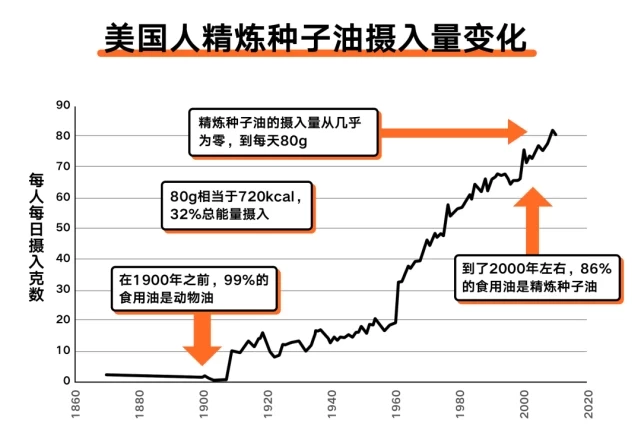
1980年,美国开始推出膳食营养指南,建议民众少吃动物油脂、并用植物油脂来替代。
与之同步的,是美国人的超重、肥胖率的惊人飙升。
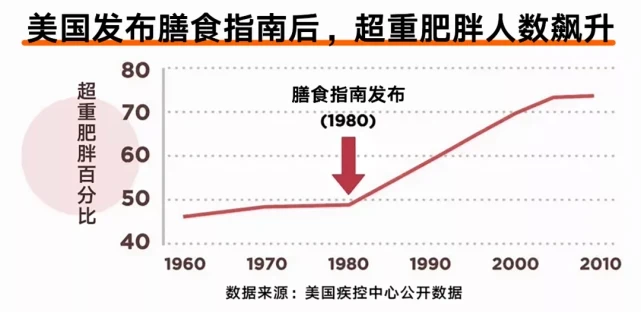
糖尿病
在几十年内,美国2型糖尿病的发病率增加了25倍。根据美国著名医生、NBA湖人队前队医Cathrine Shanahan博士的统计,2型糖尿病的发病率与精炼种子油消耗量呈现几乎完全同步的趋势。
而2型糖尿病被认为是心脏病、脑卒中、阿兹海默病、癌症等几乎所有慢性疾病的重要危险因素。
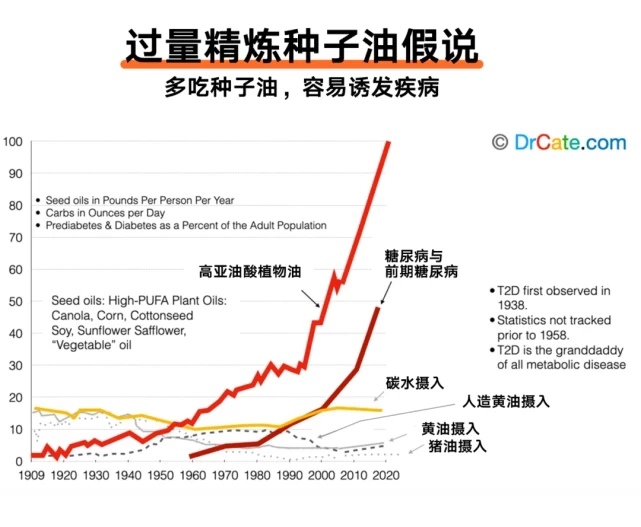
心脏病
从心脏病来看,直到1912年,美国才有第一个心肌梗死病例记录。
而从20世纪30年代开始,这种曾经罕见的疾病,居然渐渐成为美国人口主要死亡原因。

人们曾经认为,饱和脂肪容易升高胆固醇,因此是导致心脏病的重要因素。
但是,从下图可以看出,心脏病死亡的增加,与饱和脂肪摄入量无关,反而与精炼种子油摄入的增加呈现惊人的一致性。

癌症
美国著名医生、临床医学教授Chris Knobbe博士指出,从癌症来看,1811年,人们几乎不吃种子油的时代,癌症死亡仅占美国死亡人口的0.5%。到2010年,这个数字达到31.1%。
也就是说,美国人口中,癌症死亡占比在两百年间增长了62倍。
当然,相关性≠因果性,癌症的死亡人数与医疗水平、人均寿命变化关系很大。但即使考虑到这些因素,癌症死亡的增长也是十分惊人的。

黄斑变性
黄斑变性是导致老年人失明的主要原因,也是全世界最难治疗的眼病之一。
据Chris Knobbe博士统计,从1851年到1930年,世界文献记载不超过50例,而今天全球黄斑变性患者则将近2亿人。在中国,老年人发病率也高达10%左右。
同样,黄斑变性发病率的激增,也与精炼种子油的食用呈现惊人的正相关。

到底有多少种疾病与精炼种子油的食用量「神同步」呢?
根据Cathrine Shannahan博士的统计,精炼种子油至少与下列疾病存在明确的关联:
(上下滑动查看全部)
Adipose Fatty Acid Profile Changes from High PUFA Intake 人体脂肪的脂肪酸比例改变
Adipose Toxicity 人体脂肪毒性化
ARDS (Acute Respiratory Distress Syndrome) 急性呼吸窘迫
Atherosclerosis 动脉粥样硬化
Blood clots 血栓
Brain development abnormalities 脑部发育异常
Cancer 癌症
Crohn's Disease 克罗恩病
Diabetes 糖尿病
Endothelial Dysfunction 内皮功能障碍
Fatty Liver 脂肪肝
Gut Inflammation 肠道炎症
Gut Microbiome Abnormalities 肠道微生物组异常
Heart Attack 心脏病
Heart Failure 心力衰竭
Diastolic Dysfunction 舒张期功能障碍
HDL Dysfunction and lowered HDL 低HDL
Insulin Resistance and Diabetes 胰岛素抵抗
Macular Degeneration 黄斑变性
Mitochondrial Dysfunction 线粒体功能障碍
Muscle Atrophy 肌肉萎缩
Obesity 肥胖
Omega-3 Fatty Acid Depletion Omega 3脂肪酸吸收障碍
Oxidized Cholesterol 氧化胆固醇
Schizophrenia 精神分裂症
Stomach Acid Deficit 胃酸缺乏
再次强调:上面的「神同步」只是相关性,并不直接代表因果关系。
但是,如果这些疾病真的全部与过量精炼种子油摄入有关,这一切是如何发生的呢?
02
过量精炼种子油
到底可怕在哪儿
根据Chris Knobbe博士的研究,当我们吃了过量的精炼种子油以后,它会通过一系列复杂的分子生物机制,在我们体内引发可怕的「脂质过氧化级联反应」。
这会导致2个可怕的结果,一是线粒体功能障碍,二是产生有毒代谢物。
精炼种子油中富含多不饱和脂肪酸(PUFA),当过量摄入,会引发「脂质过氧化级联反应」,进一步导致线粒体电子传递链信号失灵,并诱发线粒体内膜心磷脂病理性重构。
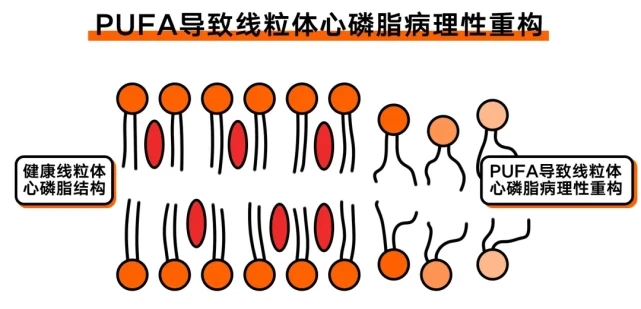
这会导致我们细胞内的「能量工厂」减产、甚至停产。
此外,精炼种子油的制造需要经过高温、高压、化学溶剂萃取、脱胶、除臭等复杂工序,化学性质极不稳定的多不饱和脂肪酸(PUFA)会不同程度地发生变质反应,产生潜在有害物质。
加上存储、高温烹饪,尤其是反复使用的话,产生的潜在有毒有害物质浓度会更高。
然而,过量摄入多不饱和脂肪酸(PUFA),会导致潜在有毒有害物质会在我们体内继续发生。
具体来说,过量精炼种子油会导致体内过量的脂质过氧化,产生脂质过氧化氢。然后,脂质过氧化氢会迅速退化,形成潜在有毒有害物质,包括:
4羟基壬烯酸(4-HNE)
丙二醛(MDA)
氧化亚油酸代谢物(oxLAMs)
丙烯醛
羧乙基吡咯
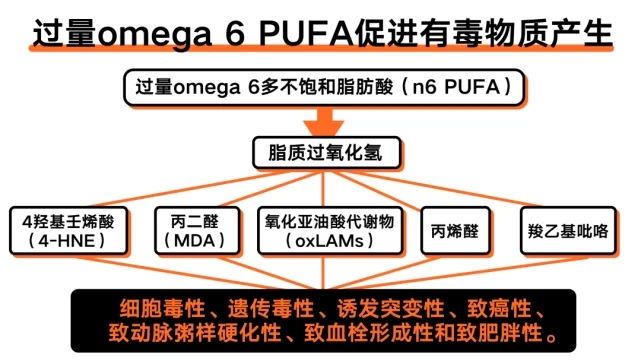
这些物质的共同特性包括:细胞毒性、遗传毒性、诱发突变性、致癌性、致动脉粥样硬化性、致血栓形成性和致肥胖性。
线粒体功能障碍+有毒有害物质产生,俨然是绝大多数现代慢性疾病的「催命符」。
03
过量精炼种子油
是怎样让你生病的
由于过量多不饱和脂肪酸(PUFA)会导致线粒体功能障碍、有害物质的产生,精炼种子油的危害还远不止发胖。
线粒体功能障碍会扰乱胰岛素信号,造成胰岛素抵抗,久而久之会逐渐恶化成代谢综合征和2型糖尿病。
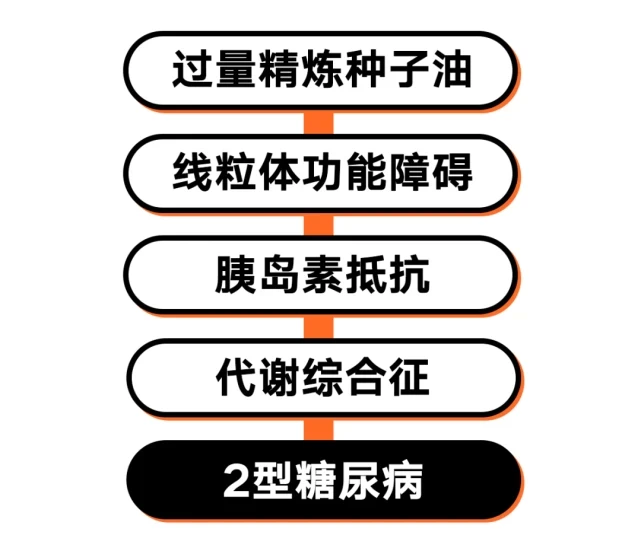
胰岛素抵抗、代谢综合征和2型糖尿病又是几乎所有其他慢性代谢性疾病的共同驱动因素。
线粒体功能障碍发生在心脏细胞,会直接导致心脏衰竭。
有毒有害物质攻击动脉内膜和脂蛋白、胆固醇,会导致血管内皮炎症反应、脂质积累,从而诱发动脉粥样硬化,久而久之就会诱发冠心病、中风。

线粒体功能障碍会导致细胞凋亡和细胞坏死,进一步诱发黄斑变性、阿兹海默症、帕金森症等疾病。
线粒体功能障碍导致细胞能量的缺乏,加上有毒有害物质的毒性作用,会诱发细胞核和线粒体DNA突变,久而久之,就会促进癌症的产生。
总之,过量Omega 6脂肪酸的摄入,几乎是所有现代慢性疾病的「幕后推手」。

04
所有健康饮食
种子油吃得都少
熟悉野兽生活的小伙伴都知道,我们推荐精心搭配、正确执行的生酮、低碳水饮食,同时我们也一直强调,这只是健康饮食的一种,而不是唯一真理。
在我们看来,包括正确执行的生酮、低碳水饮食在内,几乎所有「健康饮食」都有一个共同特点,那就是精炼种子油含量极低。
与标准西方式饮食相比,不管是原始人饮食、地中海饮食,甚至低脂肪素食,都可能改善很多人的健康水平,这些饮食都强调减少omega 6多不饱和脂肪酸(n6 PUFA)的摄入。

北极因纽特人、东非马赛人、太平洋托克劳人、传统法国人的饮食结构富含饱和脂肪,而omega 6多不饱和脂肪酸(n6 PUFA)极低,他们很少有肥胖、糖尿病、心脏病、癌症。
以色列人的饮食结构中,omega 6多不饱和脂肪酸(n6 PUFA)很高,而饱和脂肪较低,他们的肥胖、糖尿病、心脏病、癌症却高于大多数发达国家。

可见,几乎所有健康饮食,都是低精炼种子油饮食。
最后几句
我们今天分享的信息,尽管理论上非常合理,但尚没有得到大规模随机对照试验的证实,因此还不能当做「科学结论」来看待。我们期待的有更多高质量研究,来揭示真正的答案。
但在我们看来,传统「限制饱和脂肪、用多不饱和脂肪代替」的建议,是明显不符合科学与事实的。
这里想再次提醒大家的是,不论是我们的理念,还是主流营养学的观点都有可能是错的。好在,每个人有选择自己饮食和生活方式的权利。
最后复习一下,我们推荐的油脂选择原则是:

参考文献:
[1] Dr. Chris Knobbe. 'Diseases of Civilization: Are Seed Oil Excesses the Unifying Mechanism?'. Low Carb Down Under. https://www.youtube.com/watch?v=7kGnfXXIKZM
[2] Dr. Chris Knobbe. Omega-6 Apocalypse: From Heart Disease to Cancer and Macular Degeneration - AHS19. AncestryFoundation. https://www.youtube.com/watch?v=pHnPinYI2Yc
PUFA-Project: Scientific References on Seed Oil Toxicity
[3] Catherine Shanahan. PUFA-Project: Scientific References on Seed Oil Toxicity. https://drcate.com/pufa-project/
[4] Ben-Dor M, Barkai R. Supersize does matter: The importance of large prey in Paleolithic subsistence and a method for measurement of its significance in zooarchaeological assemblages. In: Konidaris G, Barkai R, Tourloukis V, Harvati K, editors. Human-elephant interactions: from past to present: Tübingen University Press; In press.
[5] Ben-Dor M, Barkai R. The importance of large prey animals during the Pleistocene and the implications of their extinction on the use of dietary ethnographic analogies. Journal of Anthropological Archaeology. 2020;59:101192.
[6] Ben-Dor M, Sirtoli R, Barkai R. The evolution of the human trophic level during the Pleistocene. Yb Phys Anthrop. 2021.
[7] Ben-Dor M, Barkai R. Prey Size Decline as a Unifying Ecological Selecting Agent in Pleistocene Human Evolution. Quaternary. 2021;4(1):7.
[8] Ben-Dor M, Gopher A, Hershkovitz I, Barkai R. Man the fat hunter: The demise of Homo erectus and the emergence of a new hominin lineage in the Middle Pleistocene (ca. 400 kyr) Levant. PLoS One. 2011;6(12):e28689. doi: 10.1371/journal.pone.0028689
[9] Fanaroff A C, Califf R M, Windecker S, et al. Levels of evidence supporting American College of Cardiology/American Heart Association and European Society of Cardiology guidelines, 2008-2018[J]. Jama, 2019, 321(11): 1069-1080.
[10] Astrup A, Magkos F, Bier D M, et al. Saturated fats and health: A reassessment and proposal for food-based recommendations: JACC state-of-the-art review[J]. Journal of the American College of Cardiology, 2020.
[11] Okuyama H, Kobayashi T, Watanabe S. Dietary fatty acids—The n-6n-3 balance and chronic elderly diseases. Excess linoleic acid and relative n-3 deficiency syndrome seen in Japan[J]. Progress in lipid research, 1996, 35(4): 409-457.
[12] Yam D, Eliraz A, Berry EM. Diet and disease--the Israeli paradox: possible dangers of a high omega-6 polyunsaturated fatty acid diet. Isr J Med Sci. 1996 Nov;32(11):1134-43. PMID: 8960090.
[13] Guyenet S J, Carlson S E. Increase in adipose tissue linoleic acid of US adults in the last half century[J]. Advances in Nutrition, 2015, 6(6): 660-664.
[14] Campbell T C, Parpia B, Chen J. Diet, lifestyle, and the etiology of coronary artery disease: the Cornell China study[J]. The American journal of cardiology, 1998, 82(10): 18-21.
[15] García-Serrano, S., Moreno-Santos, I., Garrido-Sánchez, L. et al. Stearoyl-CoA Desaturase-1 Is Associated with Insulin Resistance in Morbidly Obese Subjects. Mol Med 17, 273–280 (2011). https://doi.org/10.2119/molmed.2010.00078
[16] Cohen G, Riahi Y, Sasson S. Lipid peroxidation of poly-unsaturated fatty acids in normal and obese adipose tissues[J]. Archives of physiology and biochemistry, 2011, 117(3): 131-139.
[17] Pan D A, Storlien L H. Dietary lipid profile is a determinant of tissue phospholipid fatty acid composition and rate of weight gain in rats[J]. The Journal of nutrition, 1993, 123(3): 512-519.
[18] Deol P, Evans J R, Dhahbi J, et al. Soybean oil is more obesogenic and diabetogenic than coconut oil and fructose in mouse: potential role for the liver[J]. PloS one, 2015, 10(7): e0132672.
[19] Hall K D, Guo J, Courville A B, et al. Effect of a plant-based, low-fat diet versus an animal-based, ketogenic diet on ad libitum energy intake[J]. Nature Medicine, 2021, 27(2): 344-353.
[20] Penzo D, Tagliapietra C, Colonna R, et al. Effects of fatty acids on mitochondria: implications for cell death[J]. Biochimica et Biophysica Acta (BBA)-Bioenergetics, 2002, 1555(1-3): 160-165.
[21] You M, Fan R, Kim J, et al. Alpha-linolenic acid-enriched butter promotes fatty acid remodeling and thermogenic activation in the brown adipose tissue[J]. Nutrients, 2020, 12(1): 136.
[22] Munro D, Thomas DW. The role of polyunsaturated fatty acids in the expression of torpor by mammals: a review. Zoology. Published online March 2004:29-48. doi:10.1016/j.zool.2003.12.001
[230] Giroud S, Chery I, Bertile F, et al. Lipidomics Reveals Seasonal Shifts in a Large-Bodied Hibernator, the Brown Bear. Front Physiol. Published online April 12, 2019. doi:10.3389/fphys.2019.00389
[24] Chayama Y, Ando L, Sato Y, et al. Molecular Basis of White Adipose Tissue Remodeling That Precedes and Coincides With Hibernation in the Syrian Hamster, a Food-Storing Hibernator. Front Physiol. Published online January 28, 2019. doi:10.3389/fphys.2018.01973
[25] Ailhaud G, Guesnet P. Fatty acid composition of fats is an early determinant of childhood obesity: a short review and an opinion. Obes Rev. 2004 Feb;5(1):21-6. doi: 10.1111/j.1467-789x.2004.00121.x. PMID: 14969504.
[26] Owen OE, Holup JL, D’Alessio DA, et al. A reappraisal of the caloric requirements of men. The American Journal of Clinical Nutrition. Published online December 1, 1987:875-885. doi:10.1093/ajcn/46.6.875
The End
本文作者


本文科学审核

本文 ️ 设计
阿 翔