全球每年1750万人死于心脏病,干细胞如何保护心脏?
如今,全球每年约有1750万人死于心脏疾病,占到了全部死亡人数30%。如何有效治疗心脏疾病对人类的健康保证十分关键。而干细胞疗法相对于其他药物治疗有显著的优势,其治疗本身没有明显副作用非常安全。全球已有多个干细胞治疗心脏疾病临床研究项目正在开展中,那么用于治疗心脏疾病的干细胞种类有哪些呢?他们的治疗机制又是怎样的呢?
发表在《细胞生理学与生物化学》杂志上的一篇综述给出了答案[1],指出治疗心脏疾病的干细胞类型与机制及其改进策略。

用于治疗心脏疾病的干细胞类型
基于文献报道可知,用于治疗心脏病的干细胞类型有多种,主要包括以下几类:
(1)骨骼肌成肌细胞(Skeletal myoblasts):在心脏再生领域中,骨骼肌成肌细胞是第一个在临床前和临床试验中被测试的细胞类型。由于骨成肌细胞易于从自体肌肉组织活检中获得,骨成肌细胞在心脏细胞再生方面已被广泛应用;
(2)骨髓来源的干细胞(BMSCs):是一个异质性群体,包括少量的造血干细胞(HSCs)、内皮祖细胞(EPCs)和间充质干细(MSCs)。2001年,报告的首例患者在心肌梗死后6天采用密度梯度离心方法,从骨髓标本中分离出自体骨髓来源单个核细胞进行了冠状动脉内注射治疗。结果显示,当骨髓来源的单个核细胞移植3个月后,梗死区域显著减少,区域收缩性和灌注性改善。
(3)脂肪来源的干细胞和祖细胞(ASCs):这些细胞的治疗可以显著减少心脏重构和梗死面积以及改善心功能的能力,并且已在各种临床前研究中得到证实。
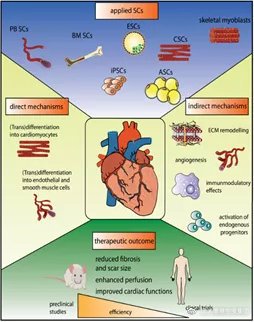
图片来源文献1
(4)心肌干细胞和祖细胞(CSCs):在一项临床1期试验(NCT00893360)中证实了CSCs的好处[2],该试验将心内膜心肌活检组织生长的心脏干细胞送入心肌梗死后左室功能障碍患者体内,可缩小梗死面积,增加存活心肌数量,改善局部收缩力和局部收缩壁增厚。
(5) 胚胎干细胞(ESCs):到目前为止,已经建立了许多不同的体外方案来诱导ESCs向心肌细胞分化,但产生大量纯的和成熟的心肌细胞仍然是一个挑战。
(6) 诱导多能干细胞(iPSCs):遗憾的是目前人类iPSCs还没有达到治疗心血管疾病的临床转化。
近年来,越来越多的研究采用间充质干细胞来治疗心脏病。间充质干细胞广泛存在于人体多种组织中,包括骨髓、脂肪、脐带、胎盘等等组织中。
科学研究已证实,间充质干细胞可以分化为多种细胞类型,包括成骨细胞、脂肪细胞、骨骼肌细胞、胰岛细胞和心肌细胞等。间充质干细胞还被证实能够移植到体内并转化为心肌细胞、修复梗死心肌。动物研究表明,间充质干细胞可以改善心肌功能。
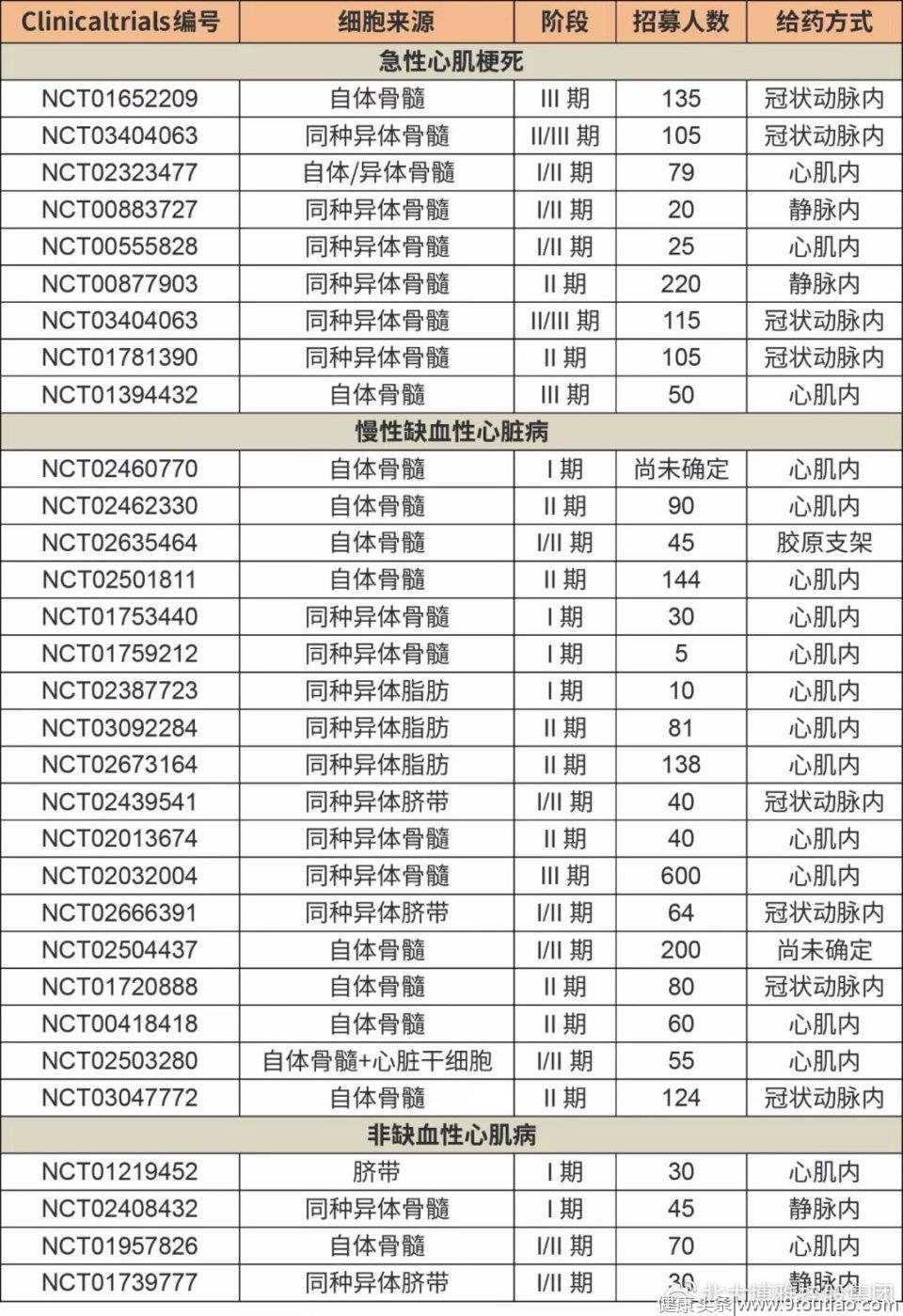
备注:表格内容整理自Stem Cell Translational Medicine,具体项目信息可以利用编号在clinicaltrials.gov网站上查询
目前,全球范围内有多个间充质干细胞治疗心脏病相关的临床试验登记注册在clinicaltrials.gov网站上,具体适应症包括急性心梗和缺血性心脏病,还有一些临床试验使用间充质干细胞来治疗非缺血性疾病,例如蒽环霉素相关性心肌病。在这些临床试验中,绝大多数处在临床II期。
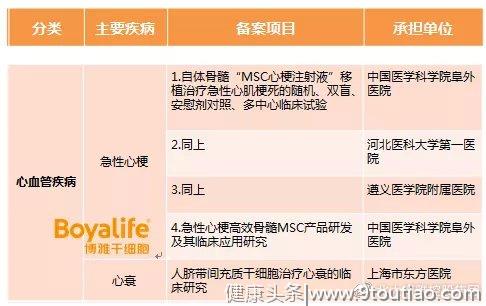
国内,间充质干细胞治疗心脏病的相关临床项目也有多个通过了备案。
干细胞治疗心脏病的机制
科学研究发现,干细胞对损伤组织的修复能力主要有基于间接/旁分泌信号和直接分化两种机制。研究不同类型干细胞控制心肌梗死组织再生的机制,对于治疗心脏疾病的发展和改进具有十分重要的意义。
间接/旁分泌信号机制
目前,人们普遍认为干细胞介导的心肌细胞再生主要机制是可溶性因子的分泌。旁分泌信号通路使干细胞能够通过激活几个信号通路刺激周围的心血管组织。移植的干细胞与祖细胞可分泌转化生长因子、血管内皮生长因子、基质细胞来源因子、表皮生长因子等生物活性分子进入管腔或血流。因此,这些细胞因子或细胞外小泡的释放是一个系统事件,可以促进各种再生过程,如新生血管形成、内源性心肌细胞凋亡的减少、组织内源性祖细胞的激活或有利于组织修复的细胞增殖。
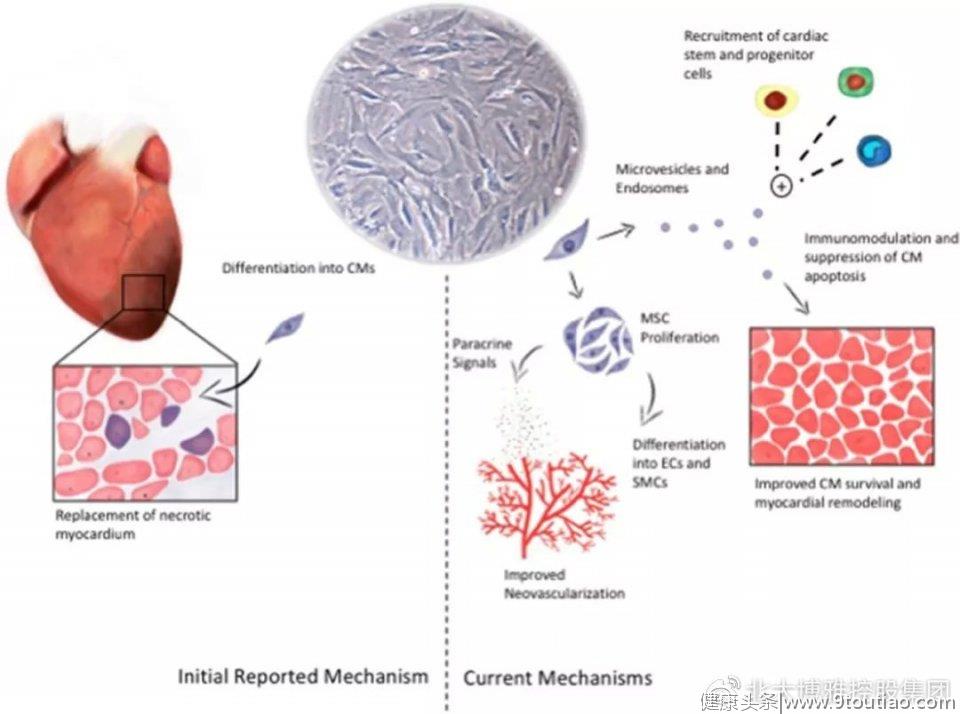
图片来源:Stem Cell Translational Medicine
干细胞直接分化机制
最初,移植的骨髓来源的干细胞被认为有助于受损心肌组织的功能恢复,在获得心肌增生后通过与宿主心肌偶联,并通过直接分化促进新生血管形成。到目前为止,成体干细胞和祖细胞在心脏内转分化为心肌细胞的能力是有争议的讨论。
事实上,一些研究表明,注入的骨髓来源的细胞不仅具有内皮细胞和平滑肌细胞的表型,而且还能转分化为功能性心肌细胞,而另一些研究则反驳了这种说法。这两种机制,转分化和细胞融合都是可导致外周血和脂肪组织来源的干细胞和祖细胞在体内转化为心肌细胞。对于心脏干细胞和祖细胞,关于它们在体内向心肌细胞分化能力的相关数据已经发表。
一方面,一些动物研究表明,这些细胞通过直接分化形成新心肌细胞。另一方面,发现干细胞移植到小鼠心肌细胞后,转分化和细胞融合的发生是相同的。
因此,从大量的体外和体内研究中获得的数据表明,间接/旁分泌信号是介导干细胞治疗有益作用的基本机制。
干细胞治疗心脏病的临床研究及趋势
近年来,全球范围内有多个干细胞治疗心脏病的临床研究项目注册与启动。针对心血管疾病领域的干细胞药物已经问世,更多的干细胞新药正在走来。
2011年,韩国FDA批准Pharmicellon公司(即FCB-Pharmicell)研发的自体间充质干细胞药物Cellgram-AMI上市,用于治疗急性心肌梗死。该疗法成为了全球首个利用自身骨髓间充质干细胞制成的治疗急性心梗的干细胞药物,给药途径为局部冠状动脉注射,每次注射费用为1800万韩元(相当于10万人民币)。

图片来源: Pharmicell官网
2018年,FDA批准BioCardia公司CardiAMP细胞疗法针对慢性心肌缺血(CMI)的临床试验器材豁免(IDE),使其成为利用CardiAMP细胞疗法治疗顽固性心绞痛(RA)的关键性临床试验。
这是一种自体骨髓衍生的单个核细胞制剂,旨在刺激人体在心脏病发作后心力衰竭的自然愈合反应。该疗法目前已经进行到了III期临床试验阶段,将在美国40个中心招募多达260名患者,以评估有效性和安全性,比如评估其能否改善患者的存活率、运动能力和生活质量等。
展望
目前,许多临床试验结果都表明干细胞对于治疗各类心脏疾病都有着良好的效果,而且干细胞疗法在改善患者病情、延长患者寿命以及提高患者生活质量上都有着极大的潜力。不过,干细胞治疗心脏病走向临床应用还需要解决许多问题以及克服未知的挑战。相信随着科技的快速发展,在不久的将来干细胞治疗心脏病可以造福更多患者。
参考文献:
[1] MULLER P, LEMCKE H, DAVID R. Stem Cell Therapy in Heart Diseases-Cell Types, Mechanisms and Improvement Strategies [J]. Cell Physiol Biochem, 2030-2018, 48(6): 2607-55.
[2]MAKKAR R R, SMITH R R, CHENG K, et al. Intracoronary cardiosphere-derived cells for heart regeneration after myocardial infarction (CADUCEUS): a prospective, randomised phase 1 trial [J]. The Lancet, 2012, 379(9819): 895-904.