知其然知其所以然丨听彭永德教授说肠道菌群与糖尿病的那些事儿

目前已公认,肠道菌群在T2DM的发生发展中起重要作用,但具体机制如何?
一方面,肠道的结构以及人体的消化功能都会对能量吸收产生重大影响;
另一方面,肠道菌群及其代谢产物通过“分子对话”的形式调节胰腺、肝脏、脂肪甚至中枢的功能,从而对人体产生影响。

对于T2DM患者来说,可通过哪些方式改善肠道菌群?
◆ 彭永德教授:更确切的说应该是肠道生态环境的正常和恢复,对于患者的健康以及代谢的改善是有重要意义的。
第一,生活方式的干预。合理饮食如选择粗纤维的食物有利于患者改善肠道生态环境;
第二,提供益生菌容易生产的肠道微生态;
第三,药物干预。
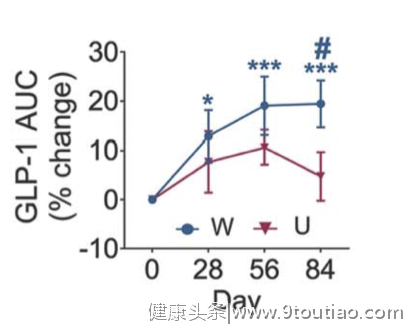
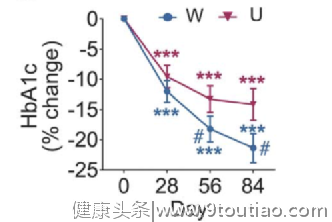
目前,能够改善肠道菌群的降糖药物主要有二甲双胍和α-葡萄糖苷酶抑制剂,其中α-葡萄糖苷酶抑制剂代表药阿卡波糖在肠道菌群方面的循证证据更为丰富。α-葡萄糖苷酶抑制剂主要作用是抑制多糖向单糖的转化,充分剂量的阿卡波糖能抑制复合碳水化合物在肠上皮刷状缘的水解,减少肠道对葡萄糖吸收,造成肠道下部碳水化合物浓度增加,下消化道的细菌就将其分解成短链脂肪酸,从而改善肠道菌群组成,发挥改善肠道内环境的作用。
近年来的多项研究肯定了 α-葡萄糖苷酶抑制剂阿卡波糖对肠道菌群的改善作用,您能否具体谈谈阿卡波糖对于肠道菌群的影响?

上海交通大学附属第一人民医院内分泌代谢科主任、甲状腺疾病诊疗中心主任、骨质疏松症联合诊疗中心主任
中华医学会内分泌学分会副主任委员 基础学组组长、中国老年保健医学研究会老年内分泌与代谢病分会副主任委员、上海市医学会内分泌分会主任委员 基础学组组长、中国医师协会内分泌代谢科医师分会常委、中华糖尿病协会副会长、上海市康复医学工程研究会常务理事、上海市糖尿病康复协会名誉主任委员、上海市松江区医学会内分泌专业委员会主任委员
《上海医学》副主编,《J Clin Endocrinol Metab》杂志编委,《中华内分泌代谢杂志》、《中华糖尿病杂志》、《中华器官移植杂志》、《中国糖尿病杂志》、《中国临床保健杂志》编委,《Metabolism》、《Microbiome》、《J Diabetes & Complications》、《China J Med》及《上海交通大学学报(医学版)》等杂志特邀审稿人
已在国、内外发表学术论文240篇(SCI 60篇,包括Science、PNAS、JCEM等),主编教材专著4部,参编教材专著12部。2004年获教育部科技进步一等奖、2012年获上海市医学科技二等奖,2014获中华医学科技三等奖、华夏医学科技三等奖。2014年获上海市第一人民医院院长奖(医疗),2016年获上海交通大学优秀教师,2018年获上海市第一人民医院院长奖(科研)。