突破固有思维,借力“肾脏排糖”治疗糖尿病
“糖尿”是糖尿病的常见现象,也是糖尿病治疗的新突破口,借助和强化“肾性糖尿”不仅有效降糖,还带来了更多的意外惊喜……
“糖尿”
一种机体应对“能量过剩”的自我保护
正常生理情况下,人体葡萄糖“输入”与“利用”量相等,使葡萄糖水平维持稳定。肾脏将滤过的葡萄糖全部重吸收,尿中不会出现葡萄糖。当血糖水平超出肾糖阈,肾脏葡萄糖重吸收能力达到饱和,导致糖尿的发生。
从能量平衡的角度来看,当体内处于能量过剩状态时,机体会产生一系列的代偿机制,如促进能量消耗,减少食物摄取,从而减少能量累积;产生胰岛素抵抗,血糖水平升高,进而促进多余葡萄糖从尿中排出,减少能量应激对组织细胞的损伤,实现自我的保护。
肾脏葡萄糖重吸收增加
T2DM发病机制八重奏中非常重要的一环
肾脏在葡萄糖处置中有三个关键作用:葡萄糖生成(主要为糖异生,约占内源性葡萄糖生成的20%),葡萄糖利用(禁食状态下,机体10%的葡萄糖在此摄取)和葡萄糖重吸收[钠葡萄糖共转运蛋白2(SGLT2)约负责90%的重吸收量]。
相比非糖尿病人群,T2DM患者肾脏葡萄糖生成和重吸收均增加,同时肾糖阈和最大重吸收量均升高。有研究表明,2型糖尿病患者肾糖阈较健康受试者升高15%,葡萄糖的最大转运值(TmG)较健康受试者升高32%。
另有研究发现,T2DM患者肾小管细胞SGLT2的表达和摄糖能力均增加,是引起葡萄糖重转运能力增加(图),因此导致肾糖阈增加,尿糖在更高的血糖范围内呈现“阴性”,也部分丧失了对能量过剩的保护作用。
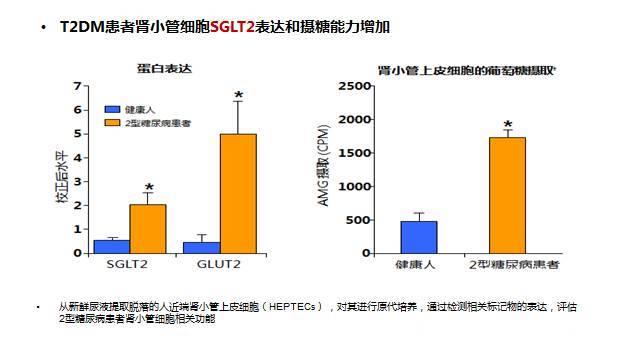
图 T2DM患者肾小管细胞SGLT2表达和摄糖能力增加
借力“肾性糖尿”机制能治疗糖尿病吗?
SGLT2抑制剂从理论走入临床,从家族性肾性糖尿症中获得了重要启示。家族性肾性糖尿症(FRG)是一种罕见家族性不伴有高血糖的“糖尿”病,表现为持续糖尿不伴有高血糖症状、不伴有肾小管功能障碍等症状。
病因主要是SGLT2编码区基因SLC5A2突变导致,FRG分为A、B、O三型,A型TmG降低SGLT2 转运蛋白数量减少;B型TmG正常,但SGLT2 转运蛋白对葡萄糖亲和力降低;O型完全缺乏肾脏葡萄糖重吸收,即使是最严重的O型肾性糖尿患者,在长达15年的持续多尿情况下,也未出现高滤过或微量白蛋白尿的征象,唯一的功能相关改变就是多尿。
家族性肾性糖尿症给我们的启示在于:FRG是一种良性尿糖,主要是SGLT2 基因突变所致,患者仅有尿糖症状,无其他症状,安全性好;表明选择性抑制SGLT2 可以带来血糖降低,不会产生严重不良后果;选择性抑制SGLT2可能成为治疗糖尿病的全新靶点,又一有效降糖武器。
基于这些启示,科学家们对SGLT2抑制剂展开了不懈探索,功夫不负有心人,终于,人们在苹果皮中找到了一种天然抑制SGLT分子的糖苷衍生物——根皮苷(phlorizin,SGLT1和SGLT2的双竞争抑制剂)。经过对根皮苷的无数次结构改造之后,科学家终于锁定了一种“完美”的化合物——达格列净(dapagliflozin),并于2012年11月12日获欧洲药品管理局(EMA) 批准上市,成为全球首个上市的SGLT2抑制剂。2017年3月,达格列净在我国上市,也成为我国首个上市的此类药物。
北京协和医院李航教授对达格列净降糖的病理生理学机制作了详细的介绍:
独特的肾脏排糖机制
不仅有效降低血糖,还能“一举多得”
SGLT2抑制剂可以降低糖尿病患者的肾糖阈,增加尿糖排泄,从“能量过剩”的角度,纠正2型糖尿病的能量失衡,中国人群注册研究显示,达格列净初始单药治疗,降低HbA1c达1.16%, 达格列净10 mg单药降低HbA1c疗效与二甲双胍缓释片2 g 相当,且更显著降低FPG。达格列净通过增加尿糖排泄,多余热量丢失,显著减轻体重(平均减重2.33 kg,超过30%患者体重下降> 5%)和腹围;通过渗透性利尿、利钠等机制,实现降压获益(ACEi/ARB使用基础上,加用达格列净,额外多降4.3 mmHg)。
30万患者真实世界研究显示:使用达格列净SGLT2抑制剂T2DM患者全因死亡风险降低51%,心衰住院风险降低39%。实现减重、降压、改善心血管结局的多重获益。
小结
“糖尿”是人体应对血糖升高的“自我保护”机制,达格列净为代表的SGLT2抑制剂,借力并强化“糖尿”这种创新的自我保护机制,让2型糖尿病患者获得降糖、降压、减重的多重获益,减少患者的心血管事件,改善生存预后。