今日 Nature 重磅:这个意外突变,有望颠覆 CAR-T 治疗!
今日,顶尖学术期刊《自然》在线刊登了一项重磅研究。癌症免疫疗法大牛、CAR- T 疗法先驱 Carl June 教授共同领导的一支科研团队,意外发现了一个可能颠覆传统 CAR- T 治疗的基因突变。它有望让原本治疗无望的白血病患者得到临床治愈。

本研究来自 Carl June 教授共同领导的团队(图片来源:Penn Medicine)
关心医药行业的读者朋友们可能知道,CAR- T 是一类突破性的抗癌疗法。它能分离出患者体内的免疫 T 细胞,在体外进行基因改造,插入识别癌细胞抗原的受体,再输回患者体内。用形象的话说,科学家们给 T 细胞佩戴上了专属的抗癌武器,让它们有效消灭癌症。2017 年,第一款和第二款 CAR- T 疗法相继得到美国 FDA 的批准上市,人类的抗癌史也就此翻开了新的篇章。
创新抗癌疗法的问世,自然离不开严格的临床试验。在这些试验里,一名罹患慢性淋巴性白血病的患者引起了 Carl June 教授等研究人员们的注意。按试验计划,这名患者将进行 3 次 CAR- T 细胞的输注治疗。可是在接受了两次治疗后,他的病情依旧没有得到有效缓解。
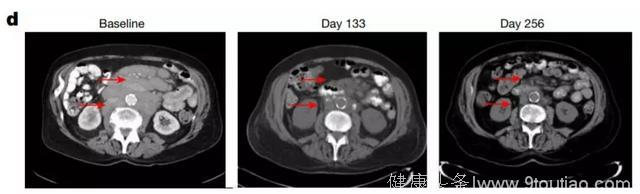
这名患者最终还是出现了病情缓解(图片来源:《自然》)
“直到治疗后的第 50 天,这名患者才出现了细胞因子释放综合征,这表明 CAR- T 疗法终于有了抗肿瘤效果。”该研究的另一名负责人 J. Joseph Melenhorst 教授说道。后续的医学影像分析也证实了这一点。在进行了最后一个疗程的治疗后,这名患者的病情得到了彻底的控制。自 2013 年接受治疗以来,他已经 5 年无癌,达到临床治愈。
尽管取得了理想的治疗效果,但这名患者的曲折经历却让研究人员们百思不得其解。通常来说,CAR- T 疗法要么迅速起效,要么彻底无效,哪有过了 50 多天才突然起效的道理?
“这个治疗效果是我们所期盼的,但我们能从每一名患者身上学到很多东西,” Carl June 教授说道:“我们重新回到了实验室,想尽可能了解背后发生了什么。”
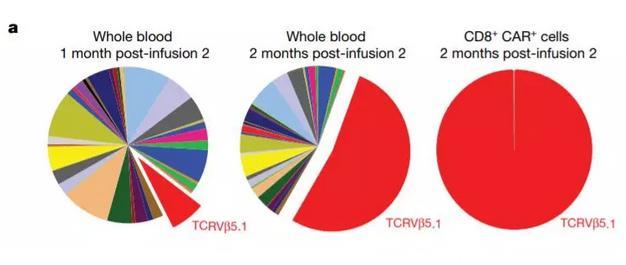
研究发现这名患者的身体里,一类细胞占了统治性的地位(图片来源:《自然》)
对这名患者的分析揭示了一个令人惊讶的事实——在他体内,94% 的 CAR- T 细胞竟然来自于同一个祖先!“这实在是令人惊讶的发现,”该研究的第一作者 Joseph A. Fraietta 教授说道:“这告诉我们,CAR- T 疗法所需的最低剂量,仅仅是一个细胞!”
这个细胞究竟发生了什么?通过测序,科学家们发现在基因改造的过程中,嵌合抗原受体(CAR)序列被意外地插入到了一个叫做 TET2 的基因里。在正常情况下,TET2 控制了血细胞的生成,避免了它们的过度增殖。而一旦 TET2 基因的结构被破坏,这个 CAR- T 细胞就开始快速繁殖,顺便把患者体内的白血病消灭得干干净净。
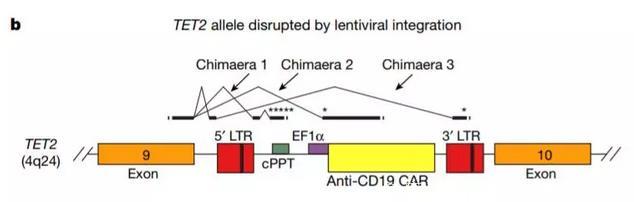
抗 CD19 的 CAR 序列意外插入到了 TET2 基因中(图片来源:《自然》)
为了确认 TET2 基因是 CAR- T 疗法起效的关键,研究人员们用 shRNA 对其表达进行了抑制。果不其然,一旦 TET2 基因的表达水平得到了下调,CAR- T 细胞就出现了显著的扩增。基于在患者中取得的数据,以及体外实验的验证,研究人员们在论文最后指出,TET2 的失活可能有助于产生强力的 CAR- T 细胞。这些细胞不但能快速起效,还能长久生存。他们乐观地估计,或许单个 CAR- T 细胞,就足以有效控制晚期白血病患者的病情。倘若这一案例能得到更多临床试验的重复,无疑将大大缩短 CAR- T 细胞的制备流程,为这一疗法带来革命。
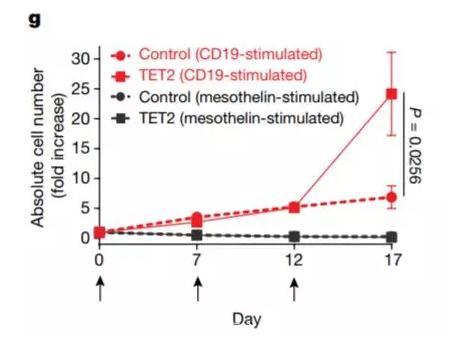
抑制 TET2 的表达可以促进 CAR- T 细胞的增殖(图片来源:《自然》)
科学家们说,这项发现是“一系列小概率事件”带来的奇迹。在机理得到阐明后,我们期待再次见证奇迹的发生!
本文题图来自 Parker Institute
参考资料:
[1] Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells
[2] CLL patient treated at Penn goes into remission thanks to single CAR T cell
本文转载自:学术经纬