两种非小细胞肺癌疫苗Vaxira 和CIMAvax联合治疗晚期肺癌会有更长的生存期吗?
将非小细胞肺癌疫苗与化疗,放疗和其他免疫治疗剂等不同抗癌疗法相结合已经取得了不同程度的成功。 然而,在临床试验中尚未探讨具有不同作用机制的癌症疫苗的组合。
据全球肿瘤医生网报道,目前,肺癌疫苗已经在古巴秘鲁等地批准临床使用应用多年,当地居民免费接受治疗。这种非小细胞肺癌疫苗未在国内上市,全球肿瘤医生网已经与古巴分子免疫中心建立联系,并协助多名患者或家属前往古巴获得非小细胞肺癌疫苗。详情致电或登录全球肿瘤医生网。
由古巴分子免疫中心发表在国际肺癌研究协会(IASLC)的一项研究,主要探讨了在晚期非小细胞肺癌患者中使用两种不同治疗疫苗获得的主要临床和免疫学结果,两种疫苗分别诱导针对表皮生长因子(CIMAvax-EGF)和NeuGcGM3神经节苷脂(Vaxira)的免疫应答。
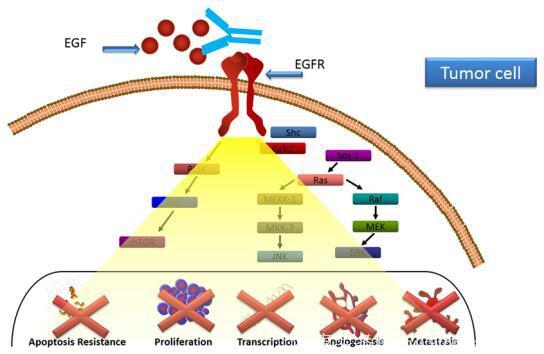
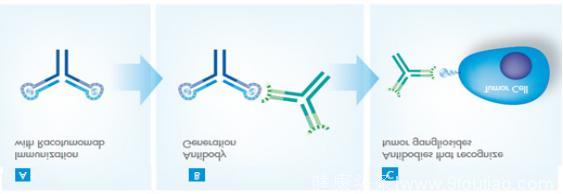
方法
一项探索性的I期研究正在进行,以评估在晚期NSCLC患者中联合使用Vaxira和CIMAvax'EGF疫苗的可行性,并确定对体液免疫应答的影响。根据“肿瘤学治疗指南”(NCCN v.04,2016)建立的标准一线顺铂/双联复合治疗后进展的,20例组织学证实的NSCLC IIIB / IV期患者进行了该项治疗。
疫苗接种计划包括Vaxira/1mg 通过皮内注射。每14天一次连续5次,之后每28天一次,肌内途径连续给予CIMAvax-EGF疫苗0.6mg,每14天一次连续4次,之后每28天一次。施用两种疫苗直到出现难以控制的毒性或患者的病情恶化。通过标准ELISA测定法测定针对Racotumomab抗独特型Mab,NeuGcGM3,EGF抗原,EGF血清水平和对EGF的抑制结合测定的体液免疫应答,通过流式细胞术分析(FACS)和细胞 - 细胞毒性测定法测定特异性NeuGcGM3抗体(IgM和IgG)在NeuGcGM3阳性表达细胞系中诱导细胞毒性。
结果
临床分期纳入包括:IIIB期9例,IV期11例,均为进展期疾病。根据RECIST标准评估疫苗组合抗肿瘤反应,50%的可评估患者在接种12个月(持久的抗肿瘤反应)后达到部分缓解(PR)。经过至少12个月的随访,将20例患者(ITT)纳入生存评估(Kaplan Meier估计)。中位生存期为6,7个月。试验证实这项组合是安全的。仅报告轻度不良事件,主要表现为注射部位反应。与以前的CIMAvax-EGF临床试验相比,获得了抗EGF的更高的抗体效价。所有患者分为GAR(良好抗体应答者)。在接种后2个月循环EGF的完全减少。在第5个月出现了80%的EGFR磷酸化抑制作用。同时也证实了racotumomab的免疫原性。抗独特型反应明显高于以前的Vaxira肺癌试验中获得的最大滴度。抗Neu GcGM3抗体反应的大小和杀死神经节苷脂阳性肿瘤细胞系的能力与以前研究中报道的该疫苗数据相当。
结论
Vaxira和CIMAvax-EGF疫苗的组合具有可接受的安全性。 目前的数据表明,该组合改善了两种疫苗诱导的体液免疫应答,并有益于一线治疗效果不佳的难治性晚期NSCLC患者。 不适合接受一线化疗的NSCLC晚期患者II期/ III期疫苗组合临床试验正在进行中。
据全球肿瘤医生网报道,目前,肺癌疫苗已经在古巴秘鲁等地批准临床使用应用多年,当地居民免费接受治疗。这种非小细胞肺癌疫苗未在国内上市,全球肿瘤医生网已经与古巴分子免疫中心建立联系,并协助多名患者或家属前往古巴获得非小细胞肺癌疫苗。详情致电或登录全球肿瘤医生网。