中山六院学者发现肠癌治疗新靶点;22万人研究再次证实饮酒增多种癌症风险 | 肿瘤情报

Advanced Science:中山大学附属第六医院李孟鸿/方乐堃团队揭示肿瘤治疗新靶点
JAMA Oncology:化疗加贝伐珠单抗不能改善复发性卵巢性索间质肿瘤患者6个月PFS率
BJC:饮酒与多种肿瘤发生风险增加有关,每周饮酒1-3天显著增加乳腺癌发生风险
新药:突破性疗法! 安斯泰来提交的ADC疗法临床申请获CDE受理
新药:康方生物PD-1/CTLA-4双抗被纳入突破性治疗品种
近日,中山大学附属第六医院胃肠病学研究所李孟鸿/方乐堃团队在学术期刊Advanced Science中发表题为“EGF relays signals to COP1 and facilitates FOXO4 degradation to promote tumorigenesis”(EGF信号通过COP1影响FOXO4稳定性调控肿瘤发生发展)的文章。该文章通讯作者为李孟鸿教授和方乐堃副研究员,第一作者为Hyunho Choi博士。
 研究截图
研究截图葡萄糖通过合成代谢近年来已经被发现在肿瘤发生发展中具有重要作用,他们主要通过以下三个方面来促进肿瘤:
通过提供NAPDH/NADH等还原力,清楚肿瘤细胞的氧化应激,使肿瘤细胞更“年轻”。
通过提供SAM原料来调控细胞的表观遗传学,转录和翻译水平调控肿瘤细胞信号通路,促进肿瘤恶性增殖。
肿瘤细胞的快速增殖需要大量的核苷酸原料,葡萄糖摄入增加可以合成核苷酸为肿瘤细胞提供“砖瓦”。然而肿瘤代谢异常的分子机制仍不清楚,靶向肿瘤带代谢通路仍然具有较大挑战。
李孟鸿/方乐堃团队前期研究发现,EGFR通路激活可以上调并稳定CSN6和COP1,以及结直肠癌细胞内的葡萄糖代谢的功能,在促进结直肠癌恶性进展过程中的关键作用,阐述了葡萄糖代谢在结直肠癌中异常的重要原因。
通过深入的机制研究,该文章进一步研究发现,CSN6-COP1可以使FOXO4发生降解。FOXO4能在mRNA水平抑制GLUT1( 葡萄糖转运蛋白)相关基因的表达水平,从而抑制肿瘤对葡萄糖的摄取以及下游的代谢途径。通过中山六院结直肠癌患者的生存曲线显示,高表达FOXO4或者高表达FOXO4合并低表达CSN6的结直肠癌患者的预后更良好。
 从左至右依次为Hyunho Choi博士、李孟鸿教授和方乐堃副研究员2JAMA Oncology:化疗加贝伐珠单抗不能改善复发性卵巢性索间质肿瘤患者6个月PFS率日前,JAMA Oncology在线发布一项临床试验,通过对纳入60例复发性卵巢性索间质肿瘤女性患者的随机临床试验分析显示,每周紫杉醇化疗中加入贝伐珠单抗不能改善患者6个月无进展生存(PFS)率。
从左至右依次为Hyunho Choi博士、李孟鸿教授和方乐堃副研究员2JAMA Oncology:化疗加贝伐珠单抗不能改善复发性卵巢性索间质肿瘤患者6个月PFS率日前,JAMA Oncology在线发布一项临床试验,通过对纳入60例复发性卵巢性索间质肿瘤女性患者的随机临床试验分析显示,每周紫杉醇化疗中加入贝伐珠单抗不能改善患者6个月无进展生存(PFS)率。 研究截图这是第一个针对卵巢性索间质肿瘤的随机临床试验。这项开放标签、国际性、临床II期对照试验(ALIENOR)纳入60名至少1次铂类药物化疗后复发的卵巢性索间质肿瘤患者。患者随机分配至紫杉醇(80 mg/m2,每4周第1、8、15天)或紫杉醇+贝伐珠单抗(15 mg/kg,每三周1次),持续1年或直到疾病进展或出现不可接受的毒性。中位随访时间为38.9个月,单用紫杉醇化疗组患者的6个月PFS率为71%(95%CI 55%-84%),紫杉醇+贝伐珠单抗为72%(95%CI 55%-87%)。添加贝伐珠单抗后,客观缓解率(ORR)从25%(95%CI 12%-43%)提高到44%(95%CI 26%-65%)。1例患者在6个月内因药物毒性停止联合治疗。这项纳入复发性索间质肿瘤患者的国际随机临床试验结果表明,贝伐珠单抗和紫杉醇的联合疗法不能提高临床获益。3BJC:饮酒与多种肿瘤发生风险增加有关,每周饮酒1-3天显著增加乳腺癌发生风险日前,BJC在线发布一项研究,分析了澳大利亚226162名超过45周岁人群的饮酒行为与癌症发生风险之间的关系,发现饮酒与多种肿瘤发生风险增加有关,且饮酒模式是乳腺癌发生风险增加的独立危险因素。
研究截图这是第一个针对卵巢性索间质肿瘤的随机临床试验。这项开放标签、国际性、临床II期对照试验(ALIENOR)纳入60名至少1次铂类药物化疗后复发的卵巢性索间质肿瘤患者。患者随机分配至紫杉醇(80 mg/m2,每4周第1、8、15天)或紫杉醇+贝伐珠单抗(15 mg/kg,每三周1次),持续1年或直到疾病进展或出现不可接受的毒性。中位随访时间为38.9个月,单用紫杉醇化疗组患者的6个月PFS率为71%(95%CI 55%-84%),紫杉醇+贝伐珠单抗为72%(95%CI 55%-87%)。添加贝伐珠单抗后,客观缓解率(ORR)从25%(95%CI 12%-43%)提高到44%(95%CI 26%-65%)。1例患者在6个月内因药物毒性停止联合治疗。这项纳入复发性索间质肿瘤患者的国际随机临床试验结果表明,贝伐珠单抗和紫杉醇的联合疗法不能提高临床获益。3BJC:饮酒与多种肿瘤发生风险增加有关,每周饮酒1-3天显著增加乳腺癌发生风险日前,BJC在线发布一项研究,分析了澳大利亚226162名超过45周岁人群的饮酒行为与癌症发生风险之间的关系,发现饮酒与多种肿瘤发生风险增加有关,且饮酒模式是乳腺癌发生风险增加的独立危险因素。 研究截图结果显示,共17332人确诊为癌症。饮酒增加与上消化道肿瘤(HR 1.19;95%CI 1.10–1.29)、口腔和咽部肿瘤(HR 1.18;95%CI 1.08–1.29)、食管癌(HR 1.22;95%CI 1.04–1.43)、结直肠癌(HR 1.09;95%CI 1.04–1.15)、结肠癌(HR 1.13;95%CI 1.06–1.20)、肝癌(HR 1.22;95%CI 1.04–1.44)和乳腺癌(HR 1.11;95%CI 1.02–1.21)发生风险增加有关。乳腺癌发生风险与饮酒模式有关。与每4-7天饮酒相比,每周饮酒1-3天(与前者相同的量)与乳腺癌发生风险增加有关。因此,研究表明,饮酒与多种肿瘤发生风险增加有关,每周饮酒1-3天显著增加乳腺癌发生风险。4新药:突破性疗法! 安斯泰来提交的ADC疗法临床申请获CDE受理近日,中国国家药品监督管理局(NMPA)药品审评中心(CDE)公示,安斯泰来提交2项注射用enfortumab vedotin的临床试验申请,并获得受理。这是一款靶向Nectin-4的抗体偶联药物(ADC),曾获得FDA授予的突破性疗法认定和优先审评资格,已于2019年底在美国获批上市,用于治疗局部晚期或转移性尿路上皮癌患者。值得一提的是,此次是该产品首次在中国申报临床。
研究截图结果显示,共17332人确诊为癌症。饮酒增加与上消化道肿瘤(HR 1.19;95%CI 1.10–1.29)、口腔和咽部肿瘤(HR 1.18;95%CI 1.08–1.29)、食管癌(HR 1.22;95%CI 1.04–1.43)、结直肠癌(HR 1.09;95%CI 1.04–1.15)、结肠癌(HR 1.13;95%CI 1.06–1.20)、肝癌(HR 1.22;95%CI 1.04–1.44)和乳腺癌(HR 1.11;95%CI 1.02–1.21)发生风险增加有关。乳腺癌发生风险与饮酒模式有关。与每4-7天饮酒相比,每周饮酒1-3天(与前者相同的量)与乳腺癌发生风险增加有关。因此,研究表明,饮酒与多种肿瘤发生风险增加有关,每周饮酒1-3天显著增加乳腺癌发生风险。4新药:突破性疗法! 安斯泰来提交的ADC疗法临床申请获CDE受理近日,中国国家药品监督管理局(NMPA)药品审评中心(CDE)公示,安斯泰来提交2项注射用enfortumab vedotin的临床试验申请,并获得受理。这是一款靶向Nectin-4的抗体偶联药物(ADC),曾获得FDA授予的突破性疗法认定和优先审评资格,已于2019年底在美国获批上市,用于治疗局部晚期或转移性尿路上皮癌患者。值得一提的是,此次是该产品首次在中国申报临床。今年9月,enfortumab vedotin在治疗局部晚期或转移性尿路上皮癌患者的III期临床试验中,达到OS的主要终点。在这项临床试验中,与化疗对照组相比,enfortumab vedotin显著改善了患者的OS,将患者死亡风险降低了30%(HR=0.70,95%CI 0.56-0.89,p=0.001)。
Enfortumab vedotin还显著改善了患者的PFS,将疾病进展或死亡风险降低39%(HR=0.61,95%CI 0.50-0.75,p<0.00001)。该产品在验证性试验中获得的生存结果对于含铂化疗和免疫疗法后疾病继续进展的患者来说是个好消息。
5新药:康方生物PD-1/CTLA-4双抗被纳入突破性治疗品种10月9日,CDE网站公示显示,康方生物AK104注射液已被纳入拟突破性治疗品种公示名单,用于治疗既往含铂治疗期间或治疗后疾病进展的复发或转移性宫颈鳞癌(含腺鳞癌)。AK104是一款PD-1/CTLA-4双特异性抗体,已于今年8月被美国FDA授予快速通道资格。AK104布局的主要适应证还包括肝癌、胃癌、肺癌、食管鳞癌及鼻咽癌等。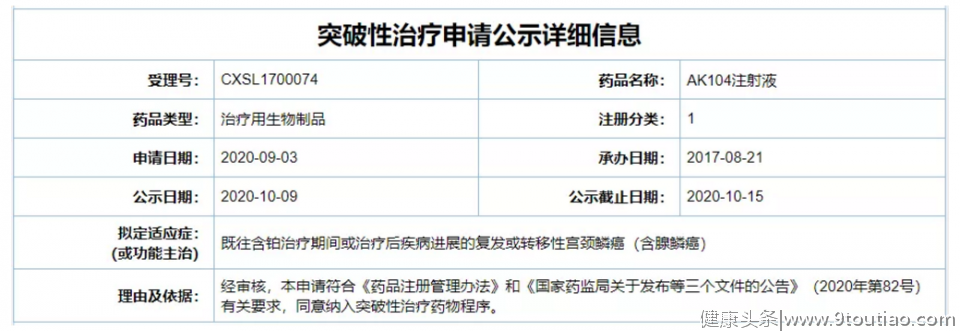
参考文献
1. Effect of Weekly Paclitaxel With or Without Bevacizumab on Progression-Free Rate Among Patients With Relapsed Ovarian Sex Cord-Stromal Tumors2. Alcohol consumption, drinking patterns and cancer incidence in an Australian cohort of 226,162 participants aged 45 years and over3. 中国国家药监局药品审评中心(CDE). Retrieved Oct 10,2020, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=21#4. Seattle Genetics and Astellas Announce PADCEV® (enfortumab vedotin-ejfv) Significantly Improved Overall Survival in Phase 3 Trial in Previously Treated Locally Advanced or Metastatic Urothelial Cancer. Retrieved September 18, 2020, from https://www.businesswire.com/news/home/20200918005101/en5. 中国国家药监局药品审评中心(CDE). Retrieved Oct 09,2020, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=26- End -