传统治疗无效!一种新型抗癌药物在四个月内清除全部肿瘤
天生患有梭形细胞瘤-四个月肿瘤全消失!
5岁的康纳·皮西(Connor Pearcy)在出生时右膝下方就有一个六厘米的肿瘤,他被带到西雅图儿童医院。
活检显示梭形细胞肿瘤具有肌纤维瘤病(一种罕见的良性肿瘤)和婴儿纤维肉瘤(一种罕见的癌性肿瘤)的特征。
医生在康纳(Connor)7周大时开始进行化学治疗,并且持续了一年。然而,化疗并没有像预期的效果那么好,肿瘤只有缩小了一点,停止化疗后,肿瘤又开始生长。医生们进行手术尽可能多地切除肿瘤,但因为腿部的血管直接穿过肿瘤,所以在冒着很大风险手术后的结果也不尽人意,不久后,肿瘤又长回来了。
临床中已经没有更好的解决方案,幸运的是,Connor在接受了基因检测后,他的主治医生Hawkins发现Connor存在NTRK融合,可以参加一种名为LOXO-101的新药。

5岁的Connor Pearcy和他的家人。他的肿瘤对传统疗法无反应,因此参加了一项测试新癌症药物的临床试验。经过四个月的治疗,扫描显示他的肿瘤消失了。
令大家都没有想到的是,两个月后,他的肿瘤惊人的缩小了78%,治疗四个月后的扫描显示体内根本没有肿瘤了。
现在,他每天用一块奶酪服用药物两次,开始正常的上幼儿园,他还可以帮助父母一起照顾两个妹妹,一家人回到了正常的生活轨迹。
获益率91%!全球首款不限癌种的靶向药-拉罗替尼
这款药物是全球首个不区分肿瘤来源用于初始治疗的靶向药--Vitrakvi ®(拉罗替尼,larotrectinib,下文统称拉罗替尼),自2018年11月获批上市以来,给全球肿瘤界的医生和患者都带来了新的希望和选择。
该药的最大看点在于,它是一款针对特定基因突变,而不针对特定癌症种类的抗癌新药。其所能治疗的NTRK基因融合实体瘤包括乳腺癌、结直肠癌、肺癌、甲状腺癌等17种癌症类型,同时对成人和儿童都可以使用。
当然,这款堪称“治愈系”的传奇抗癌药获批的临床数据的疗效更是让人印象深刻:在TRK融合癌患者的临床试验中,拉罗替尼的总缓解率高达ORR为75%,其中22%的患者完全缓解。被批准用于成人和小儿具有神经营养受体酪氨酸激酶(治疗NTRK)基因融合的实体瘤治疗。

2019年ESMO大会上,I / II期SCOUT儿童试验和II期成人/青少年NAVIGATE的篮子试验综合分析的更新数据显示:
在153例可评估的各种肿瘤类型的患者中,该药物的客观缓解率(ORR)为79%,包含24例完全响应和97例部分响应。另有12%的患者病情稳定,这意味该药物的临床获益率高达91%。在108位确诊的患者中,平均的缓解时间长达35.2个月将近三年!此外,平均的无进展生存期为25.9个月,也超过了2年。
“治愈系”靶点--NTRK
相信很多病友想知道这款药物究竟有什么神奇之处,这款药物是只针对个别肿瘤显示出特效还是对所有肿瘤都有效?
首先,这款药物是针对NTRK基因融合的肿瘤。
NTRK(NeuroTrophin Receptor Kinase)是神经营养因子受体络氨酸激酶,包含NTRK1、NTRK2和NTRK3,这个基因如果和其他的基因发生了融合突变,那么就导致了异常的活性,驱动了肿瘤的发生,比如目前,婴儿纤维肉瘤,先天性中胚层肾病和分泌性乳腺癌都显示出ETV6-NTRK3融合,就是ETV6和NTRK3基因发生了融合,以及米歇尔的肿瘤中出现的TPM3-NTRK1,就是TPM3和NTRK1基因发生了融合。
关于这个靶点的治疗,近两年也是肿瘤领域的研发热点,除了拉罗替尼(Larotrectinib)是第一款FDA批准的不分年龄和癌种类型针对NTRK融合的广谱TRK抑制剂,还有2019年上市的恩曲替尼,以及针对一代LOXO-101耐药研发的二代NTRK抑制剂loxo-195,都是抑制酪氨酸激酶的活性!TRK家族蛋白是酪氨酸激酶,如果能抑制激酶活性,就能抑制癌症生长。
因此,想使用这款“治愈系”神药有个硬性条件,必须通过基因检测证实存在NTRK1、NTRK2或NTRK3融合基因的局部晚期或转移性恶性肿瘤。注意只能是融合,NTRK突变或扩增都不适合。
如果说拉罗替尼是一把锁,NTRK基因就是打开这把锁的“生命之钥”,只要有NTRK的融合,相当于是打开了通往治愈之路的大门。
然而这把钥匙却不是每个患者都能获得的。
首先是因为存在NTRK基因融合的患者并不多。比如,在中国常见的肺癌,乳腺癌,结直肠癌中,只有1%~5%的患者存在这种突变,而一些罕见的癌症,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的频率却高达90%~99%。各类癌症存在NTRK融合频率见下表。
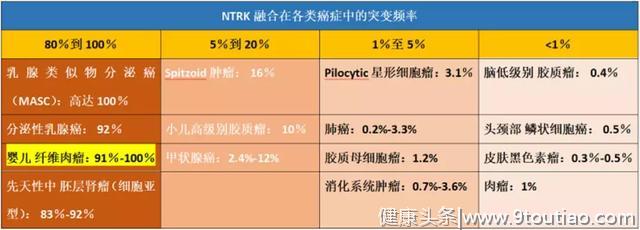
其次,NTRK基因融合容易漏检。研究人员发现,即使您使用非常好的基于DNA的NGS测试,您仍然可以错过其中一些融合。这是因为检测的内含子的长度受限,很难找到这些融合。最好的检测方法是寻找一种既包含DNA,又具有RNA的分析的检测,以便最大限度地提高检测出这些融合的可能性。这并不是国内所有的检测公司都能做到的。
所以,如果大家做了基因检测,可以先看看是否有这些可能带来生存奇迹的突变,除此之外,各类癌症的临床入组条件大家请致电全球肿瘤医生网医学部(400-666-7998)进行初步评估。
拉罗替尼已在这些国家上市!
2018年11月,美国FDA提前批准拉罗替尼上市,用于治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童患者。
2019年9月,拜耳公司宣布,欧盟委员会已在欧盟(EU)授予肿瘤精准治疗药物拉罗替尼的上市许可,该药物适用于治疗局部晚期、远端转移、无法手术切除或手术疗效欠佳的、且无满意替代治疗方案的神经营养性受体酪氨酸激酶(NTRK)基因融合的成人和儿童实体瘤患者。包括德国、法国、意大利等国家均可使用。
2019年1月,LOXO-101(Vitrakvi)在中国申报临床试验(IND),并获得正式受理。根据国家药监局药品审评中心(CDE)网站公开信息,该药品以“硫酸Larotrectinib胶囊”为名称的IND申请由拜耳公司申报,且已经于2019年1月14日获受理,受理信息如下:
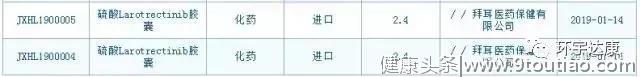
国内患者如何接受拉罗替尼治疗?
虽然拉罗替尼对于特定癌症患者的效果惊人,但目前仅在美国和欧洲上市,2019年1月在中国申报临床试验(IND),并获得国家药品监督管理局正式受理,距离上市也还需要不断的时间。再加上高昂的价格让90%的患者只能望洋兴叹。目前美国的定价为成人每月32,800美元(30天100mg),每年393600美元(约270多万人民币),此价格对于患者来说,堪称天价!某些儿童患者的口服液体制剂为每月1.1万美元,也是国内普通家庭无法承受的。很多患者迫切希望这款药物能在国内开展临床试验。
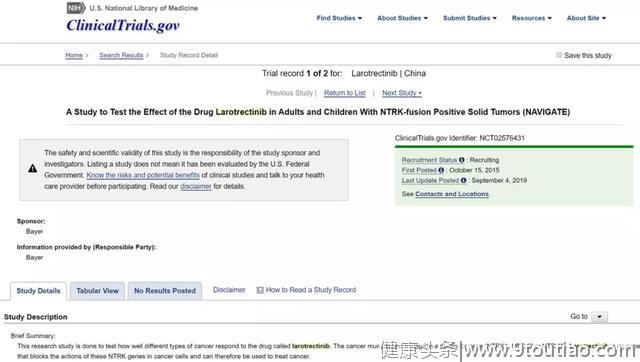
近日,我们在clinicaltrails的官网上看到,目前“治愈系”抗癌药拉罗替尼针对成人实体瘤和儿童实体瘤的两项试验即将在国内开始招募患者了,据业内消息,这项国际多中心的试验中,国内负责招募的医院都在进行最后的伦理审查,相信将很快开始正式的招募工作。
这项试验由国内肿瘤领域权威的几家医院率先开展,评估口服TRK抑制剂拉罗替尼对NTRK阳性的不同种类肿瘤的成人和儿童患者的疗效。
试验分类:安全性和有效性
试验范围:国际多中心试验
做过基因检测的病友,请将报告发送至全球肿瘤医生网医学部,我们的专家将为您全面分析检测报告,评估是否能够入组临床试验,以及有无新药可以使用。
科技的进步,拉罗替尼 Vitrakvi(larotrectinib)等新药物的研发成功是抗癌史上的一次飞跃,我们期待中国也能自主研发这类抗癌特药,将会惠及到更多的中国老百姓。更期盼人类最终完全攻克癌症的那一天,可以少一些病痛,少一些生离死别!
"