胃癌的化疗方案那么多,怎么确定用哪个
胃癌是全世界第四大癌症,也是第二大癌症相关死亡原因。胃癌的发生率有着地区性差异,超过70%的胃癌见于发展中国家。中国的胃癌新诊断病例和死亡病例约占全球的40%。由于胃癌早期筛查工作的缺位,胃癌患者在确诊时通常已到进展期,约占新诊断病例的 40%~60%。
无论是手术后复发的胃癌还是确诊时就已经转移的胃癌,晚期治疗主要采用全身系统治疗,当前主要包括化疗和抗HER-2靶向治疗。其中,抗HER-2靶向治疗仅适用于HER-2阳性的胃癌患者,且曲妥珠单抗只是作为支持铂类和氟尿嘧啶类化疗的附加药物。因此,这里只讨论化疗方案。
 化疗药物的分类
化疗药物的分类晚期胃癌的化疗方案通常由以下几种化疗药物组成。
氟尿嘧啶类:
- 5-FU
- 卡培他滨
- 替吉奥/S-1
紫杉类:
- 多西他赛
- 紫杉醇
蒽环类
- 表柔比星
喜树碱类
- 伊立替康
铂类
- 顺铂
- 卡铂
- 奥沙利铂
根据美国国立综合癌症网络(NCCN)和中国临床肿瘤学会(CSCO)的胃癌指南,晚期胃癌一线治疗可选用双药联合(氟尿嘧啶+铂类)或三药联合(氟尿嘧啶+蒽环/紫杉类+铂类)的化疗方案。
 化疗的疗效如何
化疗的疗效如何评价一种抗肿瘤治疗方案的有效性,主要是参考治疗方案在患者人群中的临床试验结果。通常会评估化疗控制肿瘤的能力和给患者带来的生存获益。前者包括客观缓解率(ORR)、疾病控制率(DCR)、中位缓解持续时间(mDoR);后者包括无进展生存期(mPFS)和中位总生存期(mOS)。
这些指标有具体的定义,但未了方便理解,这里使用了通俗的释义。
- ORR:反映肿瘤缩小的可能性
- DCR:反映肿瘤缩小或稳定的可能性
- mDoR:反映肿瘤持续缩小的时间
- mPFS:反映患者肿瘤不增大的存活时间
- mOS:反映患者存活时间
常用的化疗方案疗效见下表。
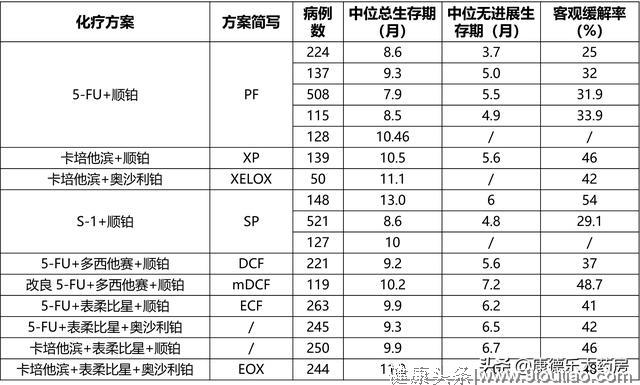 化疗方案是怎么选出来的
化疗方案是怎么选出来的医生在为患者选择化疗方案时通常会从有效性和安全性两个方面考虑,结合患者本身的体能状态选择方案。
根据NCCN和CSCO的胃癌指南,首选的方案是氟尿嘧啶类+顺铂两药化疗,仅次于这种方案的是氟尿嘧啶类+奥沙利铂。顺铂是第一代铂类化合物、疗效强但毒副作用大,需要权衡使用;奥沙利铂是第三代铂类化合物,毒副作用较弱,适用于经评估不适合顺铂的患者。如果患者不适合铂类化疗,还有氟尿嘧啶类+紫杉类和氟尿嘧啶类+喜树碱类的组合可用。
三药化疗的毒副作用通常会大于两药化疗。这也意味着尽管三药化疗对肿瘤的控制更强,但较强的不良反应可能会削弱患者的生存获益。因此,三药化疗适用于体力状况好且肿瘤负荷较大的患者。其中氟尿嘧啶类+紫杉类+铂类的方案可能会略优于氟尿嘧啶类+蒽环类+铂类的方案。
相反,如果是患者体力状况较差或其他不耐受多药化疗的情况,医生会选择氟尿嘧啶类或紫杉类单药治疗。
就目前而言,如果以上一线化疗治疗失败,再使用化疗的获益会大打折扣。在国外,胃癌的二线治疗通常只考虑一线没使用过的药物进行单药化疗或者改用PD-1/PD-L1抗体,但这不是本文介绍的重点。
 化疗之外的出路?
化疗之外的出路?虽然这些化疗药物对晚期胃癌具有一定的临床疗效(胃癌一线治疗ORR为30%~50%),但伴随疗效而来的是较高毒性反应,尽管不会直接抵消化疗的疗效,但最终的结果是患者的生存获益并不理想。
面对这种困境,一条路是追求有效性和安全性齐头并进。但说实话,这种理想治疗方案可遇不可求;另一条路则是接受一定程度的不良反应增加,换取更大的疗效提升,使天平往患者获益的一方倾斜。
这种方案指的就是化疗与免疫检查点抑制剂的联合。
机制研究表明,化疗可促使肿瘤细胞死亡,导致肿瘤抗原递送至抗原递呈细胞的增加;免疫检查点抑制剂与化疗的联合可以通过调节肿瘤细胞/免疫微环境相互作用,产生协同效应,有利于增强或延长免疫系统的抗肿瘤应答。这为开展抗 PD-1/PDL1 抗体药物联合化疗的临床研究提供了理论依据。
在国际学术大会上最新公布的数据也表明,PD-1抗体(纳武利尤单抗/帕博利珠单抗)联合含铂化疗的客观缓解率可提升到60% 以上,中位无进展生存期可达到7.2个月、中位总生存期达到13.8个月。
目前,国内外已有多项PD-1/PD-L1 抗体联合含铂化疗治疗晚期胃癌或胃食管结合部癌(含贲门癌)的临床试验正在开展,成为了当前许多医生和患者追求更优一线治疗的重要选择。
参考文献
中国临床肿瘤学会(CSCO)胃癌诊疗指南 2018.V1
NCCN临床实践指南:胃癌 2019.V1
康德乐大药房联合癌帮帮,为肺癌、甲状腺癌、乳腺癌、外周T细胞淋巴瘤等病人,提供如北京307医院、复旦大学附属中山医院等公立三甲医院的临床招募信息,帮助患者入选,获得免费用药的治疗机会。
可点击下方“了解更多”进行查看!