质子泵抑制剂导致肝癌,风险增加80%!
质子泵抑制剂又双叒叕出事了!这次是肝癌
作者| 姜飞熊
来源 | 医学界
质子泵抑制剂(PPI)又双叒叕被医学研究背后一刀了!这次,英美多所大学的研究者联合发现,质子泵抑制剂竟然还有引发肝癌的风险!

这是啥研究?
这项研究的数据采样来源于英国的“基层医疗临床信息网络”(Primary Care Clinical Informatics Unit ,PCCIU),这个网络收集了基层医疗机构的电子病例和相关档案。
他们采样了苏格兰1993-2011年的PCCIU数据,其中包括患者分布、患者的病程、诊断和治疗等详细信息。此外,他们还从UK Biobank采样了47万人的数据。
这两份数据他们分别进行了研究和分析,分别进行了对照分组。
分组按照年龄、性别、生活环境以及医生的病程记录进行吻合对照,以便排除更多的干扰因素,使得质子泵抑制剂和肝癌的最终统计结果更独立。
结果是啥?
PCCIU的数据分析结果显示,使用PPI的患者其肝癌发生风险与对照组相比,提高了80%以上,而且研究者发现每日用量和使用年限并不会对这个数据产生什么影响。
当然也不是说你在某年某月某一天,就吃了一次,就能有这么高的风险倍数。毕竟有许多使用PPI的患者用药期限都是比较长的……
虽然说用量和时间对肝癌发生没有区别影响,但不同的PPI之间可能会有些区别。比如研究者监测到,使用奥美拉唑的患者,其肝癌发生风险比对照组高83%,使用兰索拉唑仅提高34%。
同时,研究者发现,使用H2受体拮抗剂的患者与对照组相比就不存在肝癌风险升高的情况。
Biobank的数据发现,使用过PPI的患者,其肝癌发生风险是对照组的2倍,也就是大约升高了100%……
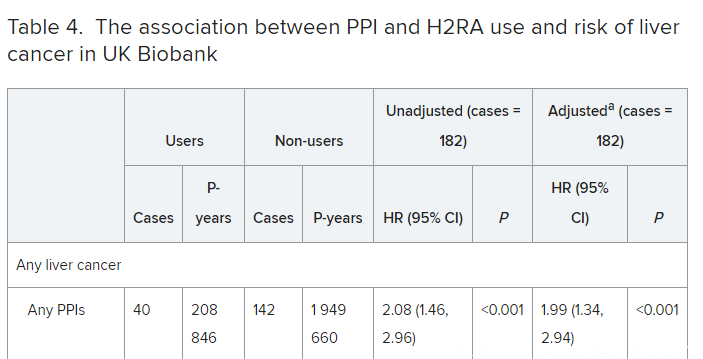
针对Biobank的数据分析
不同的是,Biobank的数据显示,各种PPIs的致癌风险差不多……
原理呢?
数据结果我们知道了,那么PPI导致肝癌风险的原理呢?
研究者分析,PPI有多种机制可能导致肝癌,几年前的动物实验中已经证实,PPI可导致小鼠发生肝脏肿瘤。
其中,最明显的一个机制是,PPI会导致高胃泌素血症,这一症状的致癌性于2015年发表于APMIS杂志,且肝细胞受这一症状影响最大。
另一个可能是,PPI抑制胃酸分泌,导致肠道菌群增长加速,过量肠道菌群使得胆汁酸水平大幅度提高,影响肝脏分泌功能。2017年,Nature子刊上发表过一项动物实验,证实过这种机制。
高水平胆汁酸造成炎症和DNA损害可导致肝细胞和胆管细胞受损,引发癌症。
至于为什么H2受体拮抗剂显示无肝癌风险,研究者认为正是因为其药效不够强,抑制胃酸能力较弱,因此不足以造成上述影响。
研究者还提到,PPI的滥用,尤其是在无清晰说明的情况下的使用,造成的额外损伤不能简单的由机制解释,一些使用PPI的肝病患者或肝癌患者的高死亡率也可能与这种滥用有关。
此外,PPI在肝病的进展中可能本身也有推动作用,今年的另一项关于非肝硬化丙肝患者使用PPI的研究就提示,PPI加速了这些患者肝硬化甚至发生肝癌的过程——

研究者提到,尽管他们在研究中排除了肝硬化患者,但现实中,许多肝硬化患者本身就在长期服用PPI,其肝病预后很大可能要受其影响……
为什么老是PPI中枪?
质子泵抑制剂仅仅是在“医学界”,就已经多次榜上有名了,“再用PPI肾就保不住”“PPI作为胃药竟然引发胃癌”“PPI存在心血管疾病风险”……
倒不是我们“医学界”针对它,主要是医学界的各位研究者追着它呀……当然,人家也不是跟它有仇,毕竟在已经公布这么多风险和副作用之后,这类药品的用量居高不下,自然成为一个大的研究目标。
三年前,“医学界”就刊文指出在临床上PPI的大量使用甚至滥用问题。据相关经济数据,尽管自2008年起,PPI的全球销量开始出现下跌,但在消化性溃疡和胃胀气的使用上,PPI占据了绝对的优势,达87.2%。
据相关药企估测,PPI在中国国内的市场大约200亿人民币/年,2016年,中国医药工业信息中心的统计报告中指出,PPI在中国医院抗消化性溃疡药物采购中占据91.8%的市场份额!

这么大的用量,其中有一个刚性因素,是因为PPI确实好用。尤其是在医患关系紧张的情况下,见效快效果好,也就顾不得后续出现的风险了。
关于这个问题,一位基层医生对“医学界”吐露心声:“知道这个风险多,问题严重,可是用惯了呀,再说真的比别的见效快……”
正如这项研究的作者所说,H2受体拮抗剂风险小,因为它药效不强……
唉。
参考文献
https://www.medscape.com/viewarticle/898227_4
https://www.medscape.com/viewarticle/890621
http://www.cphiic.com/
Fossmark R, Sagatun L, Nordrum IS, Sandvik AK, Waldum HL. Hypergastrinemia is associated with adenocarcinomas in the gastric corpus and shorter patient survival. APMIS. 2015;123:509–514.
Karn W, Panadeekarn P, Charat T, Veeravich J, Ungprasert P. Association between gastroesophageal reflux disease and nonalcoholic fatty liver disease: a meta-analysis. Saudi J Gastroenterol. 2017;23:311–317.
Bosco JLF, Silliman RA, Thwin SS, et al. A most stubborn bias: no adjustment method fully resolves confounding by indication in observational studies. J Clin Epidemiol. 2010;63:64–74.
Llorente C, Schnabl B. The gut microbiota and liver disease. Cell Mol Gastroenterol Hepatol. 2015;1:275–284.
Yadlapati R, Kahrilas PJ. When is proton pump inhibitor use appropriate? BMC Med. 2017;15:36.
UK Biobank. About UK Biobank. http://www.ukbiobank.ac.uk/about-biobank-uk/. Accessed February 2, 2018.
Cole HL, Pennycook S, Hayes PC. The impact of proton pump inhibitor therapy on patients with liver disease. Aliment Pharmacol Ther. 2016;44:1213–1223.
Llorente C, Jepsen P, Inamine T, et al. Gastric acid suppression promotes alcoholic liver disease by inducing overgrowth of intestinal Enterococcus. Nat Commun. 2017;8:1–14
- 完 -
版权申明 |本文原创欢迎转发朋友圈