PD-L1在EGFR突变或ALK重排的肺腺癌中的表达
近年来,随着对遗传驱动因子认识的迅速发展,晚期非小细胞肺癌(NSCLC)的治疗也取得了很大的进展。表皮生长因子受体基因(EGFR)突变,间变性淋巴瘤激酶基因(ALK)重排或ROS1重排的发现,预示了相应的口服酪氨酸激酶抑制剂(TKIs)的潜在疗效,理论上更高效低毒,与传统化疗相比患者生活质量更好。
免疫治疗是治疗NSCLC的新趋势,与传统化疗相比,针对PD-1或其配体PD-L1的免疫检查点抑制剂也为晚期疾病患者带来了新希望。NSCLC患者临床结果的改善与PD-1通路的阻断相关联。尽管许多抗体可用于通过免疫组化(IHC)检测PD-L1表达,但是PD-L1 IHC 22C3 pharmDx分析是唯一批准随行诊断是否可以使用PD-1靶向的单克隆抗体派姆单抗治疗NSCLC的方法。
根据KEYNOTE-024 III期临床试验的结果,随机比较了派姆单抗和铂类化疗,派姆单抗已成为晚期非小细胞肺癌一线治疗的标准选择,PD-L1肿瘤比例得分(TPS)至少为50%。鉴于试验中EGFR突变或ALK重排的患者被排除在外,含有这些致癌基因的NSCLC病例中高水平PD-L1表达的比例仍不清楚。
近日日本科学家回顾性研究分析了2013年1月至2017年11月在九州大学医院诊断并接受过TKI治疗的80例肺腺癌患者(71例EGFR突变,9例ALK重排)。
通过回顾性图表检查获取了每名患者的临床特征,病理数据和肿瘤基因型,同时早期接受TKI治疗的患者的无进展生存期(PFS)也被评估。用PD-L1 IHC 22C3 pharmDx测定法分析PD-L1表达。
试验中患者中位年龄65岁(范围24〜91岁),女性47例(58.8%),非吸烟者48例(60.0%),IV期患者63例(78.8%)。71名患者存在EGFR突变和9名患者发生ALK重排。所有患者均已酌情使用EGFR或ALK-TKI进行治疗。
在所分析的80个肺腺癌标本中,35个(43.8%)具有PD-L1 TPS ≥1%(图1A)。EGFR突变或ALK重排患者的PD-L1 TPS分别见图1B和1C。≥1%的PD-L1 TPS与患者年龄,性别,吸烟史,肿瘤分期,活检部位,活检类型或EGFR或ALK状态无关。
将PD-L1TPS≥1%的患者分成PD-L1 TPS为1%~49%(n = 26,32.5%)或≥50%(n=9,11.3%)的组(图1A)。然而,患者临床病理特征与PD-L1 TPS分层<1%,1%~49%或≥50%未见明显相关性。
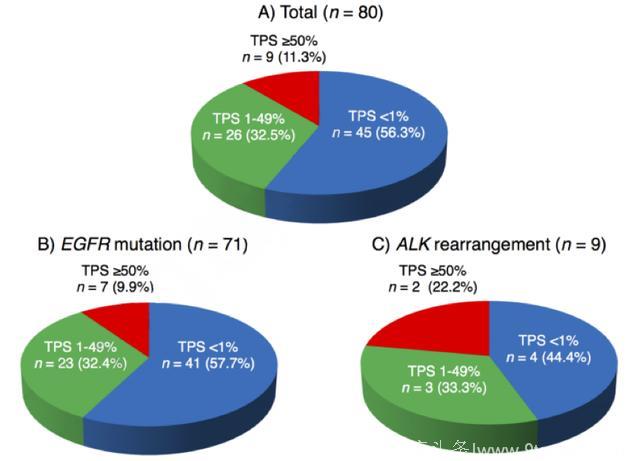
图1 已知致癌因子的肺腺癌患者的PD-L1 TPS
A)具有EGFR突变或ALK重排的所有80个肺腺癌的PD-L1 TPS。
B)具有EGFR突变的71个肺腺癌的PD-L1 TPS。
C)具有ALK重排的9个肺腺癌的PD-L1 TPS。
数据显示,大部分EGFR突变或ALK重排的肺腺癌患者PD-L1 TPS≥1%。那PD-L1表达是否可能是拥有这些驱动致癌基因患者的TKI疗效的决定因素呢?于是研究者接着评估了所有80位有EGFR或ALK-TKI患者的初始治疗的PFS。
对于PD-L1 TPS≥1%和14个月的PD-L1 TPS患者,中位PFS为9个月(95%可信区间6-13个月)<1%。与PD-L1 TPS <1%的患者相比,PD-L1 TPS≥1%的患者PFS明显较差。
对于PD-L1 TPS≥1%的患者,中位PFS为9个月,对于PD-L1 TPS <1%的患者为14个月(图2A)。与PD-L1 TPS <1%的患者相比,PD-L1 TPS≥1%的患者PFS明显较差。
PD-L1TPS≥1%的患者继而被分为PD-L1 TPS为1%〜49%或≥50%的两个组。
根据PD-L1 TPS分层的三组患者的比较显示,随着PD-L1 TPS的增加,PFS倾向于下降。在根据PD-L1 TPS分层的患者之中早期给予TKI的类型没有显著差异。当根据年龄,性别和吸烟史调整回归模型时,PD-L1表达仍然是一个显著的不良预后指标。
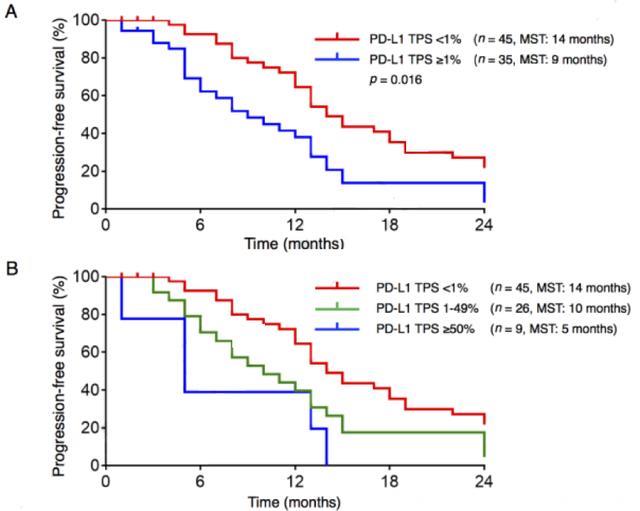
图2患者一线TKI治疗的PFS的Kaplan-Meier生存曲线
A)根据PD-L1 TPS <1%或≥1%的PFS。
B)根据PD-L1 TPS <1%,1%~49%或≥50%的PFS。
这证明了EGFR和ALK信号通路的激活可能能够诱导NSCLC细胞系中的PD-L1表达。另外,先前的研究还揭示了已知驱动致癌基因的NSCLC中PD-L1表达水平的不同。
PD-L1表达水平的这种明显的变化性被认为是由于使用不同的PD-L1抗体和IHC截断值所致。但在EGFR突变或ALK重排的NSCLC患者中,PD-L1 TPS≥50%的频率低于这些基因变化显阴性的频率,PD-1 / PD-L1抑制剂针对PD-L1表达的效果,在EGFR突变或ALK重排的肺癌患者身上比较低。
在这项研究中,有一名PD-L1TPS≥50%的患者接受了PD-1靶向单克隆抗体纳武单抗(nivolumab)的治疗,然而该患者在一个疗程时发生了疾病进展。
虽然肿瘤浸润淋巴细胞(TILs)在免疫检查点阻断反应中发挥重要作用,但在大多数有EGFR突变或ALK重排,同时50%以上肿瘤表达PD-L1的NSCLC中,似乎缺乏高水平的TILs,这一发现可能是PD-1 / PD-L1抑制剂在EGFR突变或ALK重排NSCLC中功效有限的原因。
针对PD-1 / PD-L1抑制剂对EGFR突变或ALK重排NSCLC和PD-L1 TPS≥50%患者的疗效的前瞻性研究是必要的。
EGFR突变或ALK重排的32.9%的肺腺癌患者的PD-L1 TPS为1%~49%,其中43.8%的PD-L1 TPS ≥1%。荟萃分析显示免疫检查点抑制剂对于EGFR突变阳性的NSCLC的治疗效果不如EGFR野生型肺癌。与PD-L1 TPS <1%的患者相比,PD-L1 TPS≥1%的患者早期给予TKI治疗的PFS明显较差。
数据表明,免疫逃逸可能赋予侵袭性肿瘤表型的NSCLC患者更高水平的PD-L1表达,导致TKI治疗的不良预后。当然,该结论仍然是暂时的,因为这项研究是回顾性的,只包括了单一机构招募的相对较小的患者样本。
比如,最近的一项III期IMpower150研究显示,非鳞状NSCLC患者采用atezolizumab联合铂类化疗与单独化疗相比可显著提高PFS。
在亚组分析中,用EGFR或ALK-TKI治疗的EGFR / ALK阳性患者也从联合治疗中获益,表明PD-1 / PD-L1免疫治疗联合化疗可克服EGFR / ALK阳性NSCLC患者的TKI耐药性。
总之,在EGFR突变或ALK重排的肺腺癌患者中测量了PD-L1 TPS≥50%的频率低于之前对没有这些基因突变的肿瘤的频率。但相当大比例的患者PD-L1TPS≥1%。另外,还发现对于早期TKI治疗,PD-L1的高表达与相对较差的PFS表现相关。
上期癌度快报精彩看点
III期结肠癌术后6个月辅助化疗仍然受益;
溶瘤腺病毒延长复发性脑胶质瘤生存期3年;
ALK突变阳性三代靶向药物即将问世;
依维莫司治疗甲状腺癌临床II期显示出治疗效果。
“每天10分钟,癌度快报为您奉上肿瘤领域最新最全的资讯,前沿信息、药物最新临床、群聊经典案例、专家大咖点评面面俱到!我们每天100%的认真和努力,为您的抗癌之路保驾护航!欢迎点击下方“ 了解更多”订阅。”