Science 子刊:双管齐下,顾臻团队带来智能抗癌凝胶
近年来,肿瘤免疫疗法在癌症治疗上取得了历史性的进展,诸多新药研发公司也正在开发免疫疗法组合,提高疗效。今日,《科学》子刊《Science Translational Medicine》(《科学·转化医学》)在线刊登了华人学者顾臻教授团队的一项新研究——他们开发出了一种新型凝胶药剂,能在肿瘤部位依次释放化疗小分子药物和肿瘤免疫疗法大分子抗体,起到抑制肿瘤生长的效果。

本研究的负责人顾臻教授(图片来源:UNC Health Care News)
在介绍这项研究前,我们先来了解一下免疫疗法。在我们体内,每时每刻都有细胞发生突变,产生异常。幸好,我们的免疫系统能将这些异常细胞与健康细胞区分开来,并进行攻击和摧毁。不幸的是,癌细胞利用了免疫系统的这一特性,将自己包装成“良民”的模样。因此,即使这些细胞出现了诸多突变,免疫系统也不会对它们展开攻击,放任它们增殖和生长。
近年来脱颖而出的肿瘤免疫疗法,则能“擦亮”免疫系统的双眼,让它识别并攻击癌细胞。目前最为成熟的肿瘤免疫疗法之一叫做“免疫检查点抑制剂”。通过激活 T 细胞的攻击,这类免疫疗法能有效治疗包括黑色素瘤、肾癌、头颈癌、膀胱癌、以及非小细胞肺癌等一系列疾病。然而免疫疗法也不是万能药。有时,即便用药,肿瘤仍会缺乏被免疫系统识别的特征,从而逃脱免疫细胞的攻击,让其不起效。为此,新药研发人员们期望将免疫疗法与其他抗癌疗法进行结合,起到 1 + 1 大于 2 的效果,对癌症进行更有效的治疗。
先前,临床医生们发现,有时在接受肿瘤免疫疗法的治疗前,倘若先采取化疗治疗,会提高免疫疗法的疗效。这或许是因为被化疗杀死的癌细胞会释放一些分子,让免疫系统变得更为警惕。受此发现的启发,诸多科学家们也正在尝试将化疗药物与免疫疗法结合起来,开发全新联合疗法,以期增强疗效。

这款水凝胶能根据生物环境,释放包裹在内的药物(图片来源:顾臻教授团队)
北卡罗莱纳大学教堂山分校(University of North Carolina at Chapel Hill) 及北卡罗莱纳州立大学(North Carolina State University)的顾臻教授团队带来的这一款创新药剂,是这一领域的最新进展之一。这一材料的主要成分是水凝胶,是一种由聚合物形成的网络结构。其中,我们可以装入多种药物分子。值得一提的是,由这支团队研发的水凝胶具有“智能性”。它能根据生物体中的环境不同,做出相应的变化,比如调控降解的行为,控制药物的释放。
“在体内,生物相容的聚合物(聚乙烯醇)以及对应交联物混合在一起后,能很快地形成凝胶,”这项研究的共同第一作者王金强博士说道:“其中的一款成分能被细胞代谢的自然化学产物 ROS(活性氧类)给切断。”由于肿瘤发育和生长伴随着较高浓度的 ROS,因此研究团队期望在肿瘤附近,高浓度的 ROS 能让凝胶分解,同时帮助释放出包裹在内的药物分子。
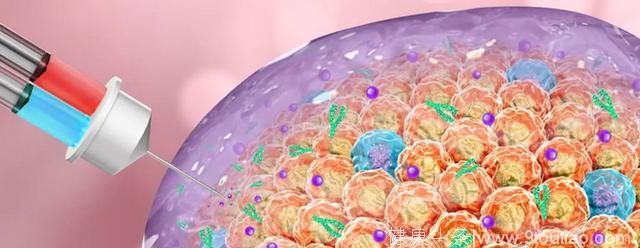
定点注射后,这款材料不但能释放抗癌药物,还能让肿瘤“更为显眼”(图片来源:顾臻教授团队)
具体说来,研究人员们将化疗药物吉西他滨(gemcitabine)和一款抗 PD-L1 抗体一道包裹在了这款凝胶内。当这些凝胶被注射入肿瘤病灶处后,就会在 ROS 的影响下逐渐降解,同时先释放出分子量较小的吉西他滨,再释放出 PD-L1 抗体,起到先化疗、再免疫治疗的效果。更有意思的是,这款凝胶自身的特性还能够让肿瘤看起来“更为显眼”,引起免疫系统的注意,帮助免疫细胞在病灶处会合,从而提高免疫疗法的效果。
“具有细胞毒性的化疗会首先杀死一些癌细胞,从而增加肿瘤对免疫检查点抑制剂的敏感度,这会进一步提高免疫检查点抑制剂疗法的效果,”该论文的共同作者 Gianpietro Dotti 教授说道:“与此同时,当水凝胶降解后,肿瘤内的 ROS 水平会下降,也会帮助抑制肿瘤生长。”
这支科研团队在动物模型中测试了这款凝胶药剂的潜力。在 B16F10 黑色素瘤与 4T1 乳腺癌模型中,这款创新药物递送技术能有效让肿瘤微环境对治疗更为敏感。当药物从中释放后,肿瘤体积也显著减小。除了缩小肿瘤体积外,这款材料还能有效防止肿瘤复发——研究人员们在肿瘤的手术切除部位加入了这款水凝胶。后续结果表明,癌症的复发得到了明显的抑制。
“我们结合肿瘤生物学、免疫治疗药物以及化疗药物,开发出了这样一款简单的局部注射、联合给药的新方法。它能够有效地抑制癌症发展,并可降低系统给药的副作用,”该研究的通讯作者顾臻教授说道:“在启动人体试验前,我们还有很多工作要做。但我们认为这款疗法很有潜力。”
按计划,顾臻团队将进一步优化药物的剂量,并寻找到最佳的治疗频率。同时,顾臻教授表示会系统评估这款凝胶药剂的医用安全性,由此带来更多的潜在临床新疗法。
参考资料:
[1] New therapeutic gel shows promise against cancerous tumors
[2] In situ formed reactive oxygen species–responsive scaffold with gemcitabine and checkpoint inhibitor for combination therapy