“获批24次,覆盖8种癌症”,免疫检查点抑制剂的前世今生!
研发历程
肿瘤免疫检查点抑制剂是目前肿瘤免疫治疗(Immuno-oncology,I/O)药物治疗的最主要方面,通过抑制肿瘤细胞的免疫逃逸,调动自身免疫系统功能消除肿瘤。
肿瘤免疫检查点抑制剂的研究主要集中在CTLA-4、PD1、PD-L1三个分子上。
CLTA4发现最早,是由法国人Pierre Goldstein在1987年无意中发现了T细胞上的一个分子,当时还是集中在免疫学方面的研究,并没有想到其在肿瘤中的作用;
PD1则是在1992年由日本人Tasuku Honjo发现的,跟CTLA-4的发现一样,当时也只认为多发现了一个细胞编程性死亡相关的蛋白而已,并没有引起太多重视;
直到1997年,由华人学者陈列平发现PD-L1(当时还被称为B7-H1)对免疫反应发挥负调节的作用,而且是肿瘤组织特异的一种蛋白,这才是PD1/PD-L1免疫检查点抑制剂能够实现肿瘤临床治疗的第一步,陈列平教授在这方面做出了杰出贡献。
CTLA-4的免疫抑制作用研究却比PD1/PD-L1早先一步,这一杰出贡献是由纪念斯隆凯特琳癌症中心的James Allison在小鼠试验中证实的,CTLA-4也就成为了第一个发现的免疫检查点蛋白分子,而James Allison则是开启肿瘤免疫检查点抑制剂应用的开创者。
由于CTLA-4主要分布在T细胞上,而且其配体并不具有肿瘤组织特异性,阻断CTLA-4会激活全身免疫系统,副作用太强,针对CTLA-4的Ipilimumab作为第一个获批的免疫检查点抑制剂药物,目前仅在2011年获批于黑色素瘤及在2015年作为晚期黑色素瘤的辅助治疗,目前还没有更多临床应用进展。
在PD1/PD-L1的研究中还有一位重要人物就是哈佛的Gorden Freeman,他与Tasuku Honjo一起在2000年发现PD-L1就是PD-1的配体,两者结合可以抑制T细胞的增殖和细胞因子的分泌,负调控淋巴细胞的激活,并在2001年发现另一个PD-1的配体PD-L2,其功能和PD-L1类似。2003年,陈列平教授首次在活体实验证明抑制PD-L1可以治愈约60%的患有头颈癌的小鼠,这也是第一次成功在活体中证明抑制PD-L1对肿瘤T细胞治疗获益。
基于这些前期研究的不断推进,才有了后期临床广泛的应用。在2013年肿瘤免疫治疗因其对于常规疗法无效的晚期肿瘤患者具有显着疗效,被 Science评为年度十大科技突破之首。
从2014年开始截止到目前已经批准的PD1抑制剂百时美施贵宝的Opdivo(Nivolumab)、默沙东Keytruda(Pembrolizumab),PD-L1抑制剂罗氏的Tecentriq(Atezolizumab)、默克/辉瑞共同开发的Bavencio(Avelumab)以及新进入场的阿斯利康Imfinzi(Durvalumab),总共五种单抗类药物,在FDA累积获批22次,覆盖八种癌种(如果MSI作为分子标志物也算一种癌种的话)。
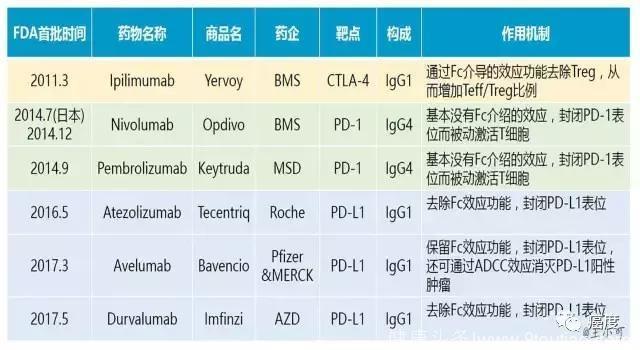
无论国外各大药企的快速推进还是国内药企III期药物研发,都有多种针对PD1/PD-L1的药物竞争各适用症的临床试验,相信最近几年还会有更多药物或适用症获批,可以说是已经进入了肿瘤免疫治疗的黄金时代。
获批适用症情况
BMS在20世纪90年代就已开始PD1的研究,在2009年收购于Medarex获得Opdivo与Yervoy后在免疫检查点抑制剂领域发力,并逐渐成为该领域的领头羊。
在2014年7月,BMS公司的PD1单克隆抗体药物Opdivo在日本获批上市,成为全球第一个抗PD-1的上市药物,该药物在美国到12月获批上市。而竞争对手默沙东公司的Keytruda在9月成为美国第一个获批的抗PD-1药物,激烈的竞争一开始就已经展开。

Opdivo从开始一直处于领跑的位置:
目前已经拿下8个适应症的批文;
同时BMS公司是同时拥有两个免疫检查点抑制剂药物的公司,对Opdivo与Yervoy联用已被批准用于晚期黑色素瘤患者;
除此之外,还凭借专利优势坐享对Keytruda专利税,在2016年仅凭销售额就达到37.74亿美元。
Keytruda近期也有不俗表现:
2017年5月这一个月内连续拿下三个适应症,成为目前获得适应症批文最多的肿瘤免疫治疗药物;
并且有针对三种适应症获批用于一线治疗,是目前免疫治疗中进入一线最多的药物,尤其在NSCLC的一线治疗获得压倒性胜利;
凭借生物标志物的筛查,如PD-L1及MSI作为患者分类的明确依据,使获益患者更易被区分从而获得更快的获批速度。
虽然Keytruda在2016年销售额只有14.02亿美元,但中途发力不可小觑,与Opdivo的竞争也会日渐激烈。
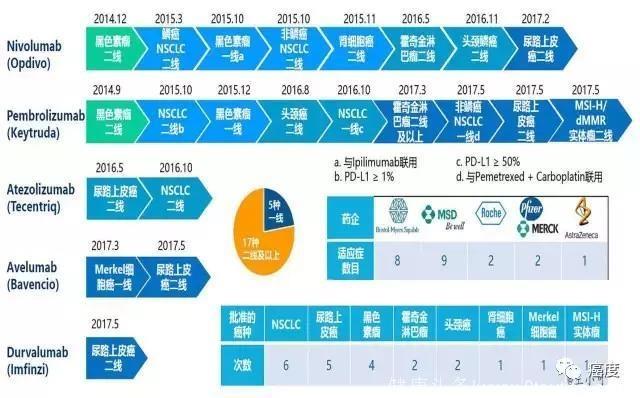
在PD-L1单抗方面,罗氏的Tecentriq是第一个获批用于抑制PD-L1的单抗,于2016年5月批准用于铂类药物不敏感或治疗失败的尿路上皮癌患者,并且也已经进入NSCLC的二线治疗。
2017年3月默克/辉瑞共同开发的Bavencio首先获批用于Merkel细胞癌,是免疫治疗药物第一次批准用于该癌种,该药物也获批用于尿路上皮癌的二线治疗。
阿斯利康的Imfinzi是PD-L1药物中最新获得FDA批准进入的药物,也是获批适用于尿路上皮癌的二线治疗。
目前大多数免疫检查点抑制剂都获批用于相应适用症(共17次)的二线治疗,有5次获批进入一线治疗中,其中有两种是通过联合用药的方式,
一种为免疫-免疫药物的联合,即Opdivo与Yervoy联合用于晚期黑色素瘤患者;
一种为免疫-化疗药物的联合,即Keytruda与培美曲塞+卡铂联合用于NSCLC的一线治疗。
另有一种是通过标志物的筛选,即PD-L1≥50%表达水平的NSCLC患者,可以从Keytruda的一线治疗中获益。其余两种分别是Opdivo用于晚期黑色素瘤的一线治疗及Bavencio获批用于Merkel细胞癌的治疗。
从进入一线治疗的免疫治疗我们可以看出,通过更有效的联合用药以及生物标注物的筛选获益人群会是免疫治疗的临床推进方向,在今年的ASCO会议中我们也看到很多免疫-免疫、免疫-靶向、免疫-化疗、免疫-放疗以及免疫-手术的报道,这都在推进免疫治疗的应用,丰富临床治疗方案的选择。
在获批的适用症中,NSCLC是占比最多的,总共有6次,其中三次由Keytruda占据,且有两次获批一线治疗。
尿路上皮癌是目前全部五种PD1/PD-L1药物都获批的适用症,可能该癌种肿瘤突变负荷较高有关。
Opdivo和Tecentriq首次获批的适应症都是晚期黑色素瘤,并且都各有两次获批,黑色素瘤也是非常适合用免疫治疗的癌种。
头颈癌和经典型霍奇金淋巴瘤也分别由Opdivo和Tecentriq各获批一次,Tecentriq是首个获批用于头颈癌的免疫检查点抑制剂,Opdivo则是免疫检查点抑制剂类药物中首先获批用于血液肿瘤的。肾细胞癌和Merkel细胞癌分别获批一次。
MSI作为首个不区分癌种的获批标志物具有划时代的意义,Keytruda在该适用症获批主要会使有高频MSI-H的结直肠癌、子宫内膜癌、胆道癌等癌症患者获益。
生物标志物
免疫检查点抑制剂治疗通过近三十年的研究及临床应用,已有越来越多的患者从中获益,然也并不是对任一患者都有疗效,筛选出可预测治疗效果和不良事件的生物标志物是一项至关重大挑战。
目前已有两项PD-L1免疫组化的伴随诊断获得FDA批准,5月份获批的MSI-H/dMMR是癌症治疗史上的突破性事件,也愈加凸显生物标志物在免疫治疗中的应用。
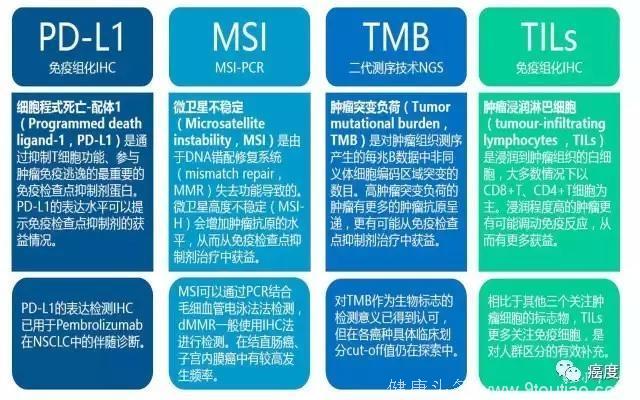
肿瘤与免疫系统的微环境构成情况是免疫治疗的关键,寻找到肿瘤细胞以及免疫细胞中的特异性标志物才能更好地预测免疫治疗的效果。
PD-L1
PD-L1是肿瘤细胞实现免疫逃逸的主要因素,通过抑制其作用实现调动免疫系统杀死癌细胞是免疫治疗的核心。在患者肿瘤组织检测到PD-L1高表达可以说明该肿瘤较多依赖免疫逃逸机制,通过阻断PD-L1通路可以去除逃逸效果,激发免疫系统识别并杀死癌细胞。
MSI
由于DNA错配修复基因(主要包括MLH1,MSH2,PMS2,MSH6等)的功能缺失会造成微卫星位点不稳定性增加,也就是MSI-H。微卫星位点可能位于编码区或是调控区,这会导致错误的氨基酸序列的产生,最终导致肿瘤新抗原的呈递,从而更多的被体内免疫细胞识别。
TMB
肿瘤突变负荷TMB与MSI提示的原理基本一致,也是因为高TMB的肿瘤有更多的肿瘤新抗原,会吸引一堆免疫T细胞到肿瘤中。TMB的情况与肿瘤中基因突变情况有很大的关系,POLE、POLD1、BRCA1/2、MMRs等DNA修复基因突变的胚系或体细胞突变往往会有很高的TMB;而在常见驱动突变如EGFR、ALK基因突变占优势的肿瘤中TMB往往较低,这类患者更多需要接受靶向治疗,从免疫治疗中可能获益较低。
与TMB一个比较相似的概念是TNB,也就是肿瘤新抗原负荷(Tumor Neoantigen Burden)是从蛋白层面跟直接的检测肿瘤表面抗原的呈递情况。
TILs
以上三种标志物都是从肿瘤细胞中预测可能获益可能,而从免疫细胞浸润情况也是很重的一个方面,通过检测浸润到肿瘤里的CD8+、CD4+的T细胞密度TILs,也可以提示免疫系统接触抑制后的活跃情况。
然而这些因素在其生物功能上是相互联系的,并且在个体肿瘤标本中经常是并不是同时出现,在免疫药物获批比较多的NSCLC和黑色素瘤中,根据TCGA数据库显示这两个癌种有很高的TMB,然而MSI水平低于各癌种的平均水平;子宫内膜癌、胃癌及结直肠癌则同时具有很高水平的MSI和较高的TMB。
通过进一步明确这些生物标志物之间的关联及区别,可以帮助我们更好地认识癌症免疫治疗,而目前对多种生物标记物的综合考量可能比单独的标记物能提供更好的疗效预测价值。
编者:王小可