中轴型脊柱关节炎,TNFi助力实现更高的治疗目标 | 前沿进展
*仅供医学专业人士阅读参考
axSpA 是一种炎症性、进展性疾病,病程中的炎症、脂肪性病变和新骨形成可持续进展,导致患者整个病程中出现以背痛为主的症状。axSpA晚期治疗可控制炎症,但新骨形成和脂肪变性控制不理想。故需更早且持续控制炎症。
GO-RAISE研究是第一个评估戈利木单抗治疗活动性AS疗效和安全性的全球性III期研究,研究纳入经改善病情抗风湿药(DMARDs)或非甾体抗炎药(NSAIDs)治疗后的活动性AS患者,评估戈利木单抗治疗活动性AS患者的疗效、依从性及安全性。结果[4-5]显示:
- 整体研究人群的Bath强直性脊柱炎病情活动指数(BASDAI)评分改善在戈利木单抗治疗5年期间持续存在(图1)。
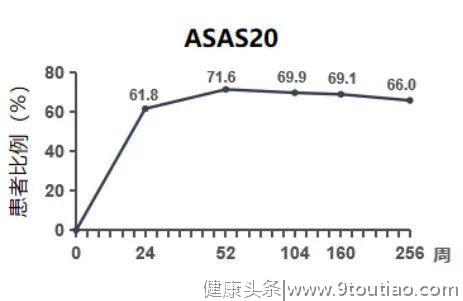
- 戈利木单抗持续治疗5年仍可获得较高的ASAS 20 应答率(图2)。

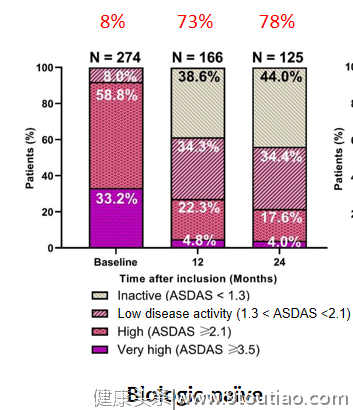
- 使用戈利木单抗治疗2年,近80%生物制剂初治患者的AS新疾病活动指数(ASDAS)<2.1(图3)。
- 无论是否曾用过生物制剂,戈利木单抗都能有效降低AS患者疾病活动度(图4)。
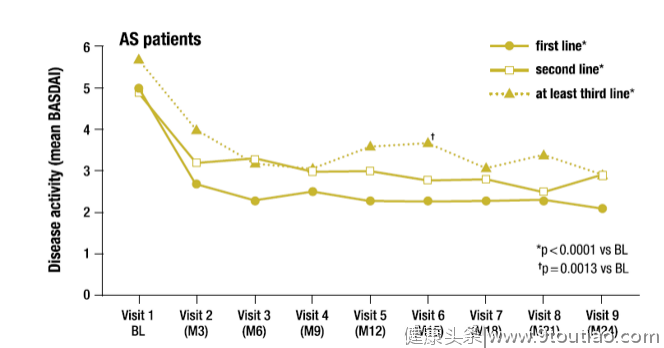
- 使用戈利木单抗作为一线、二线或三线生物制剂治疗,AS患者疾病活动指标均获得显著改善(图5)。

TNFi除了控制疾病活动度这个基本目标外,对终极目标——提高生活质量上亦有很大的帮助。炎症和/或骨沉积导致的功能损害,可对患者的健康和生活质量产生深远影响。2019美国风湿病学会(ACR)/美国脊柱炎协会(SAA)指南[9]指出治疗目标:
- 尽可能缓解症状、改善功能、维持工作能力、减少疾病并发症和防止骨骼损伤。
最新研究发现,TNFi可降低/抑制结构损伤、维持骨骼正常功能、改善axSpA患者的生活质量。
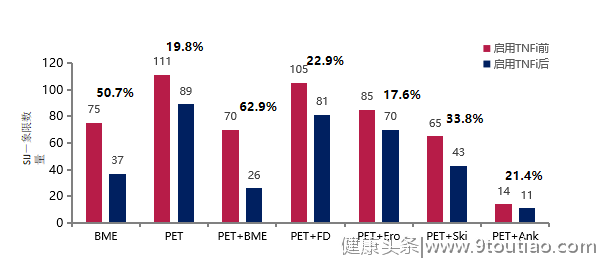
注:BME:骨髓水肿的骶髂关节数;PET:PET using bone-seeking F-Fluoride [18F]F;PET+BME:同时有PET 18F聚集和骨髓水肿的骶髂关节数;PET+FD:同时有PET 18F聚集和脂肪沉积的骶髂关节数;PET+Ero:同时有PET 18F聚集和骨侵蚀的骶髂关节数;PET+Ski:同时有PET 18F聚集和硬化的骶髂关节数;PET+Ank:同时有PET 18F聚集和强直的骶髂关节数。
另一项研究[11]纳入53名接受戈利木单抗治疗的axSpA患者,所有受试者在接受戈利木单抗治疗的第0、4、16和52周接受全身磁共振成像(WB-MRI)检查。根据加拿大脊柱关节炎研究协会MRI骶髂关节关节炎症评分、加拿大-丹麦MRI脊柱炎症评分和MRI周围关节以及附着点炎症评分,进行影像学评估戈利木单抗治疗axSpA患者的应答和缓解率。研究发现:戈利木单抗治疗axSpA患者可以显著降低WB-MRI下炎症。
戈利木单抗治疗第4周、16周、52周分别有30、39和41例(57%、74%和77%)患者达到简易Boolean MRI 应答(在脊柱关节、骶髂关节、外周关节和附着点炎三个方面,至少有一个指标应答≥50%)。
52周时,43例(81%)患者C-反应蛋白达到正常水平,18例(34%)患者获得ASAS部分缓解,20例(38%)患者获得ASDAS无疾病活动;与无应答患者相比,达到BASDAI 50或ASDAS-CII临床应答的axSpA患者,骶髂关节和脊柱关节MRI炎症显著降低,周围关节和附着点MRI炎症降低更为明显。
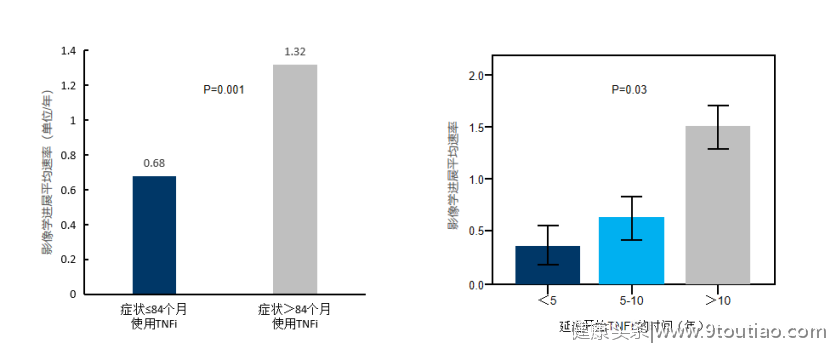
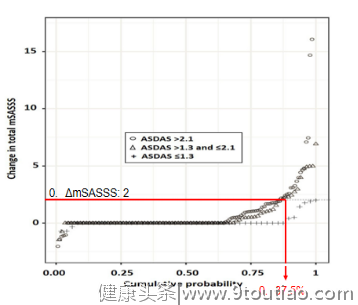
图8 AS患者接受戈利木单抗治疗的影像学进展减少
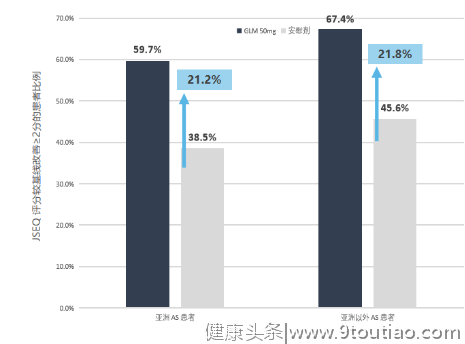
不止如此,GO-UP研究[17]显示,戈利木单抗在真实世界中可显著改善axSpA患者劳动生产力与日常活动。GO-NICE研究[18]显示:戈利木单抗有效改善患者健康评分、功能评分、疲乏评分。聚焦AS关节外表现,全面管理axSpA的治疗2019 EULAR指南及2020中国台湾风湿病学协会指南均建议根据疾病体征和症状、特征和治疗目标进行个体化及多学科治疗。axSpA第一年关节外表现常见,如心血管、肾脏、肺部异常、急性前葡萄膜炎(AAU)、银屑病。
一项研究[19]共纳入93例患者(65%男性,55%未接受过TNFi治疗,27%有AAU病史),在戈利木单抗治疗期间,AAU发生率从11.1例/100患者年降至2.2例/100患者年(率比0.20,95%CI 0.04-0.91)(图10)。
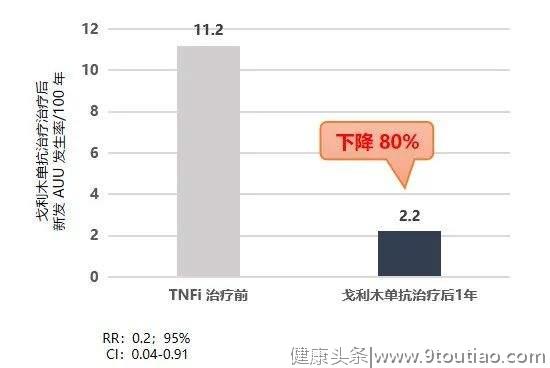
在AS中,戈利木单抗治疗期间AAU发生率和疾病活动度显著下降。因此,戈利木单抗可被认为是需要TNFi的AS患者的良好选择,尤其是在复发性AAU病例中。2020年最新发表的研究[20]发现,英夫利西单抗和戈利木单抗是改善银屑病关节炎有效的生物制剂。4总结axSpA是一种炎症性、进展性疾病,持续高疾病活动度与疾病进展和生活质量降低密切相关,放射学及MRI的数据表明TNFi 能有效抑制放射学进展,早期使用TNFi 以及长期使用TNFi都与放射性学进展降低相关,axSpA 疾病管理的终极目标——提高生活质量,是通过对影像学进展的有效控制获得的。
参考文献:
[1] Poddubnyy D, Sieper J. Curr Rheumatol Rep. 2017 Sep;19(9)55.
[2] https://max.book118.com/html/2018/0606/171088298.shtm
[3] Ole Haagen Nielsen , et al. N Engl J Med. 2013 Aug 22;369(8)754-62.
[4]Braun J, et al. Ann Rheum Dis. 2012 May;71(5):661-7.
[5]Deodhar A, et al. Ann Rheum Dis. 2015 Apr;74(4)757-61 supplement.
[6]Flipo et al (2019). ACR abstract 1499
[7]https://acrabstracts.org/abstract/golimumab-persistence-in-biologic-naive-and-non-naive-patients-with-axial-spondyloarthritis-results-of-the-go-practice-study/
[8]Klaus Krüger , et al. Rheumatol Ther. 2020 Jun;7(2):371-382.
[9]Arthritis Rheumatol. 2019 Aug 22.
[10]2020 EULAR SAT 0365
[11]Rheumatology 2020;59:3358–3368doi:10.1093/rheumatology/keaa153
[12] Jeong H, et al. Int J Rheum Dis. 2018 May;21(5):1098-1105.
[13] Haroon N, et al. Arthritis Rheum. 2013 Oct;65(10):2645-54.
[14]Molnar C, et al. Ann Rheum Dis. 2018 Jan;77(1):63-69.
[15]https://www.sohu.com/a/427742855_377336
[16]Wen-Chan Tsai,et al.Improvements in Patient-reported Outcomes in Ankylosing Spondylitis (AS) Patients Treated With Golimumab: Subanalysis of Asian Patients Enrolled in Phase 3 Clinical Trials,APLAR 2020.
[17]Athanassiou P, et al. EULAR 2020 #SAT0630-HPR
[18]Klaus Krüger, et al. Rheumatol Int. 2019; 39(1): 131–140.
[19]van Bentum RE, et al. J Rheumatol. 2019 Feb;46(2):153-159.
[20]Adeline Ruyssen-Witrand, et al. RMD Open. 2020 Feb;6(1)e001117