如何实现类风湿关节炎的“持续缓解”?专家有话说
达标治疗策略应用于类风湿关节炎(RA)治疗以来,越来越多RA患者因此受益。近年来,RA治疗手段的进步,推动了RA治疗目标的进阶。“持续缓解”的概念应运而生,为RA治疗带来了更严格的治疗目标。
2020北京医学会风湿病学分会学术年会于11月20日-21日在北京会议中心盛大召开。会上,中国医科大学附属第一医院杨娉婷教授为参会专家带来了题为《浅尝辄止还是继往开来——RA持续缓解从哪里来到哪里去?》的学术专题报告,深入探讨了RA"持续缓解"这一概念的由来与发展,介绍了RA领域治疗手段的进步。医学界特撷取精华,以飨读者。
从ACR70到持续缓解
2010年欧洲抗风湿病联盟(EULAR)首次提出达标治疗理念[1],成为新时代RA治疗史上一座重要的里程碑,让越来越多的RA患者从中获益。《2018中国类风湿关节炎诊疗指南》在中国指南中首次明确了RA达标治疗的理念[2],为中国RA治疗的临床实践提供了更清晰的指导。RA的治疗经历了漫长的发展阶段,新世纪来RA治疗正式步入生物靶向时代,其治疗目标也随之发生了巨大的变化。早期关键临床研究终点对临床缓解的重视度不高,美国风湿病学会制定的70%疾病改善标准(ACR 70)是优先考虑的研究终点。TEMPO研究结果启示,相当部分患者在ACR 70应答时仍有较高的疾病活动度,不能很好识别患者疾病缓解,而DAS及DAS28缓解患者疾病活动度更低[3]。为实现更深度的RA缓解,风湿病学术界对临床缓解标准的定义进行了大量的探索。2011年,发布于Annals of the Rheumatic Diseases的一篇文章中,作者对RA的临床缓解标准的变迁进行了总结(表1)[4]。
表1 RA临床缓解标准的变化
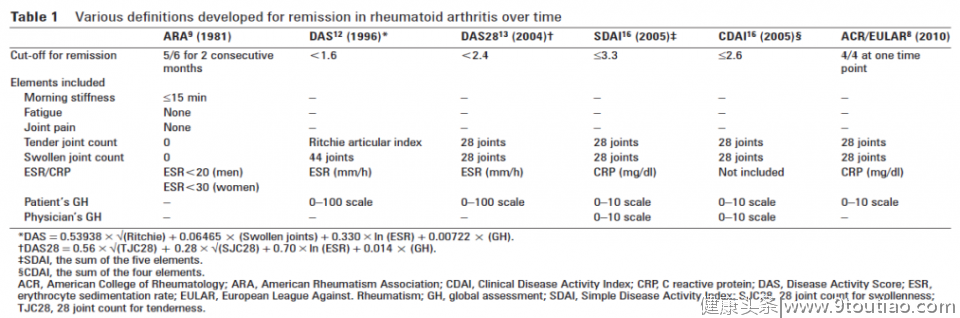
目前,国内外权威指南均推荐达标治疗策略,并强调应尽早实现并长期维持缓解。
一项研究随机选取ASPIRE、ATTRACT、DE0 19、ERA、Leflunomide、PREMIER与TEMPO研究中605例持续至少6个月获得临床缓解(DAS28-CRP2.6或SDAI≤3.3)的患者数据,评估6个月期间患者生理功能的改善情况。结果显示,患者健康评估问卷(HAQ评分)随着DAS-CRP及简化疾病活动指数(SDAI)缓解持续时间改善(图1)。
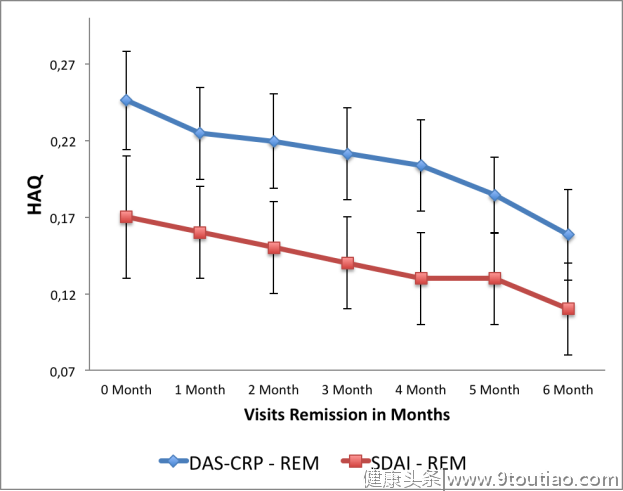
另外,DAS28-CRP缓解组达到完全功能恢复(HAQ=0)患者比例高达42.5%,SDAI缓解组达50.1%。早期RA患者相较于长期RA患者,获得HAQ=0的比例更高[(DAS28-CRP:47.6%;SDAI:52.6%)VS(DAS28-CRP:33.3%;SDAI:44.1%)]。研究证实,随着RA患者达到临床持续缓解,其生理功能不断改善[5]。更严格的缓解标准决定了达到缓解的患者可获得更好的功能改善。
多项研究表明,早期及持续的缓解能为RA带来近期与远期的获益。
一项由M.Verstappen团队完成的系统综述结果显示,在获得缓解后改善病情抗风湿药物(DMARDs)逐渐减量的RA患者中,疾病复发率为41.8%~75.0%。值得注意的是,停药缓解持续大于5个月的患者复发率为10.4%~11.8%,而停药缓解持续至少一年以上的患者疾病复发率为0.3%~3.5%[6]。另一项研究共纳入2045名早期RA患者,根据DAS 28分类进行分组,随访25年,观察大型骨科手术的累计发生率,结果表明,高疾病活动度RA患者(DAS 28>5.1)进行大型骨科手术的累计发生率显著高于临床缓解组(DAS 28≤2.6)(HR:2.48;95%CI:1.50–4.11)[7]。此外,RA持续缓解可以减少患者心血管疾病(CVD)风险。多中心、前瞻性、观察性的挪威 DMARD 登记中心NOR-DMARD研究共纳入3251例RA患者,旨在比较缓解和非缓解RA患者的CVD风险,并比较使用生物制剂达标和使用传统抗风湿药物(csDMARD)达标的RA患者CVD风险。结果显示,临床缓解的RA患者其CVD风险显著低于非缓解患者。使用生物制剂达标的患者其CVD风险低于csDMARD达标的患者,但差异无统计学意义[8]。然而,目前RA持续缓解尚无统一定义。EULAR 2019指南指出:"目前没有关于‘持久’的定义,因为尚无研究探讨过3个月、6个月还是12个月的严格缓解,哪个更符合持续缓解的定义[9]。"不同研究中对持续缓解的定义存在一定差异。比如TEMPO研究对持续缓解的三种标准为[10]:
2.持续的DAS缓解:DAS缓解连续达6个月;
瑞典风湿病管理质量登记的持续缓解定义为:在一种缓解标准下,在6个月以上至少两次诊所随访都是缓解状态,每个患者的首次缓解计入持续缓解,即一个患者只能计一次持续缓解[11]。如何实现持续缓解?
一项前瞻性观察性研究纳入了2007-2017年间2097例早期RA(<1年)患者,分析在临床实践中实现持续缓解的情况(间隔≥6月两次连续随访均DAS 28<2.6),结果显示,40%患者实现持续缓解,提示早期RA患者在临床实践中实现持续缓解是可行的[12]。早期缓解对持续缓解同样具有重要的意义。对869例RA患者进行回顾性研究,分析6月内实现不同标准早期临床缓解的患者与未早期缓解患者的持续缓解率,分析早期缓解的预测因素,结果显示,6个月内实现早期缓解的患者中实现持续缓解的比例显著更高(图2)[13]。
一项回顾性研究纳入779例中国RA患者,分析持续缓解(≥6个月)的发生率,并分析持续缓解的预测因素,结果显示随访期间,42.4%~51.6%患者实现持续缓解,表明中国RA患者中持续缓解并不罕见,持续缓解的预测因素包括更早缓解、应用达标治疗策略、病程、基线临床的疾病活动指数(CDAI)等[14]。
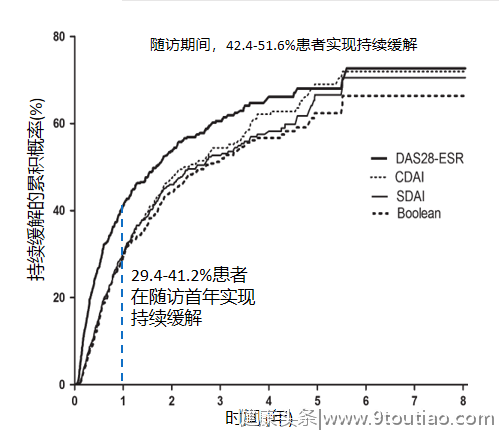
新世纪来,多种生物制剂的问世改变了RA的治疗与管理模式,为RA患者带来了新的希望。一项研究入组了100名使用csDMARD达到临床缓解的RA患者,这些患者被随访了2年,每4个月进行一次评估,如果在随访中出现未达标,则依次采用以下升级治疗方案:
- 增加csDMARD单药/联合剂量(n=73);
- 加用一种TNF抑制剂(n=39);
- 换用另一种生物类改善病情抗风湿药物(bDMARDs)(n=21);
- 无变化(n=58);
表2升级治疗至bDMARDs相比csDMARD,可更加有效的改善MRI炎症表现,关节功能及疾病活动度

阿达木单抗助力持续缓解达标
阿达木单抗(修美乐)为全球首个全人源IgG1型抗TNF-α单克隆抗体,誉为全球药王。
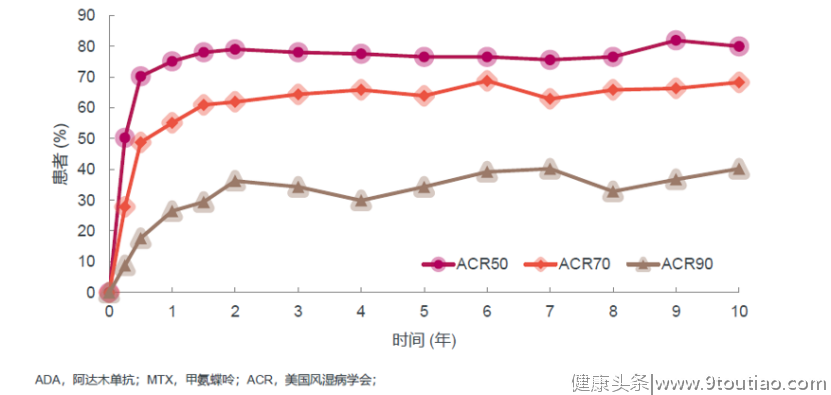 图4 PREMIER研究结果DE019研究共纳入407例中重度RA患者,分别接受阿达木单抗40mg隔周1次+MTX(n=207)或安慰剂+MTX(n=200)治疗52周。主要终点包括52周时的放射学进展、24周时的ACR 20和52周时的功能水平。结果显示,阿达木单抗组患者52周时改良Sharp评分自基线改变2.7,相比安慰剂组显著较高,SF-36评分改善同样显著高于安慰剂组(图5),表明阿达木单抗治疗RA患者可强效抑制放射学进展,且持续改善RA患者生活质量[18-19]。
图4 PREMIER研究结果DE019研究共纳入407例中重度RA患者,分别接受阿达木单抗40mg隔周1次+MTX(n=207)或安慰剂+MTX(n=200)治疗52周。主要终点包括52周时的放射学进展、24周时的ACR 20和52周时的功能水平。结果显示,阿达木单抗组患者52周时改良Sharp评分自基线改变2.7,相比安慰剂组显著较高,SF-36评分改善同样显著高于安慰剂组(图5),表明阿达木单抗治疗RA患者可强效抑制放射学进展,且持续改善RA患者生活质量[18-19]。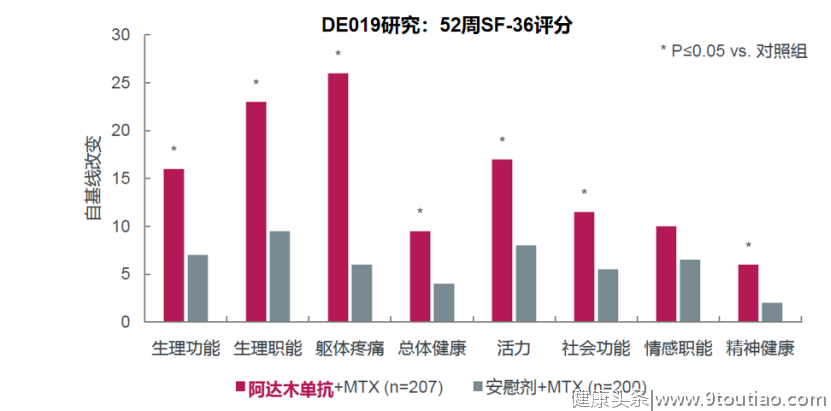 图5阿达木单抗治疗持续改善RA患者生活质量真实世界研究数据进一步证实阿达木单抗有益于RA患者实现持续缓解。英国风湿病学会的生物制剂治疗RA登记研究(BSRBR-RA)纳入2001-2013期间启动首个抗TNF治疗的14436例RA患者,其中2144例在随访期间实现持续DAS28-ESR缓解≥6个月,使用多变量逻辑回归分析以调查持续临床缓解的预测因素,结果显示,抗TNF治疗为RA实现持续缓解的预测因素(表3)[20]。表3英国BSRBR-RA研究长期(12年)数据分析
图5阿达木单抗治疗持续改善RA患者生活质量真实世界研究数据进一步证实阿达木单抗有益于RA患者实现持续缓解。英国风湿病学会的生物制剂治疗RA登记研究(BSRBR-RA)纳入2001-2013期间启动首个抗TNF治疗的14436例RA患者,其中2144例在随访期间实现持续DAS28-ESR缓解≥6个月,使用多变量逻辑回归分析以调查持续临床缓解的预测因素,结果显示,抗TNF治疗为RA实现持续缓解的预测因素(表3)[20]。表3英国BSRBR-RA研究长期(12年)数据分析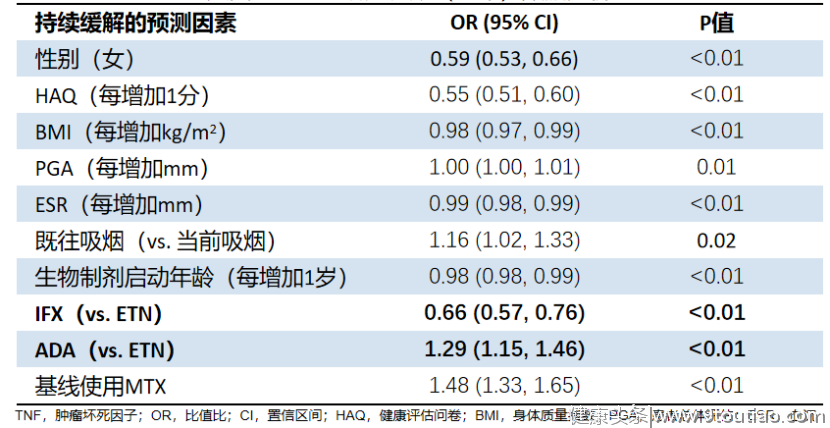
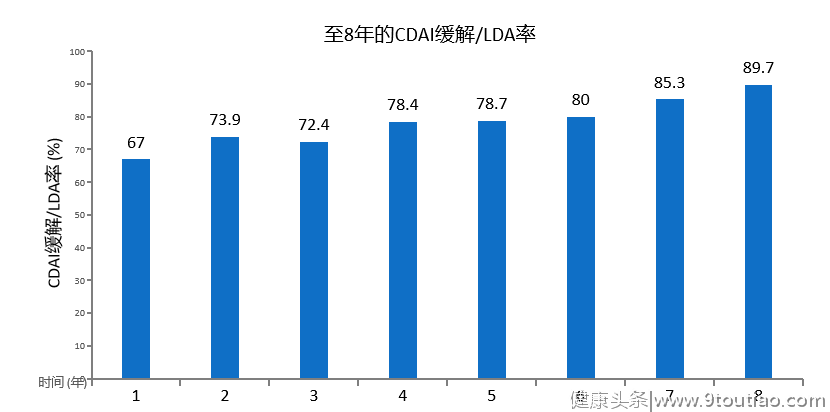 图6阿达木单抗治疗大部分RA患者长期维持缓解
图6阿达木单抗治疗大部分RA患者长期维持缓解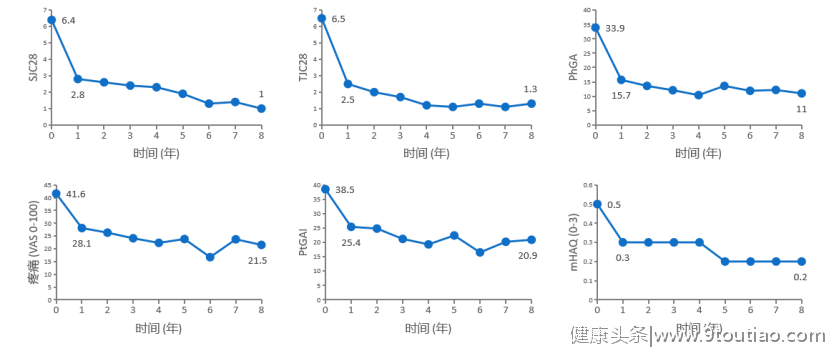
图7阿达木单抗可长期改善RA患者的关节症状、PRO、肢体功能
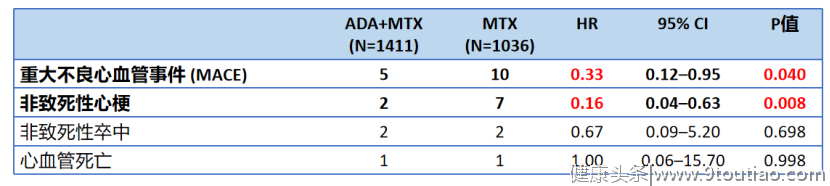
表4阿达木单抗显著降低RA患者的心血管事件风险
04
专家总结
报告最后,杨娉婷教授指出,虽然目前RA持续缓解尚无统一定义,但持续缓解为RA患者带来的近期及远期获益毋庸置疑。初始生物制剂强化治疗、早期缓解以及药物安全性是实现持续缓解的重要因素。
*上述内容仅代表专家临床观点

杨娉婷 教授
中国医科大学附属一院 风湿免疫科主任、辽宁省狼疮脑病重点实验室主任、院党委副书记,辽宁特聘教授,首届辽宁青年名医。
中华医学会风湿病学分会常委,中国医师协会风湿免疫科医师分会常委,海峡两岸卫生医药交流协会风湿免疫专业委员会常委,辽宁省医学会风湿病分会候任主任委员。
1991年考入中国医科大学六年制日语医学班。
主要从事狼疮脑病的机制研究,承担国家自然基金项目2项,以第一或通讯作者发表SCI源期刊论文23篇,累计90分。
以第一申请人获得省级科技进步二等奖两项,辽宁省医学科技二等奖一项。主编教材3部,副主编及参编国家统编教材4部。
参考文献:
[1]Smolen JS, et al. Ann Rheum Dis. 2010 Apr;69(4):631-7.