美国风湿病学大师Roy Fleischmann教授分享类风湿关节炎治疗心得
不想错过界哥的推送?
戳上方蓝字“医学界风湿免疫频道”关注我们
并点击右上角“···”菜单,选择“设为星标”


Roy Fleischmann教授
曾获得美国风湿病学大师(ACR Master)称号
《风湿病学》副主编
美国德克萨斯大学西南医学中心临床医学教授
德克萨斯州风湿病协会和达拉斯-沃斯堡风湿病协会主席
Roy Fleischmann教授在750多项类风湿病学领域的临床研究中担任主要或联席研究员,主要研究类风湿关节炎、骨关节炎、强直性脊柱炎、痛风、疼痛管理和骨质疏松症。Roy Fleischmann教授撰写了100多篇以类风湿关节炎治疗为重点的论文及200多篇论文摘要,另外还担任《风湿病年鉴》、《关节炎和风湿病》及《风湿病学》审稿专家。
传统合成改善病情抗风湿药物(csDMARDs)是类风湿关节炎(RA)治疗的基石,亦是国内外指南共同认可的一线药物。尽管甲氨蝶呤(MTX)是公认的治疗RA的锚定药,但仍有1/3RA患者对MTX治疗应答不佳,不能有效地达到治疗目标[1]。对 于 经MTX、来氟米特或柳氮磺吡啶等单药规范治 疗 疗 效 不 佳 的 患 者 ,后续的治疗方案应如何选择呢?
在2019亚洲炎症与免疫学峰会(2019 ASIA REACH)上,来自美国德克萨斯大学西南医学中心的Roy Fleischmann教授通过一则病例为我们深入探讨、解答了这个问题。

Roy Fleischmann教授大会发言
01
病例回顾
患者28岁,是个非常喜欢旅行的女性。
2012年3月,患者掌指关节、近端指间关节、跖趾关节、腕关节肿痛。次月,膝关节、踝关节受累。
2012年5月,患者出现多关节肿痛,临床疾病活动指数(CDAI)32,基线DAS28-ESR评分 6.1(根据红细胞沉降率[ESR]计算得到的28关节疾病活动评分),患者健康调查问卷(HAQ)1.375。ESR 58mm/h,C反应蛋白15mg/L,类风湿因子阴性,抗环瓜氨酸肽抗体(抗-CCP)阳性,胸部及关节X片未见异常,中度贫血,血生化正常,肝炎病毒、HIV抗体阴性。
治疗方案:给予泼尼松 10mg/d+MTX 20mg/w +叶酸 1mg/d。
2012年8月,患者在服用MTX后出现严重恶心及疲劳感,肝酶升高,CDAI 6,基线DAS28-ESR评分 2.8,健康调查问卷残疾指数(HAQ-DI)0。
治疗方案:因为患者出现药物不良反应,故暂停MTX数周。
2012年9月,患者病情恶化,CDAI 28,基线DAS28-ESR评分 5.5,HAQ 1.0,肝功能正常。
治疗方案:重新给予MTX 15mg/w治疗,患者尚能耐受。
2012年12月,患者CDAI 16,基线DAS28-ESR评分 4.3,HAQ-DI 0.75,未出现药物不良反应。
2013年3月,患者出现恶心症状,肝酶升高,CDAI 16,基线DAS28-ESR评分 4.1,HAQ-DI 0.875。
治疗到此,Fleischmann教授产生了疑问,后续对于这名患者最佳治疗策略该是什么呢?
①继续目前的治疗?但患者存在明显MTX不良反应,MTX耐受性差,不可再继续目前的治疗;
②停用MTX,采用来氟米特、柳氮磺胺吡啶和羟氯喹联合方案?可能有效;
③启动生物制剂DMARDs联合MTX?不可选,MTX安全性、耐受性仍存在问题;
④生物制剂DMARDs单药?但大多数生物制剂DMARDs仍需联合MTX使用;
⑤靶向合成DMARDs(JAK抑制剂)单药治疗?患者经常旅行,口服给药更便捷,并且已有研究证实JAK抑制剂(托法替布)具有与生物制剂同等的治疗地位,若患者对MTX不耐受或不适合MTX治疗,可考虑作用不依赖于MTX的托法替布。
考虑到患者喜爱旅游及口服给药的便捷性,在Fleischmann教授与患者共同商议后, 2013年3月,患者开始托法替布5mg bid治疗。
2013年6月,患者CDAI 6,基线DAS28-ESR评分 2.7,HAQ 0,患者未出现不良反应。
2013年9月,患者CDAI 2,基线DAS28-ESR评分 2.2,HAQ 0。托法替布维持治疗,激素药物用量逐渐减少。
2013年12月,患者CDAI 1,基线DAS28-ESR评分 2.1,HAQ 0。至今患者病情维持良好。
02
病例讨论
在此病例中,患者初期治疗时出现明显MTX不良反应,停用MTX后,病情再次出现活动。后期患者接受托法替布治疗后,CDAI、基线DAS28-ESR评分等显著下降,后续随访中患者仍保持稳定的疾病缓解,并且在治疗过程中托法替布对激素的减停亦有所帮助。
托法替布是全球首个新型口服小分子靶向JAK抑制剂,被最新ACR指南、欧洲抗风湿联盟(EULAR)指南和《2018中国类风湿关节炎诊疗指南》推荐用于csDMARDs疗效不足或不耐受的RA患者[1]。托法替布通过抑制细胞内JAK信号通路,直接或间接抑制了包括 IL-2,IL-7,IL-6、IL-9,IL-15,IL-21、TNF-α、IL-17 等多个细胞因子的产生及促炎作用的发挥。相比较只在细胞外抑制单个细胞因子的生物制剂而言,托法替布具有非常独特的作用机制,同时具有强效的抗炎作用,且作用不依赖于MTX。托法替布为一线治疗效果不佳的RA患者提供了治疗新选择。
03
托法替布有效性——ORAL系列Ⅲ期临床研究,循证医学充足
会上Fleischmann教授总结了近年来有关托法替布的6项关键性Ⅲ期临床研究(ORAL Start、Solo、Sync、Standard、Scan、Step),这一系列研究非常有针对性地证实了托法替布针对不同治疗类型患者的疗效[2-7]。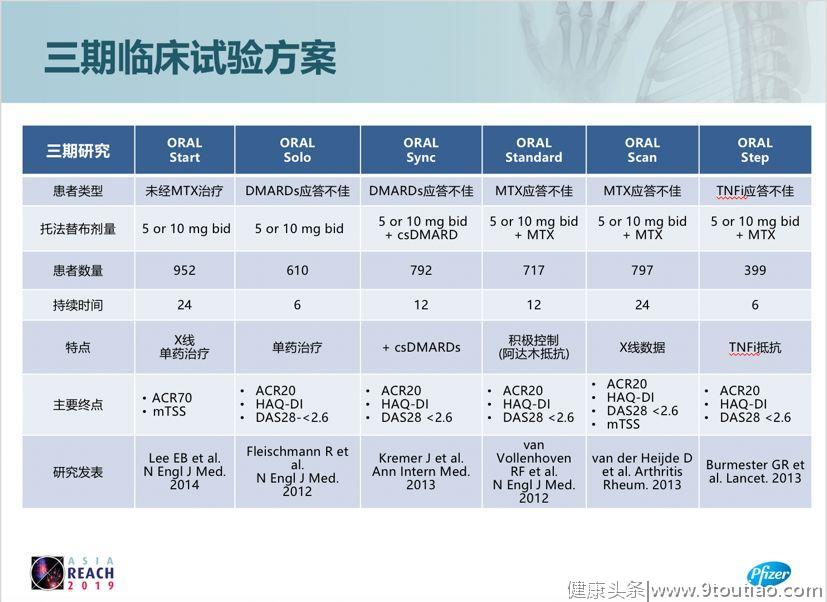
Ⅲ期临床试验方案。ACR20/50/70:美国风湿病学会定义的20%/50%/70%关节炎改善
Ⅲ期临床试验结果显示,托法替布可明显改善患者症状体征、影像学及患者报告结局。
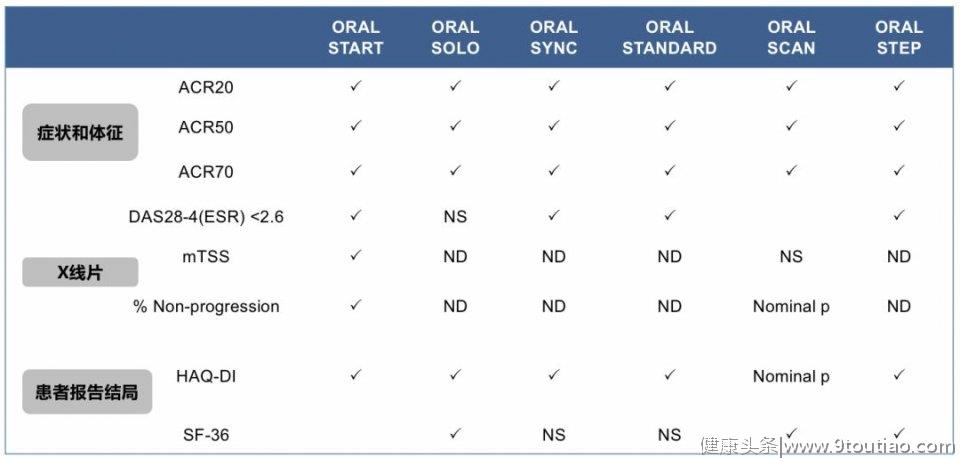
Ⅲ期临床试验结果。达到主要或次要终点(P<0.05);mTSS:影像学评分;SF-36:健康状况评估表;ND,不涉及X线片;NS,主要终点不显著;
04
托法替布安全性——9.5年长期安全性数据分析
Fleischmann教授在发言中强调,如果药品不能保证其安全性,那么讲再多的疗效都是徒劳,药品的安全是RA治疗最基本的保证。
药物安全性是症状和体征、机体功能、健康相关生活质量、影像学进程等疗效的基石
托法替布作为JAK抑制剂领导者,具有良好的安全性记录和长期大规模的RA临床研究数据积累。在全球多中心RA临床研究中共有超过7000例患者使用了托法替布,总药物暴露超过22000患者年,其中约30%的患者暴露时间>5年,最长暴露时间>9.5年[8]。经长期临床验证,应用托法替布的患者出现严重感染、结核、恶性肿瘤、心血管事件、消化道穿孔和死亡等不良反应的情况与生物制剂相当。在Cox回归分析中,严重感染及带状疱疹的发生与激素使用及高剂量有相关性。长期使用托法替布不会增加不良反应的发生概率,恶性肿瘤、严重感染、带状疱疹等发生率保持稳定。
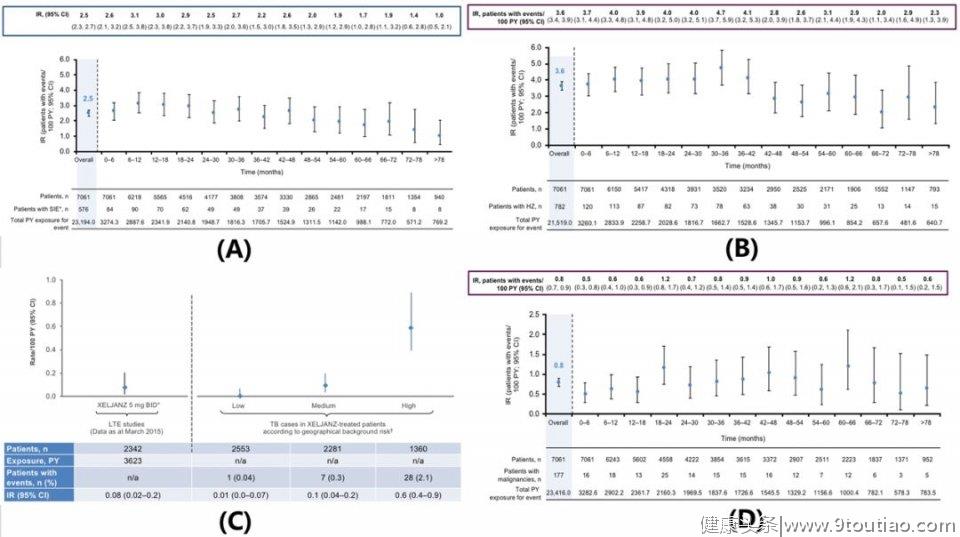

托法替布不良事件发生情况:(A)严重感染发生率(B)带状疱疹发生率(C)肺结核发生率(D)恶性肿瘤发生率(E)主要不良心血管事件发生率(F)深静脉血栓发生率(G)肺栓塞发生率均随时间增长保持稳定
05
托法替布在真实世界的应用
据Fleischmann教授介绍,CORRONA研究是一项北美洲的RA注册研究,自2002年至今,已有超过48000例注册RA患者,其中有2163名患者纳入托法替布亚组分析[9]。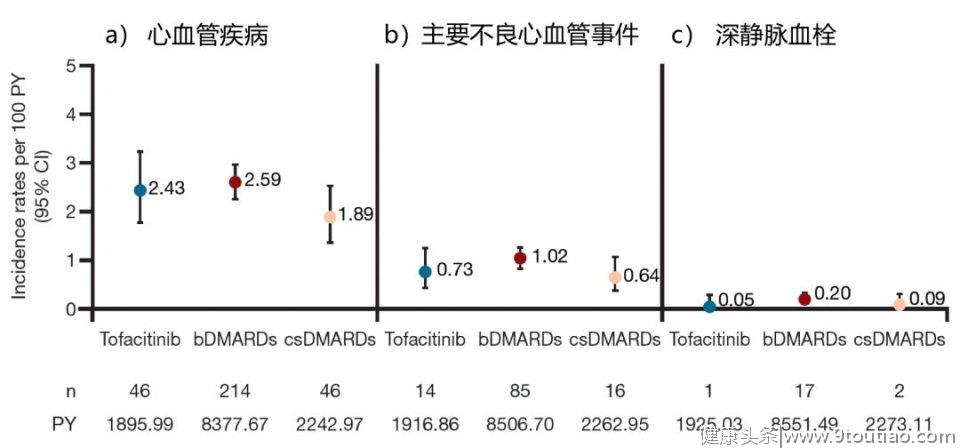
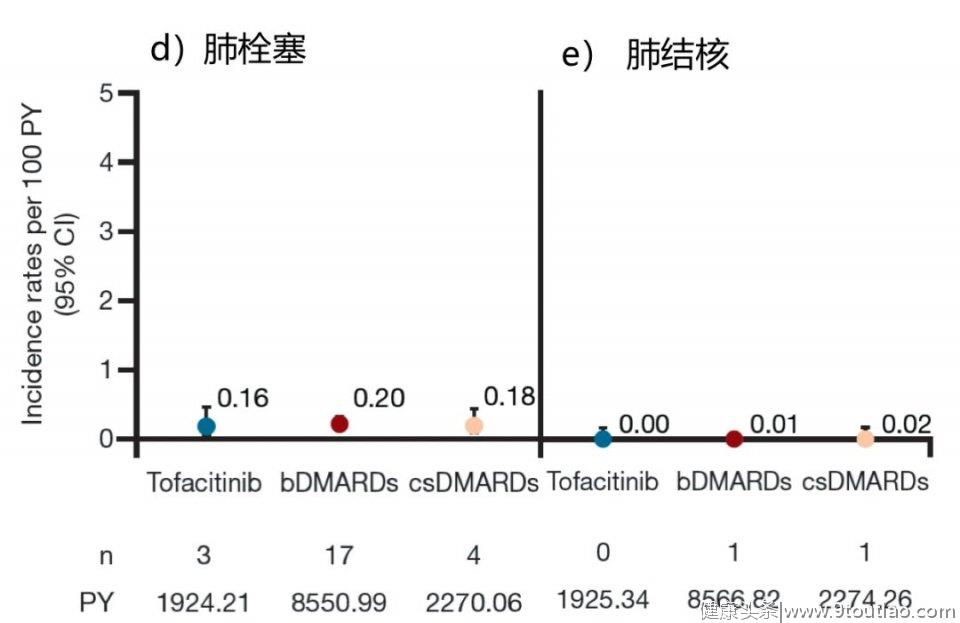
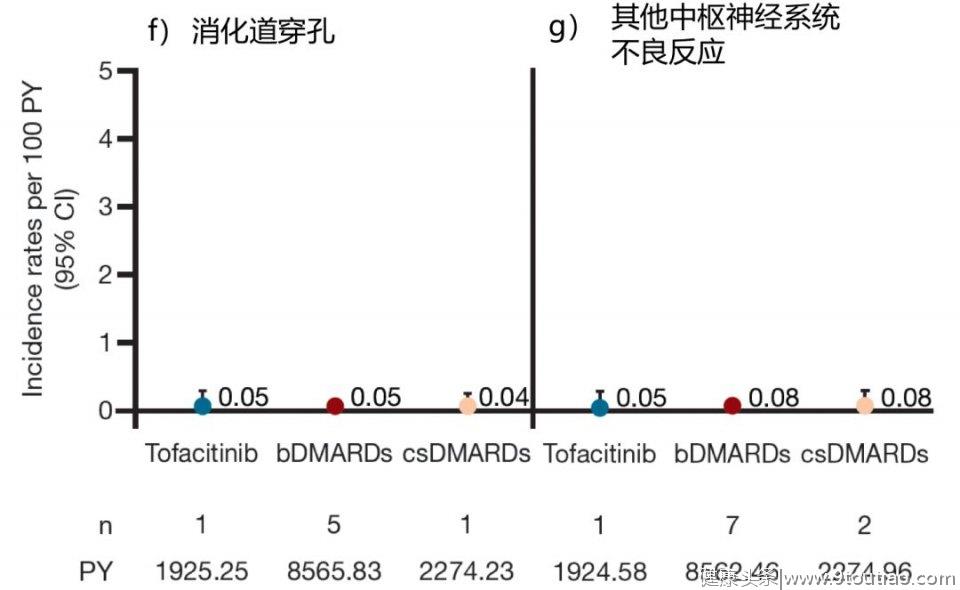
CORRONA注册研究在治疗过程中不良事件的发生率
来自CORRONA的真实世界数据分析提示:
①在这项分析中,尽管使用托法替布的这部分患者存在更长的病程和前期的生物制剂的治疗,但RA患者在以托法替布、生物制剂和csDMARDs这三种药物为初始治疗时,患者都会发生相似比例的不良事件;
②目前,在真实世界中还没有发现托法替布新的安全风险,托法替布的风险收益比状况与临床中已知的情况保持一致。
06
托法替布的使用建议
最后,Fleischmann教授分享了一些在使用托法替布方面的个人经验,包括托法替布单药治疗和与传统合成DMARDs联用。
Fleischmann教授提到,在使用生物制剂前,他通常会使用托法替布联合MTX对患者进行治疗。当患者病情达到缓解或低疾病活动度时,通常会选择保留托法替布而停用MTX,也取得了不错的疗效。另外,他也曾有过在一种生物制剂治疗失败后使用托法替布成功的经验。
此外,Fleischmann教授建议临床医生在用药前充分准备,用药后做好随访,以及注意特殊情况下的用药调整,确保用药安全。
1.用药前准备确认血常规:淋巴细胞计数>0.5x109/L,中性粒细胞计数>1x109/L,血红蛋白>90g/L;
确认基线脂质水平:如存在血脂升高,需按指南进行治疗;
筛查乙型肝炎、丙型肝炎及HIV病毒感染:如存在阳性应做好预先处理;
筛查潜伏性结核:如存在潜伏性结核病,需经预防性治疗后再开始托法替布治疗;
用药前接种带状疱疹疫苗:可以预防带状疱疹的发生。
表1:托法替布使用前和使用时监测建议

a.建议在4-8周首次检测后,在必要时仍需对血脂水平进行监测;b.在托法替布使用前,另需根据临床指南对肝炎进行筛查。
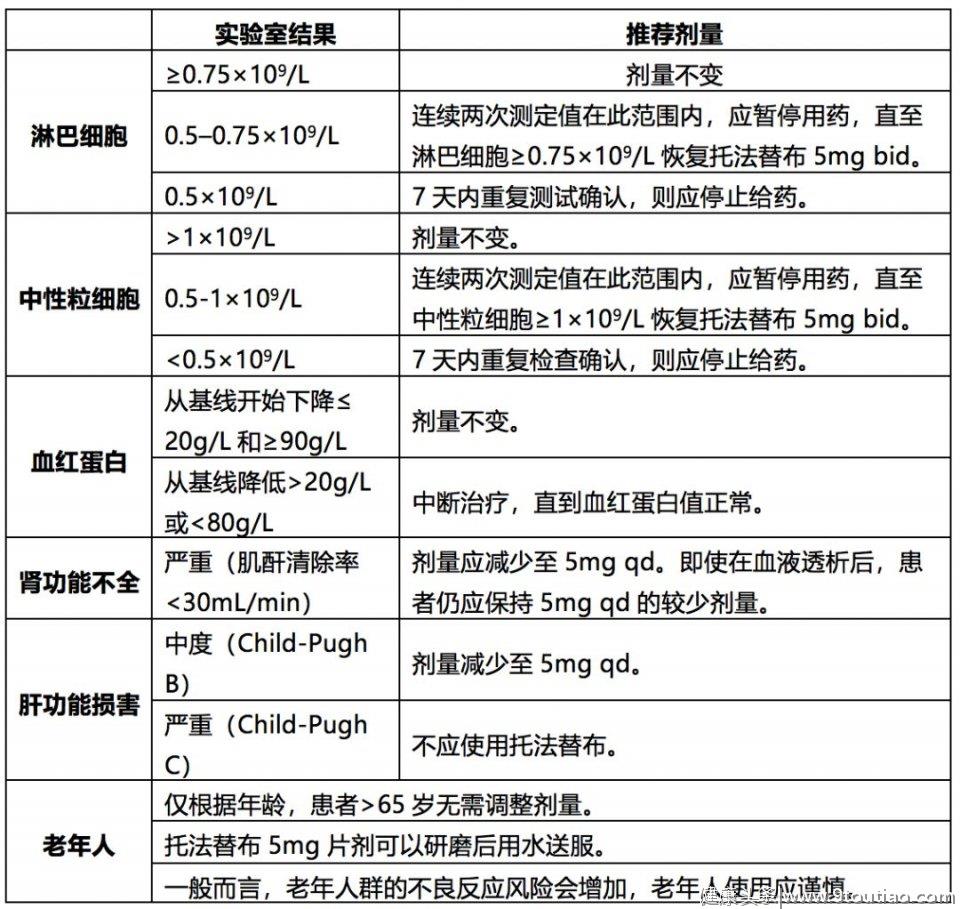
3.托法替布其他使用建议表2:特殊情况下托法替布的使用建议
参考文献:
[1]中华医学会风湿病学分会.2018中国类风湿关节炎诊疗指南.中华内科杂志.2018,57(4):242-251.
[2] Lee EB, et al. N Engl J Med 2014;370:2377-2386.
[3] Fleischmann R, et al. N Engl J Med 2012;367:495-507.
[4] Kremer J, et al. Ann Intern Med. 2013;159:253-261.
[5] van Vollenhoven RF, et al. N Engl J Med 2012;367:508-519.
[6] van der Heijde D et al. Arthritis Rheum 2013;65:559-570.
[7] Burmester GR, et al. Lancet. 2013;381:451-460.
[8] Cohen S, et al. American College of Rheumatology Congress 2018 Abstract 963.
[9] Kavanaugh AF, et al. Arthritis Rheumatol. 2016;68(suppl 10):Abstract 2595.