喜讯!传奇抗癌药LOXO-101(Vitrakvi)在中国申报临床获受理!
昨天,FDA批准的第一个不区分肿瘤来源用于初始治疗的传奇抗癌药LOXO-101(Vitrakvi)在中国申报临床试验(IND),并获得正式受理。根据国家药监局药品审评中心(CDE)网站公开信息,该药品以“硫酸Larotrectinib胶囊”为名称的IND申请由拜耳公司申报,且已经于2019年1月14日获受理,受理信息如下:
Larotrectinib在中国申报临床并获得受理,是该药在全球进行注册的又一大进展!
Larotrectinib是Loxo Oncology公司和拜耳公司开发的新一代具备高度特异性的口服TRK抑制剂。该药的最大看点在于,它是一款针对特定基因突变,而不针对特定癌症种类的抗癌新药。
其所能治疗的NTRK基因融合实体瘤包括乳腺癌、结直肠癌、肺癌、甲状腺癌等癌症类型。
因此,Larotrectinib在美国获批被认为是癌症疗法从“基于癌症在体内的起源”转向“基于肿瘤的遗传特征”这一演变过程中的重要里程碑。
关于LOXO-101
药物名称:Vitrakvi(Larotrectinib,拉罗替尼,又名LOXO-101)
美国上市时间:2018年11月26日
药物功效:有效对抗由单一罕见基因(NTRK)突变驱动的各种癌症
针对人群:患有实体肿瘤的成人和儿童患者
制造企业:Bayer(拜耳)和Loxo Oncology共同研发
使用剂量:
成年人:Larotrectinib对成年人的剂量是每天口服100mg,每天两次,直至疾病进展或出现不可接受毒性!;
儿童按年龄和体重使用剂量:体表面积小于1.0米的儿科患者,Vitrakvi的推荐剂量是100mg/m2 ,每日口服两次,与或不与食物同服。
不良反应剂量调整:出现3级或4级不良反应,减少用量直至改善或不良反应1级。如果不良反应在4周内改善,则在下一次计量时恢复。如果4周内不良反应无法消退,则永久停用Vitrakvi。
全球肿瘤医生网仅为患者提供全球抗癌新药上市及用药最新信息,如需了解详情可致电医学部400-666-7998。
LOXO-101最新药品信息
全球肿瘤医生网为大家提供该药品的最新资讯。
到货时间:全球最早到货时间为2019年1月12日左右,以实际到货时间为准!
货品规格:目前可以提供25mg*60粒/每瓶
建议用量:官方建议用法每日口服两次,每次100毫克;建议由低剂量开始服用每日口服两次,每次50毫克。
美国定价:口服胶囊形式的Larotrectinib采购价格为每月32,800美元(30天100mg),每年393600美元(约270多万人民币),此价格对于患者来说,堪称天价。某些儿童患者的口服液体制剂为每月1.1万美元。
价格估计:Vitrakvi (larotrectinib)建议售价为20万-21.5万/月。

国内第一位获得LOXO-101的患者,基因检测显示NTRK1基因融合,美国医生根据病情开处方接受治疗,因此这款药并不是适合所有的癌症患者,先去看看自己的基因检测报告吧,看不懂的患者可以致电医学部(400-666-7998)请专业人士解读报告。

由于这款“抗癌神药”还未在国内上市,对于走投无路的癌症患者来说,除了前往美国购药外,临床试验也是一种很好的选择,Rossy找到了几项患者可申请的临床试验,但是入组的首要条件是先进行基因检测,确认存在NTRK基因突变!所以先去看看你的基因检测报告吧,
1、NTRK融合阳性实体瘤患者LOXO-101(Larotrectinib)的研究
这是一项针对携带NTRK1,NTRK2或NTRK3融合基因的晚期实体瘤患者的II期多中心开放标记研究。LOXO-101将以100mg每日两次(BID)口服给药,连续给药28天为1周期。
该研究将分析8个患有NTRK融合肿瘤患者的队列,包括非小细胞肺癌,甲状腺癌,肉瘤,结肠直肠癌,唾液腺癌,胆管癌和原发性CNS肿瘤。
实验地点:
1、加州大学洛杉矶分校
2、麻省总医院
3、斯坦福大学等
2、口服TRK抑制剂LOXO-101(Larotrectinib)用于治疗晚期小儿实体或原发性中枢神经系统肿瘤
这是一项多中心,开放标签,1/2期研究,用于晚期实体或原发性CNS肿瘤的儿科患者。LOXO-101(larotrectinib)将每日两次口服(PO)(BID),剂量通过体表面积(BSA)调整。
实验地点:1、波士顿儿童医院
2、纪念斯隆凯特林中心
3、辛辛那提儿童医院医疗中心等
如何找到可以获益的患者?
由于NTRK基因融合十分罕见,如何找到临床中真正可以获益的人群是一项挑战,通过使用特定测试鉴定NTRK基因融合体来诊断,包括采用新一代测序(NGS)和荧光 原位 杂交(FISH)的测试。
在一些罕见的癌症中,NTRK融合经常发生。这些包括婴儿纤维肉瘤,分泌型乳房癌等。这些罕见癌症通常会发现NTRK融合,这些患者可能会受益于larotrectinib等药物。
做过癌症基因组检测的晚期癌症患者可能会发现他们的肿瘤存在TRK融合,因为这种基因组事件已在许多肿瘤类型中被描述,包括:
- 急性髓性白血病
- 星形细胞瘤
- 脑低级别胶质瘤
- 乳腺癌
- 结直肠癌
- 先天性中胚层肾瘤
- 胃肠道间质瘤
- 多形性胶质母细胞瘤
- 头颈部鳞状细胞癌
- 肝内胆管细胞癌
- 肺癌
- 唾液腺来源的乳腺类似物分泌癌
- 黑色素瘤
- 肉瘤
- 分泌性乳腺癌
- 甲状腺癌
一般检查融合基因需要使用二代基因检测技术。而且一定注意是NTRK基因与其他基因融合发生的突变,而不是一个随便的点突变。
全球顶尖的基因检测公司凯瑞思和Foundation Medicine最近也研发了Foundation One CDx用于NTRK融合检测,想了解的患者可以致电全球肿瘤医生网医学部咨询(400-666-7998)。

“我们欢迎 FDA 对Vitrakvi的批准和基因组测试的创新,使精确医学照进现实,我们正在看到科学进步,例如能够检测NTRK基因融合的基因组测试,开始转变癌症治疗方法并为患者提供新的希望和选择。”
随着国家和相关部门的重视,希望这款新药能够尽快在中国开展临床试验,也希望临床研究顺利开展,相信这些效果好的抗癌药都会加快在我国上市和纳入医保的步伐,让更多的百姓获益,让我们共同期待吧!
最后,我们来回顾一下这款“神药”从研发到上市的光辉历程:
2016年12月18日Loxo Oncology TRK抑制剂Larotrectinib(LOXO-101)在ESMO亚洲第1阶段更新中显示穿越TRK融合癌的持久抗肿瘤活性;
2017年2月21日Loxo Oncology宣布完成Larotrectinib NDA主要疗效分析的临床试验注册;
2017年5月12日FDA宣布授予Larotrectinib孤儿药物称号,指定用于治疗NTRK融合蛋白的实体肿瘤;
2017年6月3日Loxo Oncology突破疗法Larotrectinib在美国临床肿瘤学会提交的TRK融合成人和儿童癌症中显示76%客观反应率!
2017年12月12日Loxo Oncology更新Larotrectinib儿童临床试验数据显示TRK融合的持续耐受性;
2017年12月20日Loxo Oncology开始向美国食品和药物管理局提交Larotrectinib新药申请用于治疗TRK融合肿瘤;
2018年2月21日Loxo Oncology宣布在新英格兰医学杂志上发表Larotrectinib临床数据:权威发布!针对17种肿瘤的传奇抗癌药LOXO-101最新研究数据公布!有效率75%!
其中有一些晚期患者的病灶完全消失了:
我们可以清楚的看到,这位极晚期的肉瘤患者,肿瘤已经快要填满双肺,经过LOXO-101治疗12周期,肿瘤几乎完全消失!
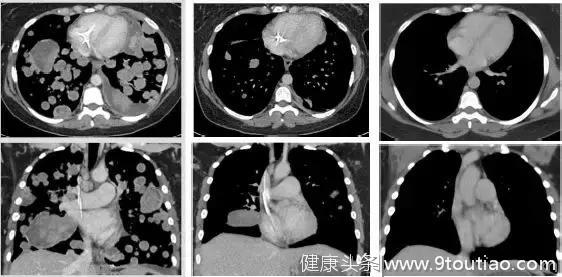
治疗前 治疗3周期第1天 治疗13周期第1天
2018年3月26日Loxo Oncology完成Larotrectinib治疗TRK融合癌新药申请滚动提交;
2018年3月28日在线的权威肿瘤学杂志柳叶刀上公布了传奇抗癌药larotrectinib(LOXO-101)的最新研究数据!该药在部分儿童癌症患者达到了93%的治疗应答!重磅新数据!针对17种肿瘤的传奇抗癌药LOXO-101公布新数据,这次有效率高达93%!
2016年,13岁的的Briana Ayala,被发现在她的腹部有一个罕见的肿瘤,包裹在她的主动脉周围。Briana参加了larotrectinib的1期临床试验,几周之内,她的腹部疼痛和肿胀消失,扫描显示她的肿瘤显着缩小。将近两年后,Briana重返学校!
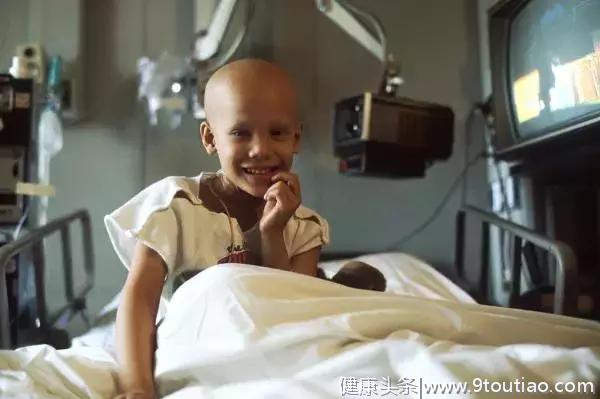
德克萨斯大学西南分校的研究人员表示,larotrectinib在1期临床试验中93%的儿科患者有效。(照片由比尔布兰森/国家癌症研究所提供)
2018年5月29日FDA接受Larotrectinib新药申请并授予优先审查;
2018年10月21日Larotrectinib在109个TRK融合癌症患者的扩展数据显示81%的总体反应率;权威公布!“治愈系”抗癌明星药LOXO-101新数据:有效率81%!下个月上市(附PDF)
参考资料:
https://www.forbes.com/sites/matthewherper/2018/11/26/loxo-and-bayers-amazing-drug-has-an-expensive-price/#77ed746524d0
https://ir.loxooncology.com/press-releases/2378241-Fda-approves-vitrakvi-larotrectinib-the-first-ever-trk-inhibitor-for-patients-with-advanced-solid-tumors-harboring-an-ntrk-gene-fusion12
https://beta.nbcnews.com/health/health-news/fda-approves-new-cancer-drug-targeted-genetic-mutation-not-cancer-n940656
"