运动裨益心血管健康:从分子到临床

通过内分泌或旁分泌方式介导组织器官间交互作用, 参与代谢及心血管保护. 在临床实践中, 适当的运动干预目前已成为多种心血管疾病治疗和康复的必要辅助手段. 但心血管疾病防治的运动处方, 尤其是个体化的具体运动方式选择及运动量的掌控等问题尚待解决. 通过多组学等方法进一步阐明运动裨益心血管健康的分子机制不仅有助于人们深入认识运动的健康效应, 还可为通过调动机体内源性保护机制防治心血管疾病和制定更精准的心血管康复运动处方提供科学依据和新思路.
运动裨益心血管健康已被广泛认可, 但其机制尚未被阐明. 运动促进心血管健康是一种全身系统性效应, 涉及神经-内分泌-代谢-免疫等多个系统, 其核心是运动通过缺氧、氧化应激和机械力刺激(如血流加速)等激活机体内源性保护机制, 包括激活细胞生存信号、改善机体代谢、提高抗氧化能力、促进干细胞动员等, 其中线粒体作为机体响应运动的核心细胞器, 通过PGC-1α(peroxisome proliferator-activated receptor-γcoactivator-1α)等信号分子促进线粒体合成和改善线粒体功能在运动健康效应中发挥重要作用(图1). 此外, 运动能够降低心血管疾病的危险因素, 重塑心血管结构与功能, 提高心血管胰岛素敏感性及抗损性等.近年研究表明, 运动可促进多种组织和器官分泌“运动因子(exerkine)”参与代谢及心血管保护, 显示出组织器官间交互作用(cross-talk)在运动心血管健康效应中的重要性. 本文综述了运动裨益心血管健康的主要机制及其研究进展, 简要介绍了当前运动防治心血管疾病的临床应用, 重点讨论了该领域目前存在的主要问题并提出了展望, 以期促进对运动心血管健康效应的认识及其在心血管病防治中的转化应用.
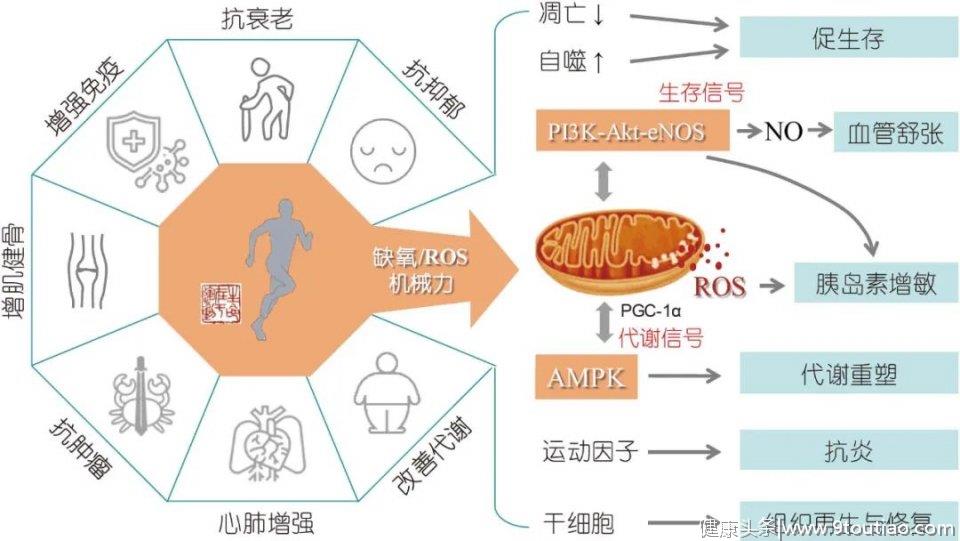
1 运动降低心血管疾病的危险因素及其主要机制
运动具有广泛的健康效应, 除改善心血管功能外,还能够显著降低心血管疾病的危险因素, 包括改善机体代谢、降压减脂、改善机体慢性炎症状态以及提高心血管抗损性等. 这些效应相互影响共同促进心血管健康.
1.1 运动改善机体代谢
以肥胖、高脂血症、糖耐量异常及胰岛素抵抗为主要表现的代谢综合征(metabolic syndrome)是高血压、动脉粥样硬化、冠心病等心血管疾病的主要危险因素. 运动可通过多种机制改善糖脂代谢及胰岛素敏感性. 运动通过直接促进分解代谢和提高胰岛素敏感性促进三大营养物质代谢, 包括促进机体对葡萄糖的利用, 维持葡萄糖稳态, 降低糖尿病患者血糖和糖化血红蛋白水平; 显著降低甘油三酯, 增加循环高密度脂蛋白水平, 并促进脂肪组织棕色化和产热; 改善机体脂肪酸代谢, 增肌减脂. 新近研究表明, 氨基酸代谢紊乱也是代谢性心血管病的重要发病机制之一,而运动不仅可增加组织细胞对氨基酸的利用, 还可改善糖尿病等病理状态下支链氨基酸(branched chain amino acid, BCAA)代谢紊乱, 促进心脏代谢健康(cardiometabolic health).
1.2 运动改善氧化还原平衡和慢性炎症状态
氧化应激是诸多心血管疾病的共同病理基础, 长期运动能够通过增强抗氧化能力改善机体氧化还原状态, 该效应是运动裨益心血管健康的重要机制之一. 运动时骨骼肌收缩使活性氧(reactive oxygen species,ROS)产生增加, 其主要来源于线粒体电子传递过程.以往认为ROS可造成细胞氧化应激, 是导致生物大分子损伤的一类有害活性物质, 近年越来越多的证据表明, 适量ROS的产生具有重要的生理意义. 运动时产生的ROS能够促进线粒体合成, 激活胰岛素信号, 促进蛋白质合成和肌肉生长, 还可调控基因表达及增强机体抗氧化能力, 而抑制运动过程中ROS的产生则使运动的健康效应减弱. 特别是长期运动能够增强线粒体功能和机体的抗氧化能力, 更好地维持机体氧化还原平衡.
许多慢性疾病, 尤其是代谢性心血管疾病都使机体处于一种低程度的慢性炎症状态, 后者既是慢性非传染性疾病(慢病, non-communicable disease, NCD)的结果也是导致慢病和加速衰老的重要原因, 使机体长期处于不良的恶性循环状态. 研究显示, 长期有氧运动能够改善机体慢性炎症, 是打破这种恶性循环的一种有效干预措施. 例如, 研究报道, 有氧运动能够使冠心病患者的高敏-C反应蛋白(high sensitivity C-reactive protein, hs-CRP, 一种炎性标志物)降低40%; 运动可促进人骨骼肌分泌白介素-6(interleukin-6, IL-6), 抑制肿瘤坏死因子α(tumornecrosis factor-α, TNF-α)、IL-1β等促炎因子的产生, 从而发挥抗炎作用. 此外, 运动可增加脂肪分解代谢, 减少内脏脂肪, 激活下丘脑-垂体-肾上腺轴和交感神经系统释放皮质醇等抑制炎性细胞因子产生. 其中, 运动抑制Janus kinase/signal transducer and activator of transcription(JAK-STAT)信号通路在运动抗炎效应中扮演重要角色. 长期运动对机体的氧化还原平衡和炎症状态的影响是系统性的,可直接或间接地促进心血管健康.
1.3 运动延缓衰老
衰老伴随机体一系列结构和功能的变化, 是心血管疾病等慢病的危险因素之一. 研究表明, 运动可促进干细胞动员使机体处于“年轻态”, 长期规律有氧运动具有延缓衰老效应. 比如, 运动可减少由于衰老引起的神经胶质细胞激活, 增加神经胶质细胞的体积,通过增加胰岛素样生长因子1(insulin-like growth factor1, IGF1)、血管内皮生长因子(vascular endothelial growth factor, VEGF)等促进神经发生和血管形成, 增强中枢神经系统胰岛素敏感性. 这些作用能够促进脑血流循环, 减少脑淀粉样蛋白-β堆积, 延缓增龄相关的神经退行性改变; 运动还可以改善由于衰老引起的下丘脑-垂体轴的内分泌功能, 改善老龄肌肉和骨骼状态等.
运动对心脏衰老的影响包括: (ⅰ) 衰老心脏β肾上腺素受体脱敏使心脏对肾上腺素刺激的敏感性降低, 运动能够增强心肌对肾上腺素的敏感性, 从而增加心脏功能储备. (ⅱ) 衰老心脏对Ca2+的处理能力减弱, 同样的刺激使细胞内Ca2+上升减少和细胞收缩力减弱, 运动能够增强细胞内Ca2+的处理能力和细胞收缩能力. (ⅲ) 心肌肥大是心肌衰老的一个典型表现,其原因与心肌细胞减少和心肌再生能力减弱有关. 虽然运动也能够导致心肌肥厚, 但其与衰老时的心脏肥大不同, 不伴有心肌纤维化和心肌功能紊乱, 运动仅适度上调Akt, 通过下游mTOR(mammalian target of rapamycin)改善心肌代谢的同时保护心脏功能, 并延缓衰老所致的心脏肥大.(ⅳ) 线粒体功能紊乱是衰老心肌功能改变的一个重要机制, 运动能够改善线粒体动力学(mitochondrial dynamics)和功能, 改善心肌代谢, 减少氧化应激和提高心脏储备能力. 此外, 血管衰老通常表现为大血管管壁增厚和僵硬度增加, 内皮功能紊乱, 血管内皮向促血栓、促炎和血管收缩表型转化, 平滑肌向分泌型转化和血管新生能力减弱等,长期有氧运动可改善甚至部分逆转上述改变, 延缓血管衰老. 目前认为, 运动延缓衰老的核心是其提高抗氧化能力, 改善机体的氧化还原状态, 而氧化应激是引起衰老的一个重要原因.
1.4 运动防治高血压
大量的基础和临床研究均表明, 运动可预防和治疗高血压. 2019年Naci等人发表在 British Journal of Sports Medicine 的Meta分析纳入了391个随机对照试验和39742名受试者, 结果显示, 所有类型的运动干预(如耐力训练、动态抗阻训练、等长肌力训练)都可有效降低收缩压. 高血压患者规律进行有氧运动可以使安静血压降低5~7 mmHg. 近年的研究表明, 高强度间歇训练和持续有氧训练在降低血压方面具有相似的效果, 但高强度间歇训练在提高心肺耐力、改善血管内皮功能和胰岛素敏感性等方面更有潜力. 目前认为, 运动防治高血压的机制主要包括: 降低交感神经兴奋性进而改善小动脉收缩状态, 改善氧化应激水平,调节肾素-血管紧张素系统进而影响血管重塑和血管张力, 增加机体胰岛素敏感性, 提高血管内皮细胞一氧化氮(nitric oxide, NO)生物利用度, 促进小血管舒张和组织灌注等.
1.5 运动的增肌效应与心血管健康
骨骼肌是人体最大的器官, 约占身体质量的40%.骨骼肌除维持机体运动功能之外, 还是葡萄糖代谢进而参与维持血糖稳态的主要器官之一. 骨骼肌质量减少可导致葡萄糖代谢及糖耐量降低; 而运动的增肌效应不仅有助于改善机体胰岛素敏感性, 还可通过增加血糖“去路”(进入骨骼肌)缓冲血糖升高, 改善葡萄糖代谢和糖耐量. 此外, 肌肉还是机体重要的内分泌器官, 可通过分泌多种运动因子调控心血管代谢和功能. 新近研究表明, 人体肌肉组织量与心血管疾病的发生率和死亡率密切相关. 肌肉萎缩(如肌少症)时肌肉来源的肉毒碱减少, 后者是心肌和骨骼肌脂肪酸转运的重要物质基础, 可导致机体脂肪酸代谢异常. 肌少症常见于射血分数保留性心衰患者, 可通过机体糖脂代谢异常、分泌运动因子减少等机制引起心血管功能紊乱. 此外, 衰老、长期航天(失重)等导致的骨骼肌萎缩也与心血管代谢和功能异常相关.
1.6 其他
近年来肠道菌群的生物学作用被广泛研究, 肠道菌群可通过其代谢物等多种途径影响心血管健康, 例如, 与久坐等体力活动减少相关的肠道菌群变化与机体脂肪含量增加、循环甘油三酯增加、循环高密度脂蛋白降低和血压增加等改变有关. 有趣的是, 专业运动员的肠道菌群与久坐人群在宏基因组学和代谢组学方面均显示出一定的差异, 提示经常运动可通过影响改善肠道菌群促进代谢健康. 例如, 研究发现, 运动可通过改善肠道菌群增加机体短链脂肪酸并降低BCAA水平, 从而提高葡萄糖代谢和胰岛素敏感性.已知精神心理因素参与缺血性心脏病的发生发展, 运动可以缓解心理应激, 使冠心病患者中度和重度焦虑发生率分别降低56%和69%, 促进心脏康复. 此外,运动还可以促进干细胞动员, 促进组织损伤修复.这些效应相互作用, 共同促进心血管健康(图2).
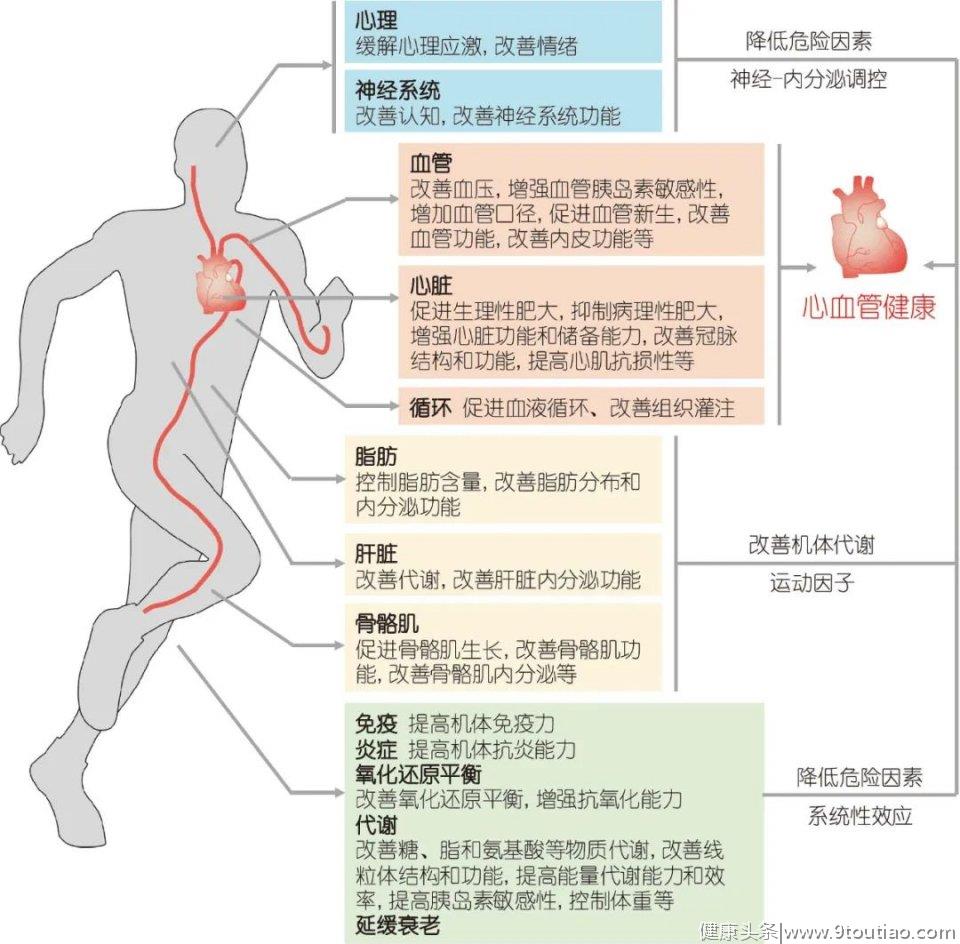
2 运动改善心血管结构与功能
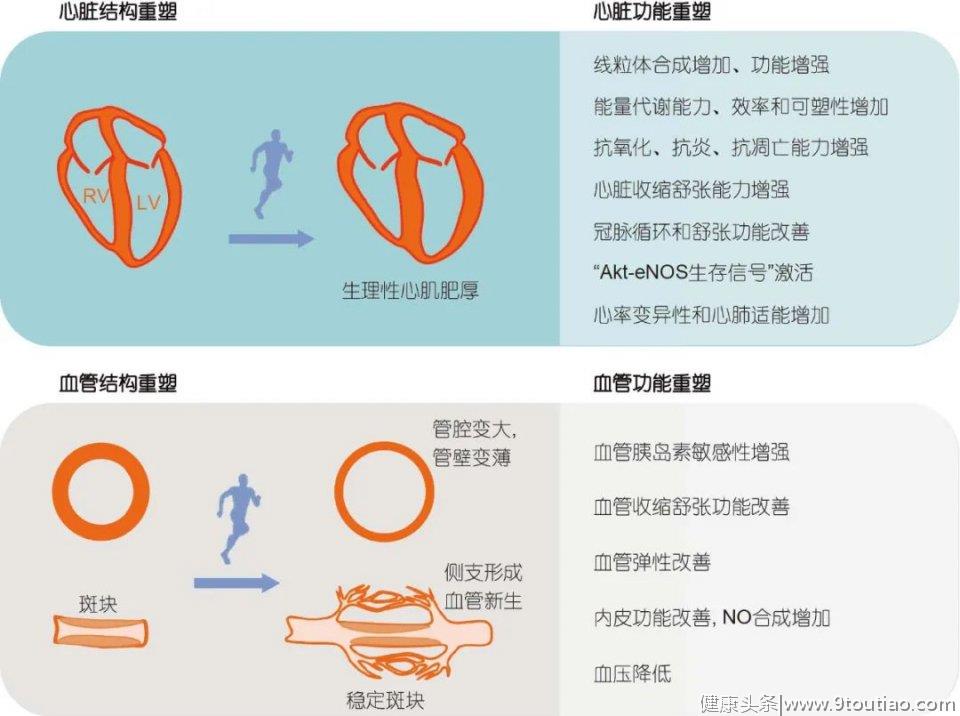
2.1 心血管结构与功能重塑长期高强度有氧运动可使心脏发生生理性肥厚,进而增强心脏功能(图3). 心肌生理性肥厚不同于病理性肥厚, 不伴有心肌纤维化等病理性改变, 其机制主要与心肌IGF1-PI3K-Akt信号通路的激活有关. 有趣的是, 虽然运动引起正常心脏的肥厚, 但适度运动对于病理性心肌肥厚(如心衰)却有抑制作用, 能够改善病理条件下的心肌结构和功能. 运动对血管的重塑包括:动脉血管(包括冠脉)口径变大和管壁变薄; 动脉粥样硬化斑块内胶原和弹性蛋白含量增加, 从而降低动脉粥样硬化引起的不良事件; 改善血管和心脏硬化,该效应可能是运动延缓衰老和保护重要器官功能的机制之一.
运动对血管的影响还包括促进血管形成. 一方面运动可以促进毛细血管和阻力血管新生(angiogenesis),另一方面可使动脉血管管腔增大, 称之为动脉生成(arteriogenesis)(图3), 该效应可发生在已有血管(包括冠脉), 是一种重要的血管适应性改变. VEGF是调控血管新生的一个关键分子, 研究发现, 运动可以增加骨骼肌和心肌VEGF的表达; 另一方面, 在动脉粥样硬化条件下, 运动可以增加循环内皮抑素(endostatin)的水平, 抑制斑块组织的血管新生, 从而抑制动脉粥样斑块的形成, 这对于冠心病的防治可能具有重要意义. 血管新生和动脉生成是保证特殊条件下组织血液灌注的基础, 这些过程的紊乱也是造成诸多疾病,特别是冠心病的病理机制之一. 运动可促进缺血心肌的血管新生和动脉生成, 增加冠脉侧支循环, 减轻心肌梗死后的心肌损伤, 在改善血液灌注和组织修复中发挥重要作用.
此外, 内皮功能紊乱是诸多心血管疾病发生发展的病理机制之一, 运动裨益心血管健康的一个重要效应就是其能够改善血管内皮功能, 该效应独立于血脂、血压、糖耐量和体重等因素.近年研究发现, 运动所致心血管健康效应部分依赖于运动对心血管产生的直接机械力刺激. 机械力是调控心血管功能的重要因素之一, 例如, 运动引起组织血流加速致剪切力增加, 可促进血管内皮细胞产生NO, 进而舒张小血管, 改善组织器官血流灌注. 本团队最近发现, 运动所致的血流剪切力增加还可直接促进血管内皮细胞分泌运动因子, 后者通过外泌体经血液循环到达心脏被心肌细胞摄取, 发挥心脏保护作用, 提示运动促进血管-心脏交互作用参与心血管调控和心脏保护. 新近一项人群对照研究显示, 拉伸运动比健步走能更有效降低血压, 其机制可能与拉伸运动对血管牵张的机械刺激改善血管僵硬度有关. 心血管感受机械力刺激并做出反应的机制尚不清楚, 近年研究发现, 血管内皮细胞、平滑肌细胞等多种组织细胞膜上具有机械力刺激的感受器(Piezo), 可以感受各种机械力的刺激并引起细胞钙内流引发细胞功能活动改变, 广泛参与运动相关的心血管功能调节, 并与动脉粥样硬化、心衰、高血压等心血管疾病的发生发展有关.
2.2 改善心肌线粒体功能与代谢
大量研究表明, 运动裨益心血管健康与其改善线粒体功能密不可分. 线粒体是机体内调控代谢、氧化还原平衡和细胞命运等生命过程的核心. 心肌是线粒体含量最丰富的组织, 心肌细胞线粒体约占心肌细胞体积的40%, 以保证心脏终生搏动的能量供给. 运动时心肌对能量的需求显著增加, 心肌所产生的ATP随之增加, 经常运动的心脏能够在短时间内使ATP的产生速率增加5~10倍, 同时伴随心肌线粒体来源的ROS产生增加. 此外, 心脏可以利用几乎所有的代谢底物. 通常状况下, 心脏主要是以脂肪酸作为代谢底物(40%~70%), 运动时心肌对脂肪酸和乳酸的利用增加, 对葡萄糖的利用降低. 长期运动使心肌对葡萄糖的利用增加, 特别是糖酵解水平增加, 该作用参与心脏生理性肥厚的发生发展. 长期运动可改善线粒体动力学和功能, 不仅能够提高心肌代谢的速率和效率, 而且增强心肌对代谢底物利用转换(metabolic switch)的灵活性, 提高心肌的抗损性.
运动激活心肌Akt, AMPK(5′ AMP-activated protein kinase), mTOR等信号通路, 促进心肌细胞对代谢底物的转运和利用. 运动激活细胞内PGC-1α, PPAR(peroxisome proliferator-activated receptor), NRF2(nuclear factorerythroid 2-related factor 2)等转录因子, 广泛参与细胞功能及线粒体稳态的调控. 运动激活PGC-1α促进线粒体生物合成, 同时也可促进线粒体自噬(mitophagy), 使得衰老或质量不佳的线粒体降解, 从而提高线粒体的整体质量和功能. 此外, 线粒体是一种高度动态的细胞器, 不断进行融合和分裂, 线粒体动力学是维持线粒体质量和调控线粒体功能的重要方式.研究表明, 运动可以改善线粒体动力学, 特别是在一些心脏疾病(缺血性心脏病、心衰)等条件下能够抑制线粒体过度分裂. 急性运动可致心肌线粒体来源的ROS增加, 对心脏产生类似“缺血预适应(preconditioning)”效应, 长期运动能够提高线粒体的抗氧化能力并改善心肌氧化还原状态. 无论是有氧运动还是阻抗运动都会显著影响线粒体稳态和功能, 并在运动裨益心血管健康效应中发挥重要作用.
2.3 其他
运动裨益心血管健康是一种全身系统性效应. 除以上机制外, 运动还通过其他作用影响心血管功能. 比如, 交感神经长期过度兴奋对心血管的结构和功能会带来负面影响, 是多种心血管疾病的发病机制之一.长期有氧运动能够改善心血管自主神经系统功能和平衡状态, 增强副交感神经活动和降低交感神经活动, 增加心率变异性(heart rate variability, HRV), 发挥心血管保护效应. 此外, 老龄或长期缺乏运动所致的心肺适能(cardiorespiratory fitness, CRF)降低也和心血管疾病的发生发展有关. 荟萃分析显示, 心肺适能每增加1个代谢当量(metabolicequivalent, MET), 全因死亡率和心血管疾病死亡率分别下降13%和15%. 无论有氧运动还是抗阻运动均可提高心肺适能, 促进心血管健康.
3 运动提高心血管胰岛素敏感性及抗损性
3.1 提高心血管胰岛素敏感性
胰岛素抵抗是高血压、冠心病、糖尿病等多种心血管疾病的共同病理生理基础. 研究表明, 缺乏体力活动与机体葡萄糖耐量受损存在密切关系, 而后者是糖尿病及多种心血管代谢疾病的重要病理标志. 运动对正常及胰岛素抵抗者的胰岛素敏感性均具有提高和改善作用. 研究表明, 单次运动和长期运动均可显著改善机体胰岛素敏感性, 急性运动可使骨骼肌葡萄糖转运体4(glucose transporter 4, GLUT4)转位和葡萄糖转运增加, 该作用可持续16~48小时; 而长期规律的运动可持久改善正常人及糖尿病患者骨骼肌葡萄糖摄取及代谢. 运动可以逆转胰岛素信号通路各环节的分子异常, 例如, 运动增加胰岛素受体、胰岛素受体底物(insulin receptor substrate, IRS), PI3K, Akt等分子的表达及活性和GLUT4的表达及上膜转运; 还可激活细胞内AMPK,Akt, PGC-1α和MAPK(mitogen-activated protein kinase)等代谢相关信号通路等.
以往对胰岛素敏感性的研究主要关注的是全身和骨骼肌、肝脏和脂肪等胰岛素作用的主要靶器官, 而对心血管胰岛素敏感性的研究相对较少. 近年的研究表明, 胰岛素抵抗还具有组织器官特异性, 心肌和血管胰岛素抵抗可独立于全身胰岛素抵抗(systemic insulin resistance), 并与心血管功能不良及多种心血管病发生发展有密切关系. 比如在心肌缺血早期,心肌组织TNF-α为主的炎症反应可导致心肌胰岛素抵抗, 后者参与缺血性心衰的发生和发展; 动物实验显示, 血管胰岛素抵抗在高血压前期即出现, 并参与血管功能紊乱和高血压的发生发展. 长期有氧运动可改善心血管慢性炎症状态及心血管胰岛素敏感性,降低高血糖、高血脂、肥胖等心血管病危险因素, 促进心血管代谢健康和心血管保护.
3.2 提高心血管抗损性
运动不仅能改善心血管功能, 还可以提高心血管抵抗损伤的能力(抗损性). 研究表明, 单次运动便可降低随后的心肌缺血/再灌注损伤, 而经常运动者能够在停止运动后数月内依然保留这种心脏保护效应. 运动锻炼对于心肌缺血/再灌注损伤的保护效应类似于缺血预处理, 该效应独立于传统已知的心血管病危险因素. 运动提高心血管抗损性的主要机制与运动引起的氧化应激激活机体内源性保护机制, 如激活HIF-1α(hypoxia inducible factor-1α)、Akt-eNOS等促细胞生存信号, 改善线粒体功能, 提高心肌抗氧化能力, 改善胰岛素敏感性, 提高心肌抗损伤和修复能力等有关. 本团队在不同动物的运动模型上均发现, 有氧运动具有缺血预处理样作用, 能够增强心肌Akt的表达和磷酸化, 抑制Caspase 3等促凋亡信号, 提高缺血/再灌注心肌的抗损伤能力, 减轻心肌细胞凋亡和心肌梗死.
4 运动因子与心血管保护
运动促进健康是一种系统、综合性效应. 运动不仅在器官或组织局部产生直接作用, 还通过组织器官之间的交互调控发挥心血管保护效应, 其机制之一是通过运动因子实现的. 运动因子的概念是加拿大学者Tarnopolsky团队于2016年在Nature Reviews Endocrinology中提出的, 泛指运动引起的骨骼肌等组织器官释放的、介导运动所致生物学效应的肽或核酸等生物活性物质. 这一概念目前得到进一步扩展, 指运动时产生或产生增加的一类生物活性物质, 可来源于不同的组织和器官, 可以是蛋白质、核酸等大分子也可以是代谢物等小分子物质, 通过内分泌或旁分泌等方式作用于自身或其他组织器官, 影响组织器官生长、功能活动和机体健康(图2和4). 本团队认为, 运动因子应该具备以下三个基本特性: (ⅰ) 运动时产生或运动促进释放的生物活性物质; (ⅱ) 从组织细胞释放作用于临近细胞或进入血液循环作用于其他器官或组织细胞; (ⅲ) 可影响接受细胞(recipient cell)的生长或功能活动, 通常是介导运动所致的健康效应. 早期发现的运动因子(如IL-6、鸢尾素等)主要来源于骨骼肌, 被称为肌因子(myokine), 近年来不断有新的运动因子被发现和报道, 其来源包括脂肪、肝脏、血管内皮等多种组织细胞.

4.1 肌因子
运动时或运动后骨骼肌分泌多种具有生物活性的细胞因子, 统称为肌因子. 肌因子通过内分泌或旁分泌方式作用于全身各组织器官, 是运动裨益心血管健康的重要机制之一. 肌生成抑制蛋白(myostatin)是第一个被发现的肌因子, 它可以通过激活SMAD信号通路和抑制mTOR信号通路抑制骨骼肌生长. 运动可降低肌生成抑制蛋白的表达, 该效应与运动降低脂肪含量, 促进白色脂肪棕色化以及改善肌无力有关. 心衰时心肌细胞myostatin表达增加具有心脏保护效应,但其也是引起心衰时骨骼肌萎缩的原因之一. IL-6是报道最多的一种肌因子. 运动促进骨骼肌IL-6的分泌, IL-6在运动介导的代谢重塑和抗炎效应中具有重要作用, 能够激活骨骼肌和脂肪中的AMPK信号通路,促进葡萄糖和脂肪酸代谢, 还能促进IL-10和sTNF-R(soluble tumor necrosis factor receptor)等抗炎因子的分泌并抑制TNF-α等促炎因子; 此外, IL-6具有促进肌肉生长和血管生成的作用. 白细胞介素家族中的肌因子还有IL-15, IL-7, IL-8, IL-4和IL-13等, 这些肌因子均参与了运动的健康效应.
鸢尾素(irisin)是近年来被广泛研究的另一种肌因子. 运动促进骨骼肌分泌鸢尾素, 后者能够促进白色脂肪棕色化, 从而促进产热和能量消耗. 运动通过激活骨骼肌PGC-1α信号通路增加FNDC5(fibronectin type III domain-containing protein 5)的表达和剪切, 剪切后被分泌出骨骼肌细胞的FNDC5就是鸢尾素. 鸢尾素主要通过激活靶细胞内MAPK及解偶联蛋白1(uncouplingprotein-1, UCP-1)等信号机制增强线粒体活动, 产生多种生物学效应, 如促进心肌再生、血管新生, 改善内皮依赖性和非内皮依赖性的血管舒张和降低心肌纤维化, 对心衰、心肌缺血/再灌注损伤和其他心血管疾病具有保护作用. 其他报道的肌因子还包括METRNL(meteorin-like protein), 具有改善糖耐量和促产热的作用;FSTL1(follistatin like 1)通过激活eNOS改善内皮功能和促进血管再生; Apelin能够改善胰岛素敏感性, 并通过促进血管舒张, 增强心肌收缩力和促进血管新生等发挥心血管功能保护作用; 肌联素(myonectin)促进脂肪酸代谢; 肌肉素(musclin)促进线粒体生物合成和抑制骨骼肌对葡萄糖的摄取等. 以往发现的这些蛋白类肌因子均是由细胞核基因编码, 最近有研究发现, 线粒体基因编码的MOTS-c也是一种运动因子, 其可以促进机体的运动能力. 除上述蛋白类物质外, 骨骼肌分泌的一些小分子代谢物(如氨基丁酸)、核酸等也可能是肌因子, 这些肌因子通过直接或间接作用参与心血管保护效应.
4.2 脂肪因子
脂肪组织除储存能量外还可分泌多种细胞因子,统称脂肪因子(adipokine). 运动可影响多种脂肪因子的产生和分泌, 尤其是促进脂联素(adiponectin)的分泌而降低瘦素(leptin)的产生. 脂联素是迄今研究最深入的脂肪因子之一, 它能够促进骨骼肌对脂肪酸和葡萄糖的利用并抑制肝脏糖异生, 抑制巨噬细胞促炎因子TNF-α的产生和促进抗炎因子IL-10的产生. 低脂联素血症是2型糖尿病、冠心病和高血压等代谢性疾病的危险因素之一. 脂联素具有心血管保护作用, 可以通过激活AMPK抑制心肌肥大和减轻细胞凋亡, 并通过促进环氧合酶2(Cox-2)表达发挥抗炎效应. 另一个被广为研究的脂肪因子是瘦素, 瘦素主要参与调控机体的脂肪含量和代谢水平. 高瘦素血症和动脉粥样硬化、高血压等心血管疾病密切相关, 研究表明,瘦素参与动脉粥样硬化和高血压等疾病的发生发展,其机制与瘦素增加线粒体ROS产生, 引起炎症反应, 促进平滑肌细胞增值和表型转化, 激活交感神经等有关. 此外, 运动可降低循环内脂素(visfatin)水平, 其与代谢和衰老等生物学过程密切相关.
4.3 非编码RNA
运动可影响多种组织非编码RNA(non-coding RNA, ncRNA)的表达, 这些ncRNAs可在细胞内发挥生物学效应,也可分泌至细胞外调节临近或远隔细胞的功能. 近年愈来愈多的研究显示, 运动可通过ncRNAs发挥心血管保护作用. 有报道运动后骨骼肌中微小RNA(microRNA, miRNA)miR-1, miR-133a及miR-761等表达的变化可促进骨骼肌代谢相关蛋白MAPK及PGC-1α的表达增加, 进而改善机体的代谢, 提高心脏抗损能力; 运动可促进中性粒细胞产生miR-16,miR-17, miR-18a等参与多种炎症反应; 运动促进多种细胞分泌miR-342-5p, 后者靶向进入心脏发挥心脏保护效应; 运动通过调控miR-143, miR-124和miR- 145等的表达参与运动后心脏生理性肥大的发生和发展; 而在心脏发生缺血/再灌注损伤后, 运动可通过抑制miR-214, miR-1和miR-29a的异常表达减轻心肌损伤. MALAT1是一个在糖尿病中升高的长链非编码RNA(long noncoding RNA, lncRNA), 可导致机体胰岛素抵抗, 参与糖尿病的发展, 运动可降低MALAT1改善糖尿病的代谢异常. 这些研究表明,ncRNAs广泛参与了运动所致的心血管生理和病理过程.
循环中的ncRNA主要是以外泌体等细胞外囊泡为转运载体. 外泌体是一类直径为40~100 nm的细胞外囊泡, 内含RNA、DNA、多肽和蛋白质等多种生物活性物质, 机体几乎所有的组织细胞均可释放和摄取外泌体, 后者介导细胞-细胞间的信息传递, 并广泛参与机体生理与病理过程. 研究表明, 急性运动(尤其是高强度运动)可致循环中的外泌体量显著增加, 通常在运动后24小时内循环外泌体数量恢复正常. 有趣的是,研究发现, 长期运动者在非运动状态时血液中外泌体总量虽无明显变化, 但外泌体的“质”(内含的活性因子)发生了改变, 并具有心血管保护效应. 本团队新近发现, 运动后循环血液中外泌体的多种miRNAs表达发生改变并具有特定的生物学意义. 例如, 运动引起的血流剪切力增加可促进血管内皮细胞释放富含miR-342-5p的外泌体, 后者经血液循环被心肌细胞吞噬, 其中的miR-342-5p通过靶向caspase9和Ppm1f, 激活抗凋亡和促细胞生存信号(Akt), 发挥心脏保护作用. 长期运动可促进肝脏释放富含miR-122-5p的外泌体, 促进血管新生. 这些结果提示, 运动可诱导不同组织器官产生多种ncRNAs, 由此构成的“运动RNA簇”参与代谢调节和心血管保护——这可能是运动裨益心血管健康的一个重要机制.
5 运动在心血管疾病治疗和康复中的应用
运动裨益心血管健康, 适度运动锻炼可有效防治心血管疾病已成为全球共识. 2020年, 欧洲心脏病学会(European Society of Cardiology, ESC)发布的心血管病患者运动指南中明确指出, 适当的运动干预对于心血管病患者具有显著的健康效应, 指南对不同心血管疾病的运动干预给出了详细的建议, 但同时指出运动在心血管疾病防治和康复中还有很多问题尚不清楚. 在此以心衰为例简要介绍运动在心衰患者治疗和康复应用中的新观点和进展.
心衰是多种心血管病的终末阶段, 由于心脏功能不足和运动不耐受, 以往认为心衰患者应该严格限制活动, 而这种观点现在被认为是过时甚至错误的.目前认为, 即便对于心衰这样严重的心脏病患者, 适度运动也可给患者带来多方面益处; 运动不仅是治疗心衰的一个辅助方法, 更应该成为稳定性心衰患者的必要治疗手段. 在给心衰患者制定运动处方之前, 首先要对心衰患者做一个系统性的医学评估, 主要包括三个方面: (ⅰ) 排除运动禁忌患者, 比如安静状态或运动时出现低血压或高血压, 疾病处于不稳定状态或者恶化期, 显著的心肌缺血或伴随有严重的肺部疾病等; (ⅱ) 开展基础功能评估, 包括心脏功能的全面检测、并发症、最大运动能力和运动风险等的评估;(ⅲ) 优化治疗方案, 对心衰患者应给予标准的治疗.其中, 心肺运动测试非常必要, 能够评估患者的最大运动能力, 从而为选择适宜的运动强度和运动方式提供依据.
在系统性评估之后, 医生制定的运动处方应该包括运动的类型、频率、时长及强度等. 一般而言, 运动的类型仅被简单分为有氧运动、阻力运动和综合性运动, 具体的运动形式不限, 但运动强度和频率应遵循因人而异及循序渐进的原则. 病情稳定的心衰患者在排除运动风险后应尽早开展运动干预, 运动过程中(尤其是开始阶段)应有医生或其他专业人士的指导和评估, 其中心率是评估运动强度的最常用方法, 可采用最大心率的百分比或心率储备的百分比来评估运动强度, 同时监测和记录运动过程中心律失常、血压异常等的发生情况. 心衰患者的运动方案要根据病情进展和患者状态及时调整, 一般至少3~6个月要调整一次运动方案. 此外, 还要注意充分调动患者运动训练的积极性, 研究显示, 患者良好的心态和积极的配合能够产生更好的健康效果.
HF-ACTIN临床研究结果显示, 中等强度运动能够显著提高心衰患者的最大运动能力, 且运动量越高可能带来的益处更明显, 而运动对佩戴有植入式除颤器的心衰患者并未带来负面影响. 有氧运动适合大多数心衰患者, 一般采用的运动方案为3~5天/周,运动强度为40%~80%的最大耗氧量, 每次20~60分钟,连续的中等强度训练或高强度间歇性训练(适合低风险心衰患者)均可. 研究表明, 耐力运动和阻力运动结合效果更好, 其中阻力运动更适合低风险的心衰患者, 有助于老年患者改善肌肉状态和机体稳定性,通常采用的训练方案为2~3天/周, 每次40%~60%的最大肌力(one-repetition maximum, 1RM)训练. 但阻力运动不能替代有氧运动,可作为有氧运动的补充. 此外, 心衰患者的运动方案还应注意区分心衰的类型,比如射血分数降低的心衰患者不建议进行竞技性运动, 而低风险的射血分数保留性心衰患者可参加部分竞技性运动.
除心衰外, 近年来对冠心病、高血压、糖尿病等的运动处方研究也愈发深入. 由于患者的不同及运动训练的复杂性, 如何针对不同心血管疾病患者制定适宜的运动处方目前还存在诸多挑战, 其中对患者运动强度的精准评估最为重要, 因人而异和风险控制是最重要的原则.
6 问题与展望
虽然运动裨益心血管健康作用已经得到了广泛认可, 但迄今对运动促进心血管健康效应的机制还远不清楚, 其临床应用还主要局限于心脏康复, 且仍处于缺乏精准指导的初级阶段. 此领域目前还存在以下重要问题有待进一步明确.
(1) 以往的研究多关注运动对某一组织器官的局部效应, 对运动健康效应的整合机制研究不够深入.随着各种整合研究策略和多组学技术的建立和成熟,以效应-多组学-分子-功能为范式的研究将为人们认识运动的整体作用机制提供新的认识; 其中多维度组学(包括多组学、多器官及其时-空联合应用)研究策略将愈显其重要性.
(2) 不同人群或患者选择何种运动方式和运动强度会带来更好的健康效应亟需进一步明确. 有研究比较了不同运动方式对机体健康的效应, 发现运动的健康效应与运动的方式有关, 通常团队性运动的健康效果更佳. 此外, 不同运动强度所带来的健康效应也不同: 低强度和中等强度运动对于降低心血管疾病风险和改善代谢具有显著效应, 而高强度运动对于提高心肺适能(cardiopulmonary fitness)具有更好的效果.有研究显示, 在运动总量一定的条件下, 高强度运动伴随的功能提升和健康效应更显著, 提示在相同运动量条件下, 不同运动强度的生物学效应可能存在差异, 但具体机制尚不完全清楚. 不同年龄阶段、不同身体状态下运动方式和运动强度的选择是大众健身关注的一个重要问题. 本团队的研究显示, 无论运动方式、强度和年龄如何, 只要动起来使心率加快、血流加速就有健康裨益. 但运动健身要遵循一个基本原则,即“适可而止(listen to your body)”, 尤其是不同生理或病理状态下(如高血压、糖尿病、心衰等)及老年人,精准确定运动强度尤为重要, 这是临床心血管康复医生特别关注的问题, 也是运动健康领域目前研究的重点和难点之一. 此外, 近年来人们越发注意到生物节律对人体生理病理活动的影响, 因此, 每天在什么时间运动可达最佳健康效果, 即健身运动的“时辰”选择也是目前人们感兴趣的问题. 最近, Zierath团队的研究显示, 对于糖尿病患者每日下午运动比早晨或上午具有更佳的控糖和健康效果.
(3) 运动健康效应的持续时间尚不明确. 以往研究主要关注的是运动的短期效应, 新近研究发现, 长期运动还可能通过表观遗传学修饰产生远期健康效应. 最近一项流行病学研究显示, 7~17岁青少年期间运动量达每周180分钟以上且坚持9个月以上的人群在老年时罹患高血压及2型糖尿病的发病率降低50%以上.此外, 新近发现, 亲代运动能够改善子代健康.这些研究结果提示, 运动可能还具有远期健康效应,但其机制尚不清楚. 此外, 人在成长的不同阶段(如儿童或老年)的运动锻炼是否具有特殊的健康效应及其意义也是近年来学者关注和感兴趣的新问题.
(4) 揭示运动健康效应的分子机制, 尤其是通过各种组学等技术寻找具有健康裨益的运动因子, 是运动健康领域近年研究的一个热点. 运动裨益心血管健康是一种全身系统性效应, 近年运动因子相关新发现为揭示运动所致健康效应的机制尤其是组织器官间交互作用方式提供了新认识, 并可望为研发新的药物或手段模拟运动的健康效应提供新思路和新策略. 阐明运动健康效应中组织器官间的交互作用及其分子机制, 将为精准制定个体化运动处方提供重要依据和指导. 此方面的研究方兴未艾, 并将是运动健康领域研究的前沿和热点.
(5) 运动在临床心血管病防治中的应用潜力巨大,但一些具体问题亟待明确和解决. 我们每个人都自带“内源性药箱”, 如何挖掘并利用好机体自身的内源性健康资源, 尤其是如何针对不同疾病、不同患者制定科学且依从性高的个性化心脏康复运动处方, 亟需深入的基础研究. 此外, 随着当今智能科技的发展, 如何通过现代科技手段, 如各种智能化穿戴、大数据等高效监测并优化个体运动效果, 及时避免由于不合理运动带来的各种不良心血管事件等, 这些都是运动健康领域具有实际意义且亟待攻关解决的重要问题.
(6) 值得关注的是, 中国传统医学中的运动养生方式, 如太极、八段锦等并无剧烈的身体活动, 而是注重“以动运气、身心协调”, 以达健身益寿的功效, 提示健身运动中身-心兼修的重要性, 其中的机制也值得深入探讨和挖掘. 这对于大众运动健康尤其是老龄健康活动的指导及制定具有中国特色的个性化运动处方具有特殊重要的现实意义.
在人类进化过程中, 机体已经形成了复杂而高效的内源性保护机制, 运动是调动机体内源性保护机制、促进健康的有效刺激因素之一. 与药物防治心血管疾病不同, 运动主要是通过调动机体内源性保护机制发挥系统性的心血管保护作用, 是一种经济、安全、快乐、高效的促进心血管健康的方式. 实际上,我国传统中医理论与养生实践早就强调“生命在于运动”. 阐明运动裨益心血管健康的机制, 制定个体化的精准运动处方, 通过合理运动调动机体内源性保护机制, 是促进心血管健康和防治心血管疾病大有可为并亟待开发的重要策略和方向.文献来源:
张星,李嘉,高峰.运动裨益心血管健康:从分子机制到临床应用[J/OL].中国科学:生命科学:1-16[2021-04-06]. http://kns.cnki.net/kcms/detail/11.5840.Q.20210330.1527.006.html.