人类在与白血病的战争中胜利了一次
每当剧中的男女主人公历经千难万险终于走在了一起,但是女主日渐苍白,突然一日高烧不退或者血流不止,瘫倒于男主面前;又或是家庭美满之时,萝莉或者正太突然出现在了惨白的医院,父母强颜欢笑并努力准备二胎,套路模式就可以自动开启了。此时必然会反复出现一个词——造血干细胞移植。此后一切剧情冲突的根源就在于造血干细胞的稀缺,各种情节纠结于不能及时找到合适的供者。当然现实生活中,更多的人会止步于经济压力和对疾病的妥协,这就又是后话了。

人诱导多能干细胞分化成的成熟血细胞(拍摄: Rio Sugimura|Nature Press)
造血干细胞是凭借一“人”之力就能够构建起整套造血系统的细胞。红细胞、白细胞、血小板…… 我们血管里、淋巴管里流淌着的所有有形成分(就是干货)都来自于它。造血干细胞如此神奇,人类自然对它热情高涨,各个研究小组都卯足了劲儿想“多、快、好、省”地培养出造血干细胞,为研究生理病理机制、药物筛选及细胞治疗创造条件。

人诱导多能干细胞形成造血干祖细胞(拍摄: Rio Sugimura|Nature Press)
目前,“生产”造血干细胞的套路主要是使用胚胎干细胞,或者诱导多能干细胞向造血干细胞分化。无论是使用胚胎干细胞,还是诱导多能干细胞,都要先形成拟胚体;再与基质(细胞)共培养;再通过严格控制培养条件,让细胞尽可能多的向造血细胞分化;然后通过连续移植来验证获得的细胞确实能够在移植后建立造血机能,这才能最终证明这些细胞有凭借一己之力重建造血王国的能力。
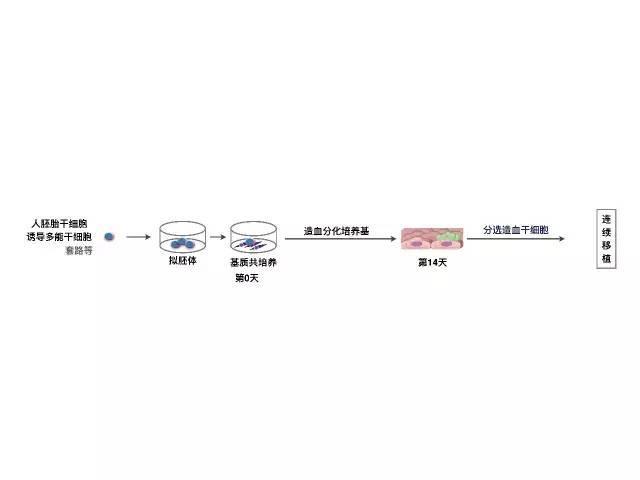
多能干细胞产生造血干细胞流程 (绘制:脑洞谢)
今日,《自然》(Nature)杂志同时在线了两篇研究如何“生产”造血干细胞的文章,异曲同工地向成功迈出了一小步。
哈佛医学院的乔治·戴利(George Daley)研究组之前也用套路培养人的造血干细胞。但是这样培养出来的“产品”不能成功的重建免疫缺陷鼠的造血系统。试了数次之后,他们丢弃了套路。发育学研究表明,在胚胎发育期间,造血内皮细胞会产生造血干细胞。使用基因编辑技术“调教”后的造血内皮细胞,可以直接在小鼠体内完成向造血干细胞的分化。将萌芽直接种在体内,经过半个月的诱导绽放出造血之花。
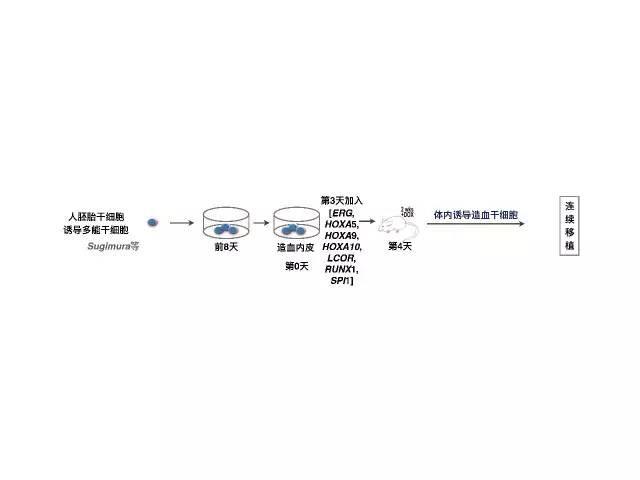
George Daley研究组造血干细胞“生产流程”(绘制:脑洞谢)
康奈尔大学沙欣·拉斐(Shahin Rafii)团队的研究则跳过了从体细胞诱导至多能干细胞,再由多能干细胞分化至造血干细胞的阶段,直接利用内皮细胞,一步到位制造造血干细胞。从内皮细胞直接“蹦出”浑圆的血细胞,想想就让人激动。这样产生的细胞还能在二次移植中保持住造血的功能,简直令人感动。
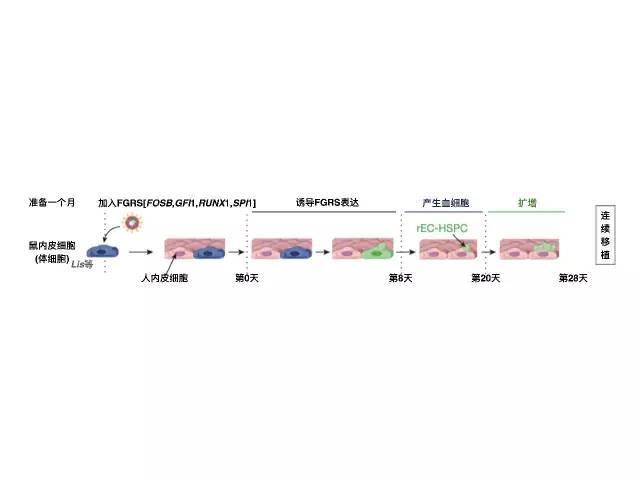
Shahin Rafii团队造血干细胞“生产流程”(绘制:脑洞谢)
如果将这两个研究结合在一起看,就可以直接将“调教”后的人内皮细胞移植到受者,在体内诱导生成造血干细胞,完美翻越“需要经过多能干细胞阶段”,和“移植免疫反应”两座大山。
不过,科学家离“制造”出能够用于临床的造血干细胞,还有很长的路。无论是安全性、简便性,还是经济角度,都还有很多的研究需要进行。 而且,用逆转录病毒将转录因子加入细胞是一种随机插入。也许,使用更新更为稳妥的基因编辑技术(如CRISPR-Cas9)可以弥补此类不足。另一方面,通过“调教”的细胞中,只有一部分完成了“华丽转身”,怎样提高转化率及诱导出来的造血干细胞的均一性都任重而道远。
此外,研究经费,也许才是更棘手的问题。 剑桥大学的研究者卡罗莱娜(Carolina Guibentif)在为《自然》(Nature)撰文报道这两项研究的时候,就提到了经费的问题。这两项研究依靠的内皮细胞及相似的转录因子(RUNX 1、SPI 1)都来自于发育生物学家们对胚胎造血发育过程的研究。假如缩减了此类“貌似无用”的研究经费,缩减掉的还可能是“人造造血干细胞”这种性命攸关的研究赖以进步的基础。
总之,在“多、快、好、省”地培养出造血干细胞的道路上,我们又迈出了一小步。数十年后,造血干细胞移植的桥段也许就没法用了,后人们会发出类似“何不食肉糜”的感叹。