PD-1/PD-L1最新抗癌新进展,抑制癌细胞扩散转移
近日,《Nature》期刊的一篇文章显示,来自于斯坦福大学医学院病理学和发育生物学教授Irving Weissman博士带领团队发现,除了调动T细胞之外,PD-1/PD-L1抗体还可以“解封”肿瘤相关巨噬细胞(tumour-associated macrophages,TAMs),促使它们“吞噬”癌症。(抗癌助手app提醒:了解更多抗癌信息就到全球华人抗癌新药网)团队以“PD-1 expression by tumour-associated macrophages inhibits phagocytosis and tumour immunity”为题,揭示了以PD-1/PD-L1抗体为代表的免疫检查点抑制剂以一种完全不同的方式对抗癌症。
浸润在肿瘤组织中的巨噬细胞称为肿瘤相关巨噬细胞,是肿瘤微环境中最多的免疫细胞。肿瘤发生初期,这类细胞负责识别并清除肿瘤细胞。但是随着肿瘤病情的发生与发展,巨噬细胞又会辅助癌变细胞的扩散和转移。
研究人员希望这一新发现将改善、扩大免疫疗法的效率和使用范畴。
癌细胞如何与PD-1里应外合?
免疫细胞中的T细胞负责侦查、清理受损或者病变细胞,但是这类细胞有时候会错误地攻击健康细胞,引发自身免疫性疾病,例如红斑狼疮或者多发性硬化症。PD-1是一种表达于T细胞表面的免疫检查点分子,通过抑制T细胞响应而保护机体免于过度活跃的免疫系统,被称为“刹车分子”。
大约10年前,科学家们发现了癌细胞的“狡猾之处”,它们会利用PD-1免疫检查点掩饰自己的“坏人身份”。也就是说:肿瘤表面表达的PD-L1蛋白会与T细胞表面的PD-1蛋白结合,向免疫系统传递“自己人、别杀我”的信号,从而躲避免疫细胞的侦查和攻击。为了阻挡这些漏网之鱼,科学家们研发出阻断PD-1/ PD-L1结合的抗体。
除了T细胞,抗体还解放了TAMS
Weissman教授表示:“PD-1/ PD-L1抗体是癌症免疫治疗的‘明星药物’。虽然大多数科学家认为这一类抗体是通过释放T细胞实现抗癌目标,但是现在,我们找到了另一种方式。”研究团队发现,PD-1受体同样会抑制肿瘤相关巨噬细胞的抗癌活性。“这一类巨噬细胞表面同样表达有PD-1受体,当PD-1或者PD-L1被抗体封锁,TAMS抑制接触,从而恢复吞噬、消灭癌细胞的能力。”Weissman解释道。
他们以患癌小鼠为模型发现,PD-1/ PD-L1抗体会增强吞噬作用,有效抑制肿瘤扩散、延长小鼠寿命。
同时,Weissman课题组研究的另一种抗体——CD47抑制剂同样也存在这种机制。他们发现,CD47抑制剂会激活巨噬细胞“吞噬”癌细胞。这意味着,CD47抗体同样也是癌症免疫治疗的重要研究方向之一。
但是,已有的研究还不足以表明,肿瘤相关巨噬细胞助力PD-1/ PD-L1抗体有效对抗肿瘤的程度。研究人员认为,这一最新发现有助于通过调动T细胞或者巨噬细胞攻击癌症,研发出新的抗癌方法。
巨噬细胞作为人体自身免疫系统的重要组成部分,可以自动识别患者体内异常的细胞。Weissman课题组的研究说明了,PD-1/PD-L1抗体的抗癌效果或比我们现在认知的具有更广阔的发展和应用空间。
PD-1、PD-L1的免疫治疗
簡介:PD-1全称程序性死亡受体1,英文名字为programmed death 1,是一种重要的免疫抑制分子。PD-L1全称程序性死亡受体-配体1,英文名字 programmed cell death-Ligand 1,是大小为40kDa的第一型跨膜蛋白。
正常情形下:免疫系统会对聚集在淋巴结或脾脏的外来抗原产生反应,促进具有抗原特异性的T细胞增生。而细胞程序化死亡受体-1(PD-1)与细胞程式死亡-配体1(PD-L1)结合,可以传导抑制性的信号,减低T细胞的增生。
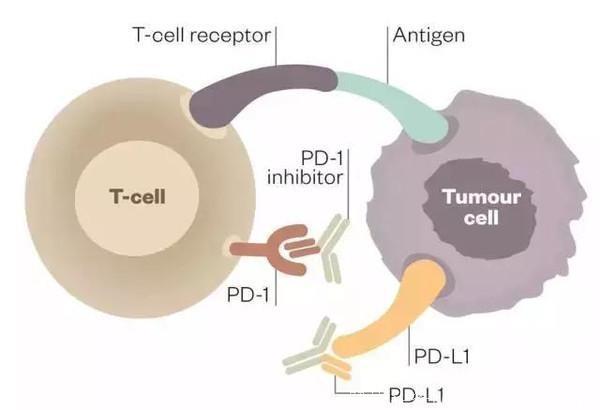
在腫瘤中:肿瘤细胞逃避T细胞摧毁的一种途径是通过在它表面产生PD-L1,当免疫细胞T细胞表面的PD-1识别PD-L1后,可以传导抑制行信号,T细胞就不能发现肿瘤细胞和向肿瘤细胞发出攻击信号。
免疫療法:PD-1免疫疗法的作用机制是针对PD-1或PD-L1设计特定的蛋白质抗体,阻止PD-1和PD-L1的识别过程,部分恢复T细胞功能,从而使T细胞可以杀死肿瘤细胞。
pd-1
為什麼不用PD-1檢測?PD-1/PD-L1抑制劑均只做PD-L1檢測
有些厂家在检测时同时进行了肿瘤细胞PD-1的检测,首先,PD-1单抗是表达于效应T细胞上的,而非肿瘤细胞。其次,虽然PD-L1在肿瘤细胞或是浸润的免疫细胞的表达对疗效均有预测作用,但是PD-1的检测还未证实与疗效有相关性。
PD-L1檢測水平:PD-L1的检测是基于蛋白水平,目前有些检测厂家针对于此进行基因检测(DNA),目前还没有研究证实PD-1/PD-L1的基因拷贝情况与免疫治疗的单抗疗效有独立预测关系。这种蛋白对等基因的简单跨越还是具有争议的,不知是否有数据支持,望在无数据支持情况下勿误导大众。
免疫治療與PD-L1表達
2016年10月25日,FDA批准Pembrolizumab(Keytruda,健痊得)用於治療PD-L1高表達(>50%)的轉移性非小細胞肺癌患者。這是目前唯一獲批用於一線治療非小細胞肺癌的的抗PD-1免疫療法。PD-L1是一個免疫相關的可表達在癌細胞上的生物靶標。在診斷疾病時,測量PD-L1的表達水平有助於了解患者腫瘤狀況,及有助於制定適合患者本身的治療方案。PD-L1的表達水平或會成為是否將免疫治療納入治療計劃的關鍵。
有關研究顯示PD-L1的表達比例與Pembrolizumab的治療效果相關,PD-L1表達比例超過50%的患者(與PD-L1表達比例為1-49%及小於1%的患者比較)使用Pembrolizumab有更長的腫瘤反應時間、無進展生存期及總生存期1。同時使用Pembrolizumab的PD-L1表達比例超過50%的患者,與使用常規化療的患者相比,有更好的療效和更低的副反應:中位無進展生存期為10.3個月(常規化療為6.0個月),中位半年生存率為80.2%(常規化療為72.4%),腫瘤反應率為44.8%(常規化療為27.8%),中位反應時間>2年(未到)(常規化療為6.3個月),所有副作用發生率為73.4%(常規化療為90.0%),3-5級中重度副作用發生率為26.6%(化療方案為53.3%)2。
有關PD-L1檢測
有數個檢測平台可以進行PD-L1表達水平的測試(如採用28-8,E1L3N和SP142等試劑盒)。當中FDA唯一批准的是日本DAKO公司出品的22C3試劑盒,而22C3試劑盒也是Pembrolizumab研發至獲批為治療非小細胞肺癌一線藥物的過程中一直使用的試劑盒。
目前香港已可以提供採用DAKO公司出品的22C3試劑盒的PD-L1表達水平測試。該測試的實施十分方便。一般情況下,患者需提供石蠟包埋組織塊或者組織切片及其病理報告,7-10個工作天內便有結果。
PD-1/PD-L1抑制剂对常見肿瘤的临床疗效
1. 非小细胞肺癌(FDA批准Keytruda)
非小细胞肺癌(NSCLC)的临床研究中,nivolumab和pembrolizumab在NSCLC经治患者和其他患者中均显示出较高的活性。nivolumab治疗NSCLC经治患者,可以使总缓解率达到17%,缓解的持续时间可以达到18个月以上。所有剂量的研究显示鳞状细胞癌患者中位总生存期为9.2个月,非鳞状细胞癌患者中位总生存期为10.1个月[16]。pembrolizumab(Keytruda)的总缓解率可达到21%。PD-L1阳性的NSCLC患者的总缓解率为19%~23%,PD-L1阴性的NSCLC患者的总缓解率为9%~13%[17]。因此表达PD-L1的肿瘤对这些药物更加敏感,但是在PD-L1阴性的患者中也有缓解的情况。PD-L1抑制剂MEDI4736在所有的NSCLC患者中的总缓解率达到23%。其Ⅰ期临床试验结果表明,对PD-L1阳性和阴性的患者的缓解率分别为39%和5%[18]。因此MEDI4736对PD-L1阳性患者的缓解率更高。此外针对NSCLC的287例患者,PD-L1高表达的患者接受MPDL3280A治疗明显比多烯紫杉醇效果好,患者ORR和PFS分别为:38%vs.13%,9.7个月vs.3.9个月。比较PD-L1阳性和PD-L1阴性的患者,ORR和PFS分别为:18%vs.8%,3.3个月vs.1.9个月[19]。因此,MPDL3280A对PD-L1阳性患者的治疗效果更好。
2. 黑色素瘤(FDA批准Opdivo)
Weber等[20]的一项Ⅲ期临床随机试验结果显示单药nivolumab治疗晚期黑色素瘤患者获得的平均疾病进展时间是ipilimumab的两倍多(6.9个月vs.2.9个月),且当nivolumab与ipilimumab联合使用时患者受益较大(11.5个月)。同样联合治疗使患者获得的缓解率极大地提高为57.6%,单药nivolumab为43.7%,而单药ipilimumab的缓解率仅为19%。联合组平均肿瘤负荷退缩率(反应程度)为52%,单药nivolumab为34%。与之相比,接受单药ipilimumab的患者肿瘤总负荷增加了5%。因此,初始以nivolumab为基础的治疗可显著提高黑色素瘤患者生存,单药nivolumab或联合ipilimumab初始治疗的疗效显著优于单药ipi-limumab。另一项基于173例黑色素瘤患者的非对照Ⅰ期临床试验研究显示,pembrolizumab使24%的黑色素瘤患者体内的肿瘤体积出现缩小,效果至少持续1.4~8.5个月[21]。
一项新的Ⅲ期临床试验(KEYNOTE-006)结果显示,keytruda治疗2周和3周最常见的不良反应比较得出:疲劳(20.9%vs.19.1%),腹泻(16.9%vs.14.4%),脸红(14.7%vs.13.4%)和瘙痒(14.4%vs.14.1%)。ipilimumab治疗最常见的不良反应是瘙痒(25.4%),腹泻(22.7%)和疲劳(15.2%)。结果表明keytruda的治疗效果优于ipilimumab[22]。
3. 晚期霍奇金淋巴瘤(FDA批准Keytruda)
一项nivolumab治疗霍奇金淋巴瘤(HL)的Ⅰ期临床试验研究显示,nivolumab的安全性较好,治疗过程中未出现危及生命的不良反应或治疗相关死亡[23]。23例复发难治HL患者中(有87%的患者既往经3种以上治疗失败,包括干细胞移植和Adcetris),经nivolumab治疗后,总缓解率为87%(20/23),完全缓解率为17%(4/23)。可见PD-1/PD-L1检查点抑制剂可以调动患者自身的免疫系统来识别并杀死某些类型的血癌细胞。
另一项keytruda的Ⅰ期临床试验表明,目前对已获批药物均无治疗效果的晚期霍奇金淋巴瘤(HL)患者,接受keytruda和opdvio治疗后,能够达到完全缓解。在29例复发难治HL患者(新药brentuximabve-dotin治疗失败或干细胞移植治疗失败)中27例对keytruda治疗表现出一定水平的响应或肿瘤缩小,且keytruda的耐受性较好,未出现严重的治疗相关不良反应,仅有3例患者出现轻度治疗相关不良反应[24]。
4. 肝癌(FDA未批准)
一项Ⅰ/Ⅱ期临床试验表明nivolumab在进展期肝癌中安全有效[25]。研究中75%的患者接受过全身治疗,包括68%的患者接受过索拉非尼的既往治疗。在42例可评价患者中,8例(19%)在接受nivolumab治疗后获得缓解(肿瘤缩小30%以上)。其中4例取得了12个月的持续缓解,1年的总生存率为62%。病情稳定者占48%,最长的可达17个月。nivolumab安全性和耐受性良好,即使在HBV和HCV感染者中也非常安全,因此HBV与HCV感染似乎不是治疗效果的一个决定因素。
5. 乳腺癌(FDA未批准)
Cimino-Mathews等[26]在2015 AACR年会上指出,MPDL3280A在晚期三阴性乳腺癌中表现出了持久的疗效。研究共纳入54例转移性三阴性乳腺癌受试者,每3周接受一次MPDL3280A注射。在所有21个可评估疗效的受试者中,免疫细胞的PD-L1水平达到或超过5%。总体有效率为19%,24周无进展生存为27%。其中完全缓解2例,部分缓解2例,有3例患者在停药之后仍然维持了缓解。受试者的目标病灶缩小,但其他部位出现了新的病灶,但这些新病灶最终还是对治疗表现了应答。在54例可评估安全性的受试者中,MPDL3280A耐受良好。
6. 直肠癌(FDA未批准)
Le等[27]一项Ⅱ期临床试验结果显示,在41例晚期癌症患者中有10例直肠癌患者检测示基因错配修复缺陷,采用keytruda治疗后40%患者有肿瘤缩小,而包括胃癌、小肠癌和卵巢癌在内有错配修复缺陷患者的应答率高达71%。相反,错配修复功能完好的患者对keytruda的应答率为0。由于错配修复功能缺陷在Ⅱ~Ⅲ期结直肠癌的发生率约10%~15%,Ⅳ期<5%,因此PD-1抗体免疫治疗在错配修复功能缺陷的结直肠癌中得到良好的疗效。
7. 卵巢癌(FDA未批准)
2015 ASCO年会上2项研究结果指出,针对PD-1和PD-L1的单克隆抗体对于既往治疗过的进展期卵巢癌显示出抗癌活性。一项Ⅰb期临床试验研究中,75例难治性或复发性卵巢癌的患者接受了静脉ave-lumab注射治疗,病情稳定率为44%,疾病控制率为54.7%。14.7%的患者肿瘤缩小≥30%,包括2例透明细胞癌。临床相关的3级和4级治疗相关不良事件发生率仅为8%,未发生4级或5级不良事件[28]。
另一项Ⅰb期临床研究中,使用22C3抗体克隆鉴定膜表面PD-L1阳性情况(表达率≥1%)。在筛选的96例患者中,49例(51%)PD-L1阳性患者接受了pembroli-zumab治疗,其中26例可评效,客观有效率为11.5%。另外11.5%患者肿瘤缩小<30%,6例患者(23.1%)病情稳定,疾病控制率为34.6%[29]。pembrolizumab安全性好,毒性低,无治疗相关死亡,也未出现因治疗相关不良事件而停药的病例,表明PD-1抑制剂pembrolizumab深度治疗后PD-1阳性的患者有效率较高。
8. 恶性胸膜间皮瘤(FDA未批准)
胸膜间皮瘤(pleuralmesothelioma,PM)是一种原发于胸膜间皮的罕见、侵袭性恶性肿瘤,治疗选择极其有限。一项Ⅰb期临床试验研究表明,在25例胸膜间皮瘤患者中,接受keytruda治疗后总缓解率(ORR)为28%,且48%的患者病情稳定,疾病控制率达到76%。20%以上患者出现治疗相关不良事件,包括疲乏(24%)、恶心(24%)。研究中未发生治疗相关不良事件的停药,也无治疗相关的死亡事件(抗癌助手app提醒:了解更多抗癌信息就到全球华人抗癌新药网)。因此key-truda治疗恶性胸膜间皮瘤疾病具有较好的疗效。