抗癌三十六计:一文读懂早期非小细胞肺癌中立体定向放射治疗的应用决策
编译:肿瘤资讯编辑部 来源:肿瘤资讯
近日,美国放射肿瘤学会(ASTRO)在《Practical Radiation Oncology》杂志上发布立体定向放射治疗(SBRT)应用指南,同时就4个临床重要问题给出推荐意见。
过去20年来,放疗技术的进步使得SBRT成为可能。随着研究证据的累积,SBRT已成为医学上不可手术,外周型NSCLC的标准治疗方案。然而,临床上关于大病灶、多发的、复发的或中央型肿瘤,SBRT的应用有较多的不确定性。此外,对于医学上可手术或未经组织确诊的患者,复发的患者,SBRT的应用仍存在争议。针对上述临床上存在的挑战,ASTRO临床实践指南系统性的总结了SBRT用于早期NSCLC的证据。无论何种情景,均推荐进行多学科讨论,考虑入组临床研究,在进行临床决策时充分考虑患者的意见。
方法
指南制定委员会针对4个“重要问题(Key question,KQ)”系统性检索了1995年1月~2015年11月期间,SBRT用于早期(T1-2 N0)NSCLC治疗或挽救性治疗的研究。
指南推荐分为“强”或“有条件的”两类。“强”推荐指的是专家委员会有足够信心:治疗干预的获益大于风险(或风险大于获益),且(几乎)所有的专家均会作出这一推荐;“有条件的”推荐指的是获益和风险均等或不确定,且多数的专家会作出这一推荐,但仍有一部分专家不会。
根据质量等级,将支持推荐的研究证据分为3类:
•高:非常有信心--真正的获益与预期估计的非常接近
•中等:一般有信心--真正的获益非常有可能与预期估计的接近,但也有可能存在较大差异
•低:信心不足--真正的获益与预期估计的可能存在较大差异
专家委员会还就是否同意指南推荐进行投票(5个等级:强烈反对—>非常同意)。当≥75%的投票者选择“同意”或“非常同意”时,认为这一推荐达成共识,否则需修改后再行投票。
临床指南
KQ1: 对于医学上可手术的T1-2 N0的NSCLC患者,什么情况下SBRT是合适的?
KQ 1A:任意I期可手术的NSCLC患者,考虑进行SBRT时,需要一位胸外科医生的评估,最好能有多学科讨论,减少专家意见的偏倚。

KQ 1B:“无特别手术风险”(如预期手术病死率<1.5%)的I期NSCLC患者,在临床试验外,SBRT不推荐作为手术的替代治疗手段。可以和患者讨论SBRT,但必须声明SBRT>3年的长期生存数据目前还未成熟。对于这类患者,肺叶切除联合系统性纵隔淋巴结清扫仍然是推荐的治疗方案(部分选择性患者可能会考虑进行亚肺叶切除)。
KQ 1C:对于“高手术风险”(如,不能耐受肺叶切除,但可考虑亚肺叶切除)但I期NSCLC,鼓励与患者讨论SBRT作为可能的手术替代方案。但必须声明虽然SBRT可以降低短期的疾病风险,但>3年的长期生存数据目前还未成熟。

KQ2: 对于医学上不可手术的T1-2 N0的NSCLC患者,什么情况下SBRT是合适的?
•对于中央型的肿瘤
KQ 2A:相比于外周型肿瘤,SBRT用于中央型肺肿瘤的风险更高。应避免使用3次分割放疗。
KQ 2B:SBRT用于中央型肺肿瘤应该采用4或5次分割。遵循体积和最大剂量限制,可以增加安全性。对于进行SBRT风险很大的中央型患者,可以考虑采用6-15次的大分割放疗。

•对于肿瘤直径>5cm的患者
KQ 2C:对于治疗比可接受的>5cm肿瘤,SBRT是一个合适的治疗选择。遵循体积和最大剂量限制,可以增加安全性。

•对于没有组织确诊的患者
KQ 2D:尽可能的在SBRT之前进行组织活检,获得恶性肺结节的组织学诊断。

KQ 2E:对于拒绝活检,接受过非诊断性活检,或有活检禁忌症的患者,可以进行SBRT。对于没有获得组织学确诊为恶性肿瘤,计划接受SBRT的患者,推荐进行多学科讨论,并达成共识:影像学特征和临床特征(患者和环境因素)均与肺恶性结节一致。

•同时性多原发肺肿瘤
KQ 2F:多原发肺肿瘤(MPLCs)和胸内转移肺癌很难区分,推荐多学科团队评估。

KQ 2G:对于可疑MPLCs的患者,推荐采用PET/CT,头颅MRI检查,帮助区分胸内转移型肺癌。是否进行侵袭性的纵隔镜分期,需视患者情况而定。

KQ 2H:对于同时性MPLC患者,SBRT可以考虑作为根治性治疗选择。相比于单个病灶的患者,SBRT用于同时性MPLC可以取得同等的局部控制率,且毒性相当,但患者的生存率更低。

•全肺切除术后,剩余肺新发原发肺肿瘤的患者
KQ 2J:在进行过全肺切除的患者,可考虑采用SBRT作为异时性MPLC的根治性手段。相比于单个病灶的患者,虽然SBRT用于异时性MPLC可以取得同等的局部控制率,毒性可接受,但较基线有更高肺容量的患者,SBRT用于全肺切除患者毒性可能更大。

KQ3.对于医学上不可手术的早期肺癌的“高风险”患者,如何进行个体化的SBRT,保证足够的剂量消灭肿瘤,同时减少对正常组织的损伤
•非常接近或侵犯纵隔组织(支气管树,食管,心脏等)
KQ 3A:对于非常接近近端支气管树的肿瘤,SBRT应该采用4-5次分割。考虑到既往报道的严重毒性,内科医生们应尽可能去满足前瞻性研究中已经明确过的限制因素。

KQ 3B:对于靠近食管的肿瘤,考虑到既往报道的严重的食管毒性,内科医生们应尽可能去满足前瞻性研究或文献报道中已经明确过的限制因素。

KQ 3C:对于靠近心脏或心包膜的肿瘤,SBRT应该采用4-5次分割(心脏、心包膜和大血管的严重毒性发生率较低)。遵循体积和最大剂量限制,可以增加安全性。

•肿瘤邻近或侵犯胸壁
KQ 3D:对于T1-2邻近胸壁的肿瘤,SBRT是合适的。SBRT后常见1-2度的胸壁毒性,采用保守治疗后可缓解。对于外周型靠近胸壁的肿瘤患者,应告知其这一常见毒性。
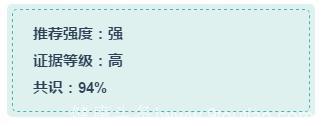
KQ 3E:相比于邻近胸部的肿瘤,对于侵犯胸壁的cT3患者,也可以穿使用SBRT,没有明确证据显示疗效降低或毒性增大。

KQ4.对医学上不可手术患者,SBRT作为下述治疗后的挽救治疗方案?
•常规分次放射治疗后
KQ 4A:常规分次放射治疗后,因既往报道有更好的局部控制率和预后,部分选择性患者可行挽救性SBRT。

KQ 4B:常规分次放射治疗后,再行挽救性SBRT的患者,需告知其严重的(包括致命性)的毒性。

KQ 4C:常规分次放射治疗后的患者,再行挽救性SBRT的患者选择是一个非常个体化的过程。放疗医生在开始治疗前应充分评估患者,肿瘤以及治疗因素。

•SBRT后
KQ 4D:在SBRT后选择患者进行挽救性SBRT是一个高度个体化的过程。放疗医生在开始治疗前应充分评估患者,肿瘤以及治疗因素。

•亚肺叶切除后
KQ 4E:在亚肺叶切除后选择患者进行挽救性SBRT是一个高度个体化的过程。放疗医生在开始治疗前应充分评估患者,肿瘤以及治疗因素。

参考文献
1.Videtic GMM, Donington J, Giuliani M, et al: TEMPORARY REMOVAL: Stereotactic body radiation therapy for early-stage non-small cell lung cancer: Executive Summary of an ASTRO Evidence-Based Guideline. PractRadiatOncol, 2017
