永不复发!刚得诺贝尔奖就被证明可有效治疗癌症,基因编辑技术或先造福人类
姚策是痛苦的,错换28年人生,错失了无数可能;现在又被癌症折磨,忍受病痛。据身边人所说,他“有时候疼得在床上趴着、顶着,痛苦的呻吟不断”。
滚蛋吧,肿瘤君
癌症,也就是恶性肿瘤,正摧残着无数患者。
世卫组织今年2月发布了《2020年世界癌症报告》。报告预计,2018年,全世界约有960万人死于癌症。

《2020年世界癌症报告》 (图源:WHO)
而中国,占新增癌症病例的23%以上,死亡人数约占全球的30%。
“恶性肿瘤死亡占居民全部死因的23.91%”
癌症的根本原因在于基因突变。
人体之中的基因有上万个,具体个数还不得而知,学界还存在争论。而其中和癌症直接相关且已知的,大概有100多个。
人成长的过程,其实就是细胞增殖的过程,这是生物体的重要生命特征,细胞以分裂的方式进行增殖。
细胞分裂,会连带着基因一起复制,从而保证遗传性状的稳定性。
人体不同的细胞其生命周期是不一样的,以具有凝血作用的血小板为例,其寿命只有7-14天。
也有一些活的比较长,比如红细胞,平均寿命可以达到120天,骨细胞差不多10年才更新一次。
当然,对于心肌细胞、神经细胞这样的不可再生细胞来说,你活多久,它们就活多久。
为了维持正常的机理,细胞会不断分裂替代死去的细胞。在人活着的几十年里,细胞会发生多次增殖分裂,再加上需要复制的基因如此之多,很难不出错。
这些复制出错的细胞,不会像工厂的次品一样被销毁,相反,它们还具有无限增殖、可转化和易转移三大特点。
它们,就是癌细胞。

肺癌细胞 (图源:Cancer Research UK)
癌细胞很大,1个顶5个正常细胞。
上面提到的人体细胞分裂是有次数限制的,一般认为约为50多次。但癌细胞不一样,它可以无限增殖。
简单来说,它不遵守“计划生育”政策。
所以,癌症,特别是发展到晚期,在癌细胞数量已经很多的情况下,是很难治愈的。
而我们常说的癌症晚期,其实就是癌细胞已经扩散到了全身,导致病情失控,这就是由癌细胞已转移的特点导致的。
毫不夸张的说,它们是人体内的“流浪杀手”。
这个杀手每年害死的人以百万计。有没有什么治疗手段呢?
治疗,千斤难敌四两
大家最熟知的治疗癌症的方法,无疑就是手术和化疗。
手术就是将癌细胞病灶切除,但这种方法治不了已扩散的癌症,对于某些特定的癌症,如白血病也无可奈何。
化疗也就是化学药物治疗,其实就是吃药。这种方式对人体正常细胞的伤害很大,常伴随着脱发、出血和呕吐等症状。
除了这两种,还有放射治疗、免疫治疗、靶向治疗等。这些治疗方式也并非一劳永逸,经常会出现癌症复发的情况。
上周,一篇新发表的研究成果宣称可以有效治疗癌症,解决了复发的问题,并且突破了现有递送系统潜在毒性和肿瘤细胞编辑效率低两大阻碍。
发表该成果的以色列研究团队称:
"...具有潜力永久破坏肿瘤存活的基因,其可以克服传统癌症治疗的重复给药的限制,提高治疗效果,并且需要的处理较少"。
我们先来看一下这次实验的成果:
一次脑内注射治疗,患癌小鼠平均寿命增加一倍,抑制肿瘤生长50%,提高生存率30%!
抑制肿瘤生长,并提高实验小鼠80%的总生存率!
这一治疗方案不同于手术和化疗,它从癌细胞产生的根源入手:既然细胞分裂过程中难免出现基因突变,那我把这种突变切除不就好了吗?
为此,研究团队开发了一种用以运送切除工具的东西,非病毒脂质纳米颗粒(LNP):
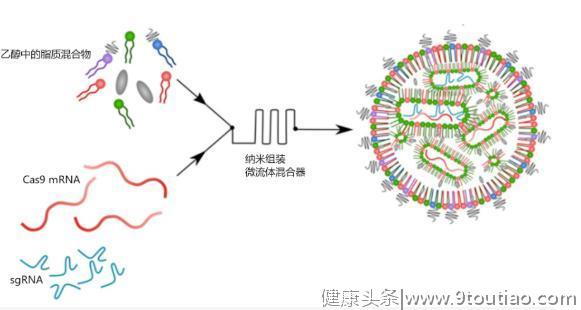
LNP制备图
脂质纳米颗粒(LNP)技术比较成熟,常用来递送RNA药物、疫苗或基因编辑工具等。在一般我们接种的灭活疫苗中,通常也会用脂质物来包裹弱化或灭活的毒株。
LNP有什么好处呢?
在此之前,人类也用过其他东西,比如病毒还运送RNA药物、疫苗等。比如这两天才出来的阿斯利康新冠疫苗,用的就是毒性弱化的腺病毒为载体。
这种运送系统是有风险的,因为它本身就具有一定毒性。
用LNP就完全没有这种问题。
运送系统潜在毒性的问题得到了解决,那么基因编辑的效率怎么提高呢?
魔盒中的希望
上个月,今年的诺贝尔化学奖授予了两位研究CRISPR/Cas9基因编辑技术的女科学家。
CRISPR/Cas9基因编辑技术正是此次以色列团队中采用的方案。
CRISPR是原核生物基因组内的一段重复序列,是细菌在与病毒的斗争中形成的一种免疫机制。
CRISPR/Cas9系统的结构并不复杂,可以说是简约高效:
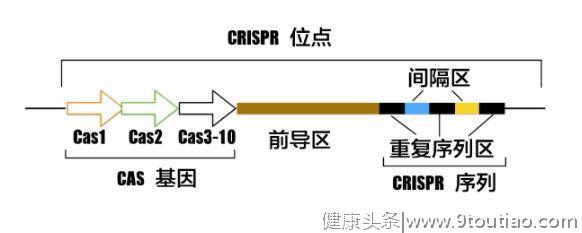
CRISPR结构(图源:http://blog.sciencenet.cn/blog-3160644-983657.html))
左边的Cas基因目前已经发现了10个,其中Cas9是发展最为成熟的一种,因此也被广泛应用。
右边被称作CRISPR序列(CRISPR array),最重要的是间隔区,其中包含了病毒的DNA信息,相当于一个病毒DNA黑名单。
从上面的LNP制备图中我们可以发现,脂质物组成了一个圆,将Cas9基因和sgRNA包裹在其中。
进入人体后,外层的脂质会在细胞中酶的作用下被分解,内部的Cas9基因和sgRNA就暴露了出来。
sgRNA即向导RNA,其作用在于指导Cas9识别癌细胞的基因靶位,Cas9则会像剪刀一样将癌细胞的基因剪断。这样一来,癌细胞就无法再复制了。
在动物实验中,这一技术表现出来的编辑效率很不错。在针对胶质瘤的实验中,其可对高达约70%的癌细胞基因组进行编辑,而在卵巢癌实验中,这一比例达到了约80%。
这一比例越高,对癌症基因的阻断效果就越好。
更重要的是,CRISPR/Cas系统这个免疫武器是有记忆的,癌细胞的DNA片段被存在间隔区黑名单中。当这些癌细胞尝试复制基因的时候,就会被再次切断。
被切断的基因组将变为线性,无法进行复制和表达,最终被酶降解掉。
需要说明的是,利用CRISPR/Cas9基因编辑技术治疗癌症并不是该团队的首创,这一想法在几年前就已经提出了。
就在今年年初,武汉大学的研究团队就开发了一种基于天然聚合物的基因治疗递送系统,将CRISPR-Cas9基因编辑质粒特异性递送至肿瘤细胞核。
以色列团队此次实验的意义在于,它首次证实CRISPR/Cas9系统可以有效治疗活体动物转移性癌症的研究。
此外,CRISPR/Cas9-LNP治疗方案仅针对的是胶质母细胞瘤和转移性卵巢癌。不过,胶质母细胞瘤是最恶性的胶质瘤,5年存活率不足10%;卵巢癌又是妇科常见的恶性肿瘤之一。以色列团队选择这两种癌还是很有代表性的。
技术和原理是相通的,运用到其他类型的癌症上理论上也是可行的。
除了癌症,在其它病症治疗方面也已经有了成功的动物实验先例。
2017年,美国国家眼科研究所研究人员吴志健(音译)及同事利用CRISPR/Cas9基因编辑技术成功阻止了实验鼠视网膜退化并改善了视觉。
有人称基因编辑是“潘多拉魔盒”,可能污染人类基因,甚至导致人类灭绝。而我认为,在那之前,或许它可以拯救更多人。
毕竟,除了灾祸和瘟疫,魔盒里面也还有希望。
人类毫无疑问是脆弱的。但幸运的是,总有那么一小群人在保护我们,尝百草的李时珍是,穿梭在病房间的医护是,实验室里埋头苦干的科学家也是。
作为享受这些成果的普通人,我们向这些保护者致以敬意,也希望这些技术早日投入临床。
或许,就在你读完这篇文章的时候,就有一个人因为癌症离开了这个世界。