美国癌症协会年终重磅盘点:2019上市的抗癌药物信息汇总
多年来,手术是癌症治疗的唯一支柱,直到今天,它仍然是癌症治愈性治疗的基础。1896年,放射治疗成为癌症治疗的第二大支柱,目前大约50%的患者接受放疗以缩小或消除肿瘤或防止局部复发。细胞毒性化学疗法是癌症治疗的第三大支柱。
三种传统治疗方法走向极致,但远未达到人们期望的治疗目标。随着我们对癌症生物学的理解取得了显着进步,包括鉴定了导致某些患者肿瘤生长的众多基因突变,为精准医学的新时代奠定了基础,基于基因突变的靶向治疗更加精准,更加有效,同时比化疗的毒性更低因此,它们不仅可以挽救癌症患者的生命,还可以使这些人拥有更高的生活质量。
在即将步入2020年的时刻,美国癌症协会盘点了2019年具有重大意义的,FDA批准的针对不同癌症的新药物,我们一起来看下。
膀胱癌
01厄达替尼
2019年4月,FDA批准了首款用于膀胱癌的靶向疗法-Balversa(erdafitinib),用于化疗后病情进展的,存在FGFR3或FGFR2基因突变的晚期膀胱癌的成年人。
Balversa“代表了第一个针对转移性膀胱癌患者的易感FGFR基因改变的个性化治疗。”
在II期研究中,32%接受Balversa治疗的患者完全或完全肿瘤缩小,其中2%完全消退。平均响应时间为5.4个月。
厄达替尼药品信息
中文名称:厄达替尼
英文名称:Erdafitinib
商品名称:Balversa
生产厂家:Janssen Biotech
美国上市日期:2019-04-12
适应症:
Balversa是一种激酶抑制剂,用于治疗局部晚期或转移性尿路上皮癌的成人患者,这些患者需满足以下条件:
(1)有FGFR3或FGFR2基因突变,以及
(2)在至少一种先前的铂类化疗方案进行中或化疗后出现疾病进展,包括新辅助或辅助铂类化疗方案治疗的12个月内。
用法用量:
(1)在启用Balversa治疗之前,先确认肿瘤标本有FGFR基因突变。
(2)推荐初始计量:为每天一次,8mg/次/天,若达到标准则增加至9mg/次/天。在初始剂量治疗后的第14至21天评估血磷水平,若血磷水平<5.5mg/dL且没有眼科疾病或2级及以上级别不良反应,则增加剂量至9mg/次/天。
(3)可与食物或不与食物整片吞服。
乳腺癌02阿特珠单抗
02阿特珠单抗
美国时间3月8日,FDA给三阴性乳腺癌患者送上最好的节日礼物!
全球首款用于治疗乳腺癌的免疫检查点抑制剂-atezolizumab(阿特珠单抗)获批上市!
FDA加速批准atezolizumab(TECENTRIQ®,Genentech Inc.)与紫杉醇蛋白结合,用于成人患者无法切除的局部晚期或转移性三阴性乳腺癌(TNBC)。这一疗法要求患者的肿瘤PD-L1表达是阳性(PD-L1(肿瘤浸润性免疫细胞)表达≥1%),而PD-L1的表达情况需由FDA批准的伴随诊断设备VENTANA PD-L1 (SP142)进行检测。
实验结果显示:
- 在意向治疗人群中,atezolizumab组的中位PFS为7.2个月,而安慰剂组为5.5个月。
- 在PD-L1阳性人群中,atezolizumab组的中位PFS为7.4个月,安慰剂组为4.8个月,同时减少40%疾病进展或死亡的风险!
阿特珠单抗药品信息
中文名:阿特珠单抗
英文名:Atezolizumab
商品名:TECENTRIQ
生产厂家:基因泰克
美国上市日期:2019年3月8日
适应症:TECENTRIQ是一种程序性死亡-配体1(PD-L1)阻断抗体,用于治疗以下患者:
(1)局部晚期或转移性尿路上皮癌具有以下特征的患者:
①不适合含顺铂的化疗,由FDA批准的检测来确定肿瘤表达PD-L1(PD-L1染色的肿瘤浸润性免疫细胞覆盖肿瘤面积的5%以上)。
或者
②无论PD-L1的状态如何,不适合任何含铂类的化疗。
或者
③在铂类化疗期间或化疗后疾病出现进展,或在新辅助或辅助化疗后12个月内疾病出现进展。
(2)与贝伐珠单抗、紫杉醇和卡铂联用,用于无EGFR或ALK基因突变的转移性非小细胞肺癌患者的一线治疗。
(3)在铂类化疗期间或化疗后出现进展的转移性非小细胞肺癌。肿瘤有EGFR或ALK基因组突变的患者应在FDA批准的治疗过程中出现疾病进展后再接受TECENTRIQ治疗。
(4)与紫杉醇蛋白结合,用于成人患者无法切除的局部晚期或转移性三阴性乳腺癌(TNBC)。这一疗法要求患者的肿瘤PD-L1表达是阳性(PD-L1(肿瘤浸润性免疫细胞)表达≥1%)
用法用量:
(1)转移性尿路上皮癌或曾经治疗过的非小细胞肺癌:
静脉输注1200毫克,每3周1次,每次输注时间超过60分钟。
(2)一线治疗非鳞癌非小细胞肺癌:
静脉输注1200毫克,输注时间超过60分钟,之后在同一天给予贝伐珠单抗、紫杉醇和卡铂,每3周一次最多给予4-6个周期。化疗完成后,给予TECENTRIQ 1200mg 静脉输注,再给予贝伐珠单抗,每3周一次。
若患者能耐受第一剂TECENTRIQ,则后续输注时间可能超过30min即可。
(3)对于TNBC患者:
其肿瘤表达PD-L1的推荐的剂量是840mg,在60分钟内静脉输注,然后给与白蛋白紫杉醇100mg / m 2。对于28天的周期,在第1天和第15天施用atezolizumab,并且在第1,8和15天施用紫杉醇蛋白结合直至疾病进展或不可接受的毒性。
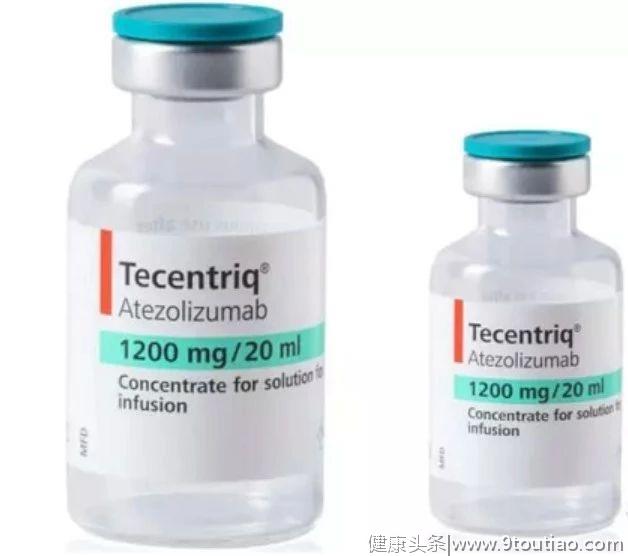
剂型规格:1200mg/20mL(60mg/mL)溶液,单剂量小瓶。
03阿培利司
2019年5月24日,美国制药巨头宣布,FDA批准Piqray (alpelisib,代号BYL719)与氟维司群联合用于治疗绝经后妇女,具有激素受体阳性,人表皮生长因子受体-2阴性(HR + / HER2-),已基于内分泌治疗的经基因检测证实存在PIK3CA突变,晚期或转移性乳腺癌的男性和女性。
在HR + / HER2-晚期乳腺癌患者中,有40%由于存在PIK3CA突变而面临预后很差的结果, Piqray是第一个也是目前唯一批准的专门针对这部分乳腺癌患者的靶向药。
在代号为SOLAR-1的临床试验中,与单独使用氟维司群相比,新药Piqray(alpelisib,既往称为BYL719)联合氟维司群治疗PIK3CA突变的HR + / HER2-晚期乳腺癌患者中的中位无进展生存期几乎翻了一倍(11.0 vs 5.7个月)!
阿培利司药品信息
中文名称:阿培利司
英文名称:alpelisib
商品名称:Piqray
生产厂家:诺华
美国上市日期:2019-5-24
头颈癌04派姆单抗
04派姆单抗
2019年6月14日,免疫疗法药物Keytruda(pembrolizumab)获得FDA批准,可用于晚期头颈癌患者的一线或初始治疗。
该批准适用于头颈部鳞状细胞癌扩散或复发且无法通过手术切除的患者。在这种情况下,Keytruda可以与化学疗法一起使用,或者如果癌细胞具有一定水平的PD-L1蛋白,也可以单独使用。
FDA的批准基于882名晚期头颈部鳞状细胞癌患者的试验。结果显示,Keytruda加化疗组的总生存期为13个月,而化学加爱必妥组则为10.7个月。在肿瘤中PD-L1蛋白检测为阳性的患者中,单独使用Keytruda的患者应答率更高。
派姆单抗药品信息
中文名称:派姆单抗
英文名称:pembrolizumab
商品名称:Keytruda
生产厂家:默沙东
美国上市日期:2019-6-14
用法用量:Keytruda的输注通常是每三周一次。
副作用:最常见的副作用是疲劳,疼痛,食欲下降,瘙痒,皮疹,腹泻,恶心,发烧,咳嗽,呼吸急促和便秘。Keytruda也有可能导致免疫系统攻击身体的其他部位,这可能导致某些人出现严重的副作用。
肺癌05阿特珠单抗
05阿特珠单抗
2019年3月19日,美国食品和药物管理局(FDA)宣布,批准对PD-L1抑制剂atezolizumab(阿特朱单抗,Tecentriq)与卡铂和依托泊苷联合用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。
基因泰克公司(Roche)首席医疗官兼全球产品开发主管Sandra Horning:
“阿特珠单抗Tecentriq是第一个批准用于初期治疗广泛期小细胞肺癌的癌症免疫疗法!到目前为止,这种疾病的治疗进展有限,我们很高兴为患者带来一种潜在的新标准治疗方案,与化疗相比,这种方案已被证明可以提高生存率。”详情点击:速递|刚刚!首个一线治疗小细胞肺癌的免疫疗法获批!
目前,FDA已经批准了三款免疫疗法用于小细胞肺癌的治疗,用药信息如下:
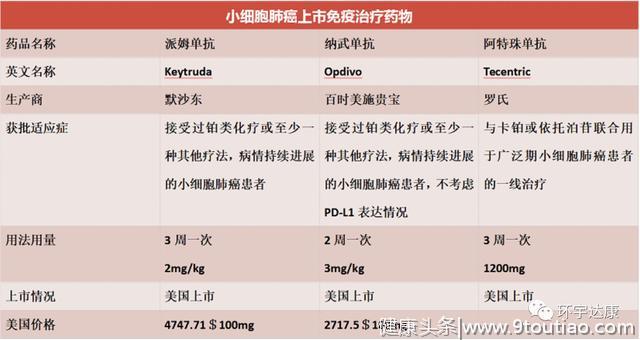
淋巴瘤06Polivy
06Polivy
2019年6月,FDA批准了首个抗体-药物结合物,用于治疗弥漫性大B细胞淋巴瘤,这是美国最常见的非霍奇金淋巴瘤。抗体-药物偶联物是与化学疗法结合的靶向药物。靶向药物找到癌细胞,然后释放化学物质以破坏它。新药Polivy(polatuzumab vedotin-piiq)已获批准与化疗药物苯达莫司汀和利妥昔单抗一起使用。这也是首款免疫化疗(chemoimmunotherapy)药物。
FDA根据随机对照临床试验中观察到的完全缓解率批准了该药物。
80名患有DLBCL的患者,这些患者在平均接受2种治疗后病情进展或复发。结果显示,标准治疗组的完全缓解率为18%,实验组的完全缓解率高达40%!
Polivy药品信息
英文名称:polatuzumab vedotin-piiq
商品名称:Polivy
生产厂家:基因泰克
美国上市日期:2019-6-1
不限癌肿的广谱抗癌药07Rozlytrek
07Rozlytrek
2019年8月,FDA加速批准了全球第三款广谱“治愈系”抗癌药Entrectinib(Rozlytrek,恩曲替尼,RXDX-101)上市,用于治疗成人和儿童患者神经营养原肌球蛋白受体激酶(NTRK)融合阳性、初始治疗后局部晚期或转移性实体肿瘤进展或无标准治疗方案的实体瘤患者,以及ROS1阳性非小细胞肺癌(NSCLC)患者。
这是FDA第三次批准基于不同类型肿瘤的常见生物标志物的癌症治疗,而不是肿瘤起源的身体部位。PD-1的获批和TRK抑制剂的成功,为不区分肿瘤来源广谱抗癌药物快速发展奠定了基础,让梦想照进现实!

拉罗替尼(Larotrectinib)和恩曲替尼的上市无疑给很多晚期患者带来了全新的选择和希望,但,目前国内均未上市。美国的售价也在每个月10-20万人民币,令国内的患者只能望药兴叹!好消息是,近期这两款药物都开展了国际多中心的临床试验,国内负责招募的医院都在进行最后的伦理审查,相信将很快开始正式的招募工作,符合条件的患者可通过全球肿瘤医生网医学部申请入组。详情点击:不限癌种,不限分期!两款“治愈系”抗癌药已上市!免费用药攻略快收藏
Rozlytrek药品信息
中文名:恩曲替尼
英文名:Entrectinib
通用名:Rozlytrek
获批适应症:治疗NTRK基因融合阳性的晚期复发实体瘤的成人和儿童患者,以及ROS1阳性非小细胞肺癌(NSCLC)患者。
研发公司:由生物制药公司Ignyta研发,2017年年底被罗氏耗资17亿收购。
作用机制:
恩曲替尼是一种具有中枢神经系统活性的酪氨酸激酶抑制剂(TKI),能够穿过血脑屏障,是临床上唯一一种被证明针对原发性和转移性脑疾病具有疗效的TRK抑制剂,并且没有不良的脱靶活性(off-target activity,未达到预先设定的目标);
可以阻断ROS1和NTRK激酶活性,并可能导致ROS1或NTRK基因融合的癌细胞死亡。
上市时间及国家:
2019年6月18日,经PMDA批准在日本上市
2019年8月16日,经FDA批准在美国上市
剂型:口服胶囊100/200mg
更多新疗法为癌症患者照亮生命之光!
以上十项突破性进展盘点,仅仅是今年众多研发热点中的一小部分,众多的新药研发,创新技术纷纷在路上,相信2020年将有更多的药物获批上市!想了解各类癌症可用的靶向及免疫治疗药物可后台留言。
还有一个好消息是,前段时间,国家医保局、人力资源社会保障部公布谈判成功的药品名单。让广大癌症患者翘首以盼的22种抗癌药终于纳入医保报销目录,相比平均零售价,平均降价65%,大部分进口药品谈判后支付标准低于周边国家或地区市场价,将极大减轻肿瘤患者的用药负担!国家看到了老百姓的需求,并力争在最短时间内让患者用的起药!抗癌药降价,进医保,这次真的不只是说说!让我们为祖国点赞!
相信随着医药改革、医学研究和无数患者与医疗工作者的共同推动,癌症患者今后会越来越好,带着这个美好的祝愿,希望社会越来越好,希望医疗越来越好!大家一定要坚定信心,前方的路会越来越亮!