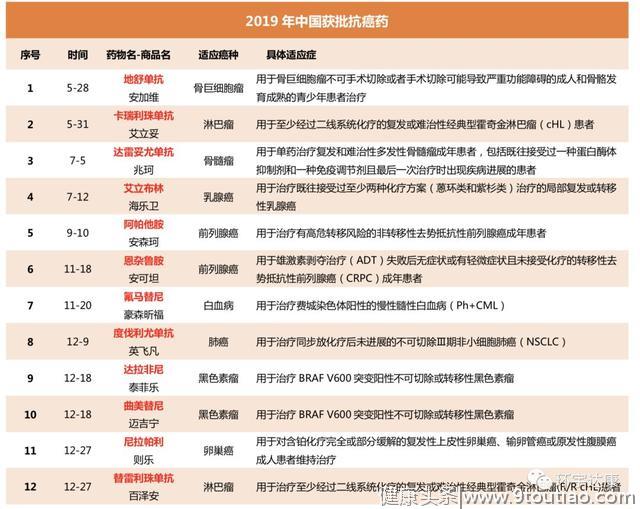
盘点!2019年,中国一共获批12种抗癌新药
01
首个骨巨细胞瘤治疗药物地舒单抗注射液在中国获批
2019年05月28日,安进公司骨巨细胞瘤靶向药安加维(通用名:地舒单抗注射液,Denosumab Injection)获国家药品监督管理局有条件批准上市,用于骨巨细胞瘤不可手术切除或者手术切除可能导致严重功能障碍的成人和骨骼发育成熟的青少年患者治疗。
02
第三个国产PD-1单抗卡瑞利珠单抗在国内获批上市
2019年05月31日,恒瑞医药宣布其自主研发的PD-1抑制剂卡瑞利珠单抗(艾瑞卡)正式获得国家药品监督管理局批准,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(cHL)患者的治疗,为临床抗击肿瘤再添利器,同时也为患者带来更多希望。
03
首个单抗类多发性骨髓瘤新药获批上市
2019年7月5日国家药品监督管理局有条件批准达雷妥尤单抗注射液(Daratumumab Injection)进口注册申请,用于单药治疗复发和难治性多发性骨髓瘤成年患者,包括既往接受过一种蛋白酶体抑制剂和一种免疫调节剂且最后一次治疗时出现疾病进展的患者。
04
晚期乳腺癌新药登录中国,开启抗癌新篇章!
2019年7 月 15 日,中国国家药品监督管理局已批准卫材原研抗癌药甲磺酸艾立布林(海乐卫®)上市,用于治疗既往接受过至少两种化疗方案(包括蒽环类和紫杉类)治疗的局部复发或转移性乳腺癌患者。
05
中国首个新一代雄激素受体抑制剂获批治疗前列腺癌患者
2019年9月10日,安森珂(阿帕他胺片)获得国家药品监督管理局加速批准,用于治疗有高危转移风险的非转移性去势抵抗性前列腺癌(NM-CRPC)成年患者。
06
前列腺癌重磅新药恩杂鲁胺在中国获批
2019年11月18日,中国国家药品监督管理局(NMPA)批准安可坦®(英文商品名:Xtandi®,通用名:恩扎卢胺或恩杂鲁胺,enzalutamide)的新药上市申请,该药用于雄激素剥夺治疗(ADT)失败后无症状或有轻微症状且未接受化疗的转移性去势抵抗性前列腺癌(CRPC)成年患者的治疗。
07
国内首款自主研发治疗白血病新药获批问世
2019月11月26日,氟马替尼(商品名: 豪森昕福),豪森自主开发的抗肿瘤1类新药,获NMPA批准上市,拟用于治疗费城染色体阳性的慢性髓性白血病(Ph+CML)。
08
国内首个PD-L1单抗获批治疗肺癌
2019年12月9日,国家药品监督管理局更新了PD-L1单抗Imfinzi(durvalumab,度伐利尤单抗)的办理状态(受理号为JXSS1800040/41),变更为“审批完毕-待制证”。Imfinzi此次获批用于治疗同步放化疗后未进展的不可切除III期非小细胞肺癌(NSCLC),这是国内上市的第6个免疫检查点制剂,也是第1个在中国内地上市的PD-L1单抗。
09
BRAF突变好搭档:达拉非尼+曲美替尼中国获批!
12月19日,国家药品监督管理局宣布,诺华肿瘤的达拉非尼-Dabrafenib(Tafinlar)和曲美替尼-Trametinib(商品名Mekinist)双靶向联合治疗药物在中国获得上市许可,适用于治疗BRAF V600突变阳性不可切除或转移性黑色素瘤。目前,已经在美国、欧盟、日本等多个国家和地区批准上市。
10
卵巢癌重磅创新药尼拉帕利获批
12月27日,再鼎医药宣布国家药品监督管理局已经批准则乐®(尼拉帕利)作为对含铂化疗完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者维持治疗的新药上市申请。作为一种强效、高选择性的PARP抑制剂,一天口服一次,用药极其方便,并且在用药之前,无需进行BRCA或其它生物标志物检测。
11
国内自主研发PD-1替雷利珠单抗获批治疗淋巴瘤
2019年12月27日,百济神州自主研发的抗PD-1抗体药物百泽安(通用名:替雷利珠单抗注射液)正式通过国家药品监督管理局(NMPA)批准,用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(R/R cHL)患者。
http://www.nmpa.gov.cn/WS04/CL2042/
"