北京协和医院核医学科朱朝晖教授等人Q1区文章
协和论文拾粹--41
北京协和医院核医学科朱朝晖教授等人于2018年2月发表于Web of Science数据库Q1区杂志“ Theranostics ”上的文章“First-in-human study of PET and optical dual-modality image-guided surgery in glioblastoma using 68Ga IRDye800CW-BBN”
影响因子“ 8.537 ”
首次应用于人体的68Ga-IRDye800CW-BBN PET与光学双模态探针引导胶质母细胞瘤手术的临床研究
作者:李德岭*,张静静*,迟崇巍*,肖雄, 王军梅, 郎立新,Iqbal Ali,牛刚,张力伟,田捷#,季楠#,朱朝晖#,陈小元#
目的
尽管使用了荧光引导手术(FGS),但对于多形性胶质母细胞瘤(GBM),因其在术前诊断和术中治疗时手术医生仍有受限,因此手术实现最大安全切除仍是一项重大挑战。目前,将术前评估与术中指导相结合的综合方法则为最大限度地安全切除难以接近的肿瘤迈出重要一步。
实验设计
我们开发了一种新型68Ga-IRDye800CW-BBN PET/近红外荧光(NIRF)双模态成像探针,对GBM中表达的胃泌素释放肽受体(GRPR)具有靶向性。
首先对原位U87MG神经胶质瘤异种移植模型进行临床前在体肿瘤动物模型成像和FGS评估。
随后,通过GBM患者进行首次前瞻性队列研究(NCT 02910804)完成术前PET评估和术中FGS。
结果
使用术中近红外导航系统可精确切除小鼠模型中的脑原位肿瘤。
14例GBM患者前瞻队列研究显示:术前PET阳性摄取与术中NIRF信号之间存在良好的相关性。
体内外肿瘤荧光信号显著高于邻近脑组织(p <0.0001)。
以病理金标准为参照,42个荧光指导采样位点的荧光敏感度和特异度分别为93.9%(95%CI 79.8%-99.3%)和100%(95%CI 66.4%-100%)。
示踪剂对人体安全,在切除范围满意的情况下,未发生新发神经功能缺损。
6个月无进展生存期(PFS)为80%,两名新诊断患者获得长期PFS。
结论
最初研究表明,通过相同的脑胶质瘤分子受体进行整合术前、术中靶向成像的新型双模态成像技术是可行的,改善了术中GBM可视化和最大安全切除的比例。
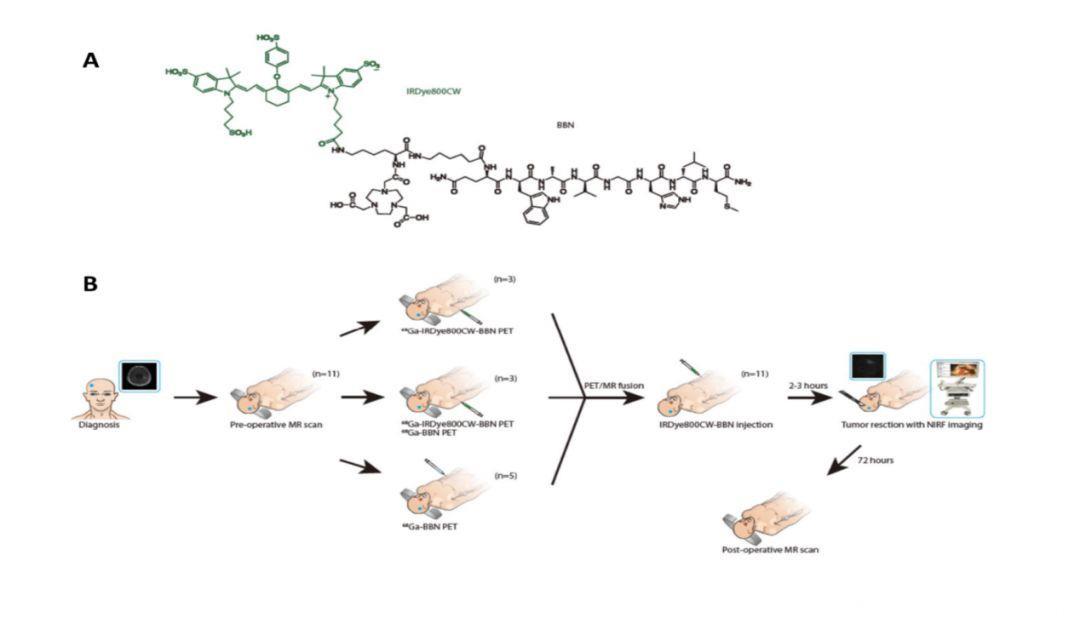
图1. IRDye800 CW-BBN示踪剂的化学结构以及这一首次人类研究的方案。
(A)BBN(黑色)的IRDye800CW(绿色)的化学结构。
(B)GBM患者的入选和研究方案。

图 2. 术中荧光引导下手术治疗GBM。
荧光图像证实了裸鼠的肿瘤存在(A)。
荧光图像逐步方式评估残存肿瘤(B)。
荧光和彩色图像显示所有的荧光组织都从小鼠中移除(C)。
H&E图像证实了肿瘤的结果(D)。
比例尺,术前行,5毫米; 术中行,5毫米; 术后排3毫米。
比例尺,H&E第2列,1,0.2毫米,分别为1-3行。
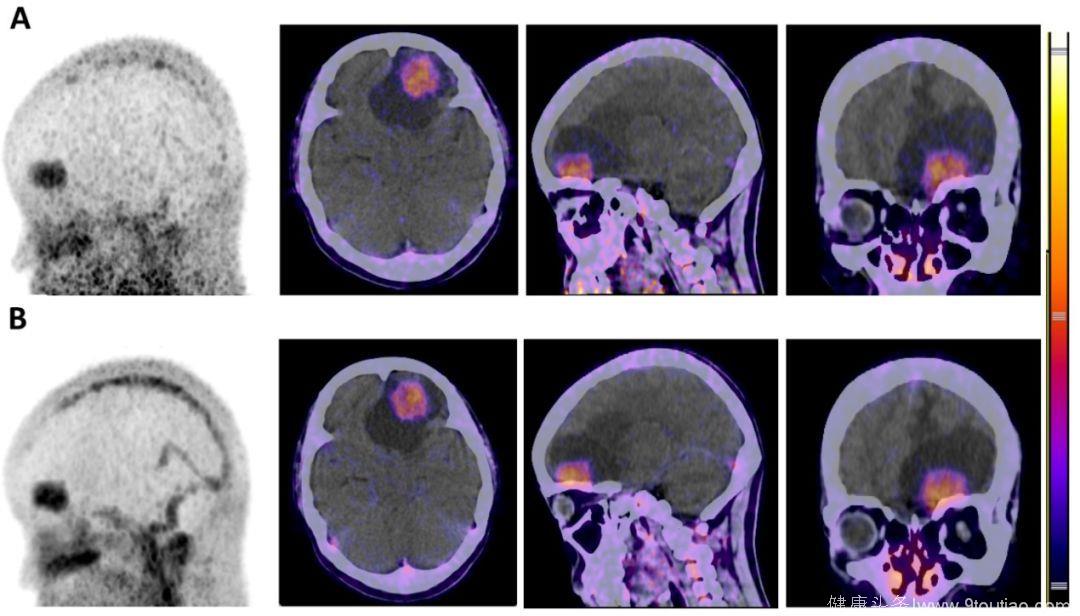
图3. 对于新诊断的GBM患者,68Ga-NOTA-BBN和68Ga-IRDye800-NOTA-BBN示踪剂PET/CT中的类似摄取模式(A)。
68Ga-NOTA-BBN(7-14)PET MIP和在68Ga-NOTA-BBN输注后30min的PCT/CT图像(B).
68Ga-IRDye800 NOTA-BBN(7-14)PET MIP和在68Ga-IRDye800-NOTA-BBN给药后60min的PCT/CT图像。
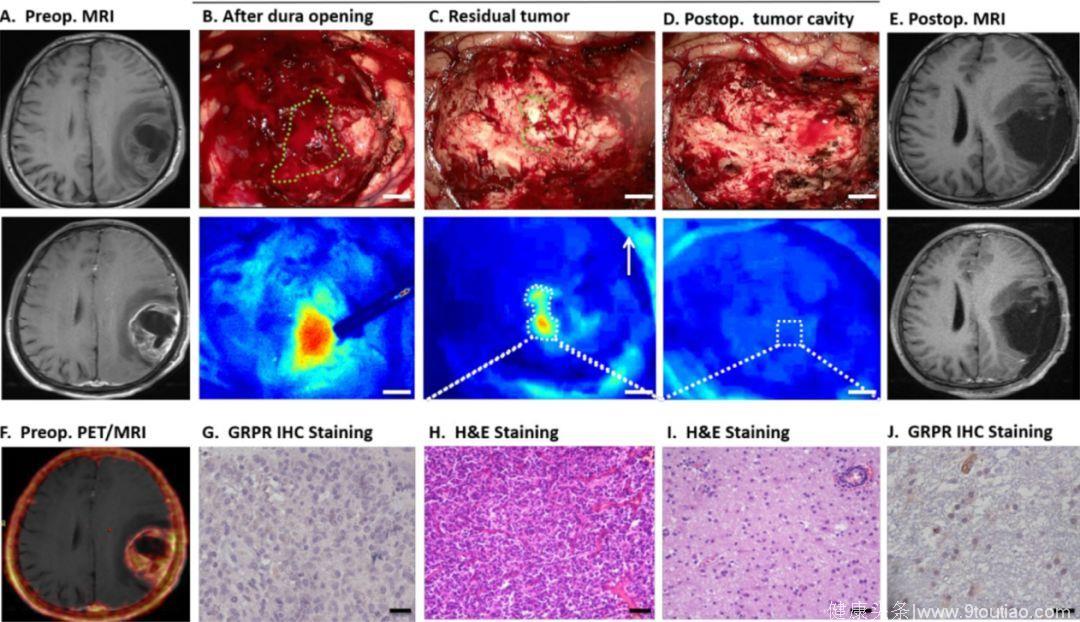
图4. 68Ga-IRDye800-BBN PET/NIRF双模式成像引导患者进行GBM切除术。轴位T1加权(T1W)MRI显示55岁男性左颞顶叶胶质母细胞瘤(功能区III)静脉注射钆30min后增强(A)。融合的68Ga-BBN PET/MRI显示阳性探针摄取具有明显的边缘(F)。硬膜开放后,NIRF成像系统可见明显的荧光肿瘤,在白光成像(B,比例尺,5mm)处用绿色虚线表示。值得注意的是,血液不是荧光的,并且不影响肿瘤可视化。通过术中白光显微镜(C)很难区分残留肿瘤(用绿色虚线表示)和邻近正常脑组织;然而,在深部肿瘤腔(C)中残留肿瘤是荧光的并且通过H&E染色(H,比例尺50um)证实并且具有丰富的GRPR阳性细胞(G,比例尺20um)。切除残留荧光的肿瘤后,腔内未见荧光(D),沿腔内进一步的小组织灶经H&E染色(H)证实为正常脑组织,仅可见少量散在的GRPR阳性细胞(J)。术后增强MRI显示增强区完全切除(E)。
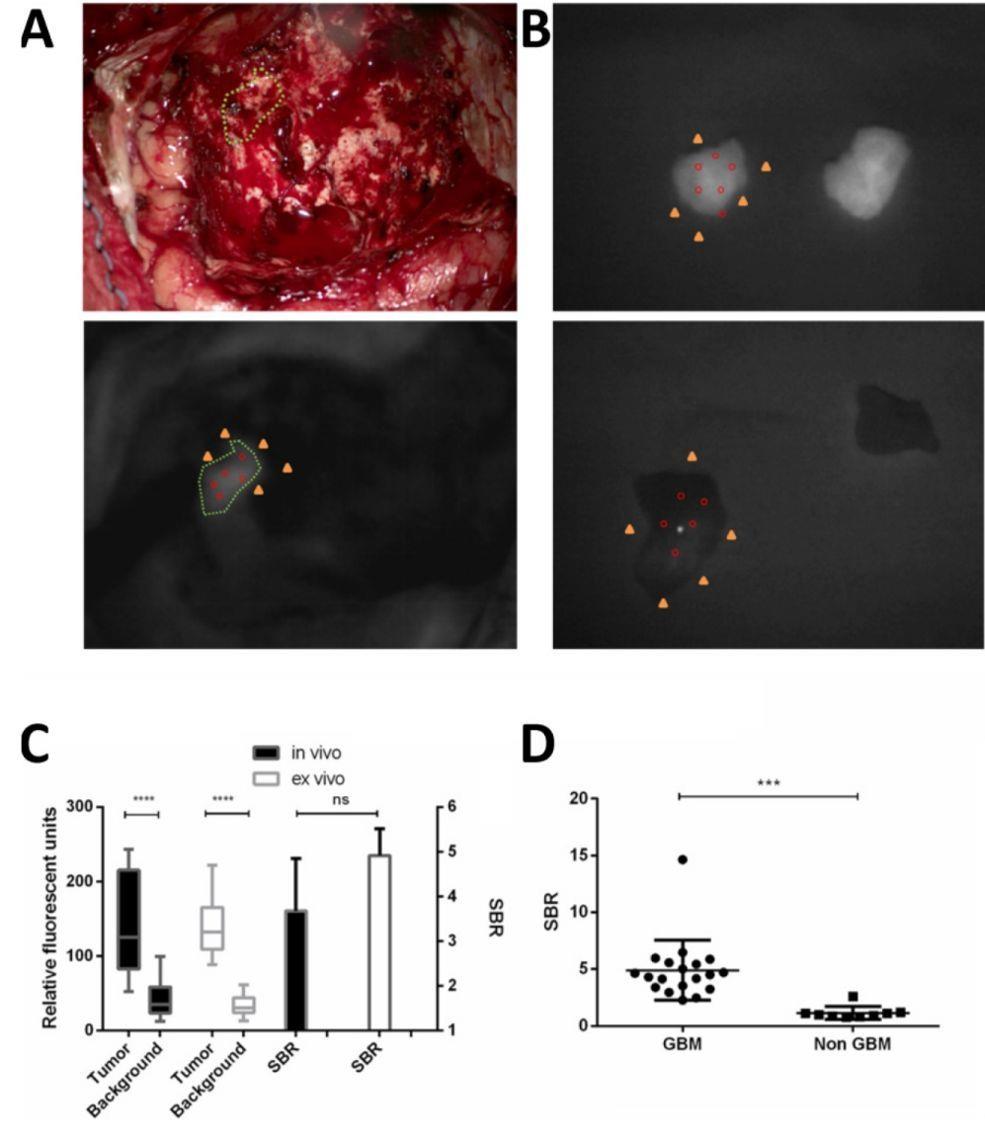
图5. 体内和体外标本病理证明为GBM或邻近脑组织的定量荧光成像。在体内残留肿瘤的术中荧光成像期间获得相对荧光单位(RFU),并在白光上叠加NIRF区域(A)。 (B)中显示了由病理证实的GBM组织和邻近脑组织的离体组织的荧光情况。展示了RFU计算的图例。在大体肿瘤(红色圆圈)荧光中选择5个点且在背景(黄色三角形)周围的皮质或肿瘤腔中选择另外5个点,计算平均RFU并且因此计算信号背景比(SBR)。肿瘤的RFU显着高于背景,体内和离体的(**** p <0.0001)。但体内和体外组织的SBR没有显着差异(C)。病理学SBR显示GBM离体组织显着高于非GBM(*** p <0.001)。数据是RFU和SBR±SD。
表1,该GBM队列的临床特征,肿瘤位置,临床症状和荧光引导手术。 记录MRI和PET术前肿瘤体积的定量评估,切除范围以及术中荧光。
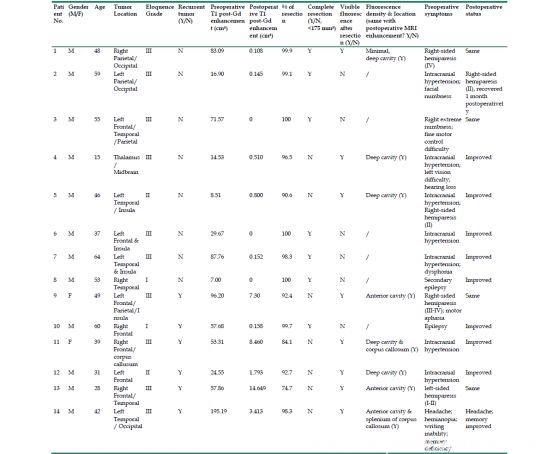
表2.患者随访资料包括术后治疗,生存概况和相关病理分析。
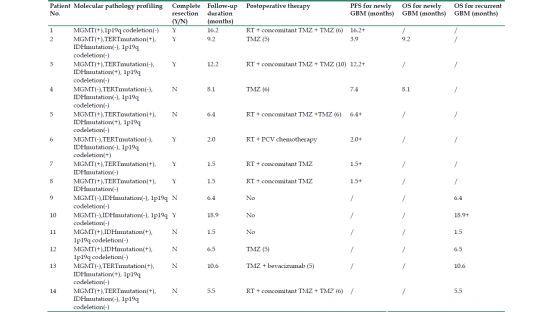
RT(放疗),TMZ(替莫唑胺),PCV(丙卡巴肼,洛莫司汀,长春新碱),PFS(无进展生存期),OS(总生存期)。
评论
胶质瘤达到完全切除仍是一个世界性的难题。术中白光显微镜无法区分肿瘤边缘与正常脑组织。 5-氨基乙酰丙酸(5-ALA)荧光引导下手术(FGS)可对术中肿瘤切除进行实时可视化指导,然而5-ALA无法在术前评估总体摄取,特别是继发胶质母细胞瘤。另一种临床使用的光学探针荧光素钠是一种非特异性的荧光物质,它在细胞外聚集,与BBB的不完整是相关的。目前尚无针对胶质瘤患者使用PET和MRI进行术前评估以及使用相同分子靶标进行术中影像引导手术的技术。
该研究首先经过多步化学合成纯度≥95%的68Ga-IRDye800CW-BBN,并进行GBM动物模型的临床前研究。14例患者于术前接受68Ga-IRDye800CW-BBN PET/CT或68Ga-IRDye800CW-BBN PET /MRI检查,并将PET图像与相应的术前增强核磁共振图片进行融合分析。
全部入组患者于术前接受1mg 68Ga-IRDye800CW-BBN 静脉用药后进行FGS,并于术中测定相应参数。术后以病理结果及相应随访结果评定手术效果。
在研究具体实施中,应避免告知主刀医生、神经放射科医生及病理科医生其专业领域以外的研究内容,降低发表性偏倚。研究期间,应注意对研究对象的护理,观察并及时对患者出现的不良反应对症处理。
这项首次在人体中的研究凸显了68Ga-IRDye800CW-BBN应用于PET/NIRF双模态技术在对GBM进行术前评估和FGS的价值。这种新型成像探针已证明了其在不损伤正常脑组织情况下可最大限度地安全切除难以接近的肿瘤的潜力。
研究目前存在随访时间不足、患者数量有限等不足,限制了该技术与临床结果有更明确的相关性。今后的工作将设计为随机临床试验,采用更严格的纳入标准,以评估此技术在改善患者生存方面的有效性。

田捷
中国科学院中自动化研究所研究员,博士生导师,中国自动化学会常务理事兼中国自动化学会模式识别与机器智能专业会员会主任,中国生物物理学会分子影像学专业委员会主任(首届)。主要从事医学影像分析与生物特征识别方向的研究与应用工作。

季楠
首都医科大学神经外科学教授、博士生导师;北京天坛医院神经外科主任医师;中国医师协会神经外科分会全国委员,副总干事;中国医促会神经外科分会全国委员,专业方向为颅内肿瘤的手术及综合治疗。

朱朝晖
北京协和医院核医学科主任医师、科研处副处长,北京协和医学院“协和学者”特聘教授、博士生导师。主要研究方向为核医学分子影像新探针、新技术的临床转化和创新应用。

陈小元
美国国立卫生研究院(NIH)生物医学影像及医学工程所(NIBIB)终身资深研究员,分子影像及纳米医学实验室主任。科研方向主要涉及体外诊断,体内成像,基因/药物的纳米载体,以及诊疗一体化。

李德岭
北京协和医学院八年制医学博士毕业,首都医科大学附属北京天坛医院神经外科副主任医师,北京市科技新星,北京市医院管理局首批“青苗计划”获得者。

张静静
医学博士。主要研究方向:新型正电子发射PET成像分子探针的临床转化研究、68Ga/177Lu等核素标记肿瘤特异性分子探针的转化及应用、肿瘤核素靶向诊疗一体化。

迟崇巍
博士,中国科学院自动化研究所,中国科学院分子影像重点实验室,副研究员。主要研究方向为分子影像手术导航成像方法,系统研发及生物医学应用等。

庄乾宇
北京协和医院骨科副主任医师、副教授、硕士生导师;国际脊柱侧凸研究学会(SRS)“委员;国际矫形与创伤外科学会(SICOT)中国部青年委员会副主任委员;中国医疗保健国际交流促进会脊柱侧凸研究分会委员;香港研究资助局(RGC)外审专家。
(本文图表来源于原文)
版权声明:
协和医学杂志倡导尊重和保护知识产权。欢迎转载、引用,但需取得本平台授权。如您对文章内容版权存疑,请发送邮件[email protected]
阅读原文啦~