医学潮头︱一勺烩:2018年ASCO结直肠癌领域的热点
一年一度备受瞩目的2018年ASCO年于6月1日至5日在美国芝加哥召开,来自世界各地的肿瘤学及相关专业的专家超过32000名参会,各类肿瘤的重要研究进展都会在会上公布。相比其他瘤种,结直肠癌领域是小年,仅有一项关于“腹腔热灌注”的研究入选LBA,但研究结果却未能优化当前的临床实践。结直肠癌的口头报告放在大会的最后一天上午,可以说是结直肠癌今年最重要的研究进展。
本文转载自“中山大学附属第六医院肿瘤内科”订阅号,
已经获得作者邓艳红教授的授权,特此声明!
1、直肠癌围手术期治疗 - 山重水复疑无路?
对于局部进展期直肠癌(II-III期)当前NCCN指南推荐的标准治疗是5-FU为基础的新辅助CRT,术后再行辅助化疗。但是,5-FU-CRT新辅助治疗模式虽然降低了局部复发率,但始终未能改善DFS和OS。无论是术前抑或术后放化疗,仍有30%的患者会出现远处转移,这也是导致治疗失败的主要原因。为了加强对远处转移的控制,目前已有六项大型RCT研究(ACCORD12,STAR-01, NSABP R-04, AIO-04, PETACC 6, FOWARC)在新辅助治疗期间引入奥沙利铂,探索是否能进一步提高DFS。
结直肠癌第一项口头报告是PETACC-6研究。研究设计是在卡培他滨为基础的CRT上引入奥沙利铂(50mg/m2,QW),同时在术后辅助化疗中也引入CapeOX方案,希望能在增加放疗敏感性的同时,加强远处转移的控制,改善DFS,主要研究终点是3年DFS。在2014年ASCO上已公布该研究的主要结果,共纳入1000多例II-III期直肠癌患者,结果显示引入每周小剂量的奥沙利铂并不能提高pCR 率(12% vs. 14%),也没有改善3年DFS (74.5% vs. 73.9%)。

今年ASCO会议上,更新了长期生存随访数据,仍然是阴性结果。对照组和试验组5年的局部复发率为8.7%vs. 6.0%,5年DFS分别为71.3% vs. 70.5%,7年的DFS为66.1% vs. 65.5%;5年的总生存OS分别为83.1% vs. 80.1%。在后续亚组分析中看到,临床分期II期和III期的患者,肿瘤下缘距肛缘位置高低等因素均未见到DFS和OS的改善。仅在非德国人群(两组各约180例)患者中看到5年DFS的改善,从67%提高到75.7% (HR, 0.65,p=0.033),但原因尚未能解释。可能与不同人种的肿瘤分子分型差异相关,包括DPD酶的表达水平不同。总体上,该研究结果是阴性的,引入奥沙利铂在直肠癌新辅助放化疗中和术后辅助化疗中未改善生存预后,但研究已在亚组中发现,不同人群的差异,而对于中国人群是否也有不同的疗效,第三项口头报告FOWARC研究似乎可以回答上述问题。
FOWARC研究是中山六院汪建平教授牵头的直肠癌新辅助治疗研究,纳入约500例患者,旨在探索FOLFOX联合放疗是否可进一步改善直肠癌患者生存预后,同时,探索单纯FOLFOX新辅助化疗是否可取代CRT。与其他奥沙利铂新辅助治疗的五大研究不同的是,该研究的采用的是mFOLFOX6方案同步放化疗,而既往研究是50-60mg/m2每周的奥沙利铂同步放疗。初步结果已在2015年ASCO入选口头报告,近期疗效显示,FOLFOX联合放疗显著提高了pCR率,而单纯FOLFOX新辅助化疗,肿瘤降期率与标准CRT相似。
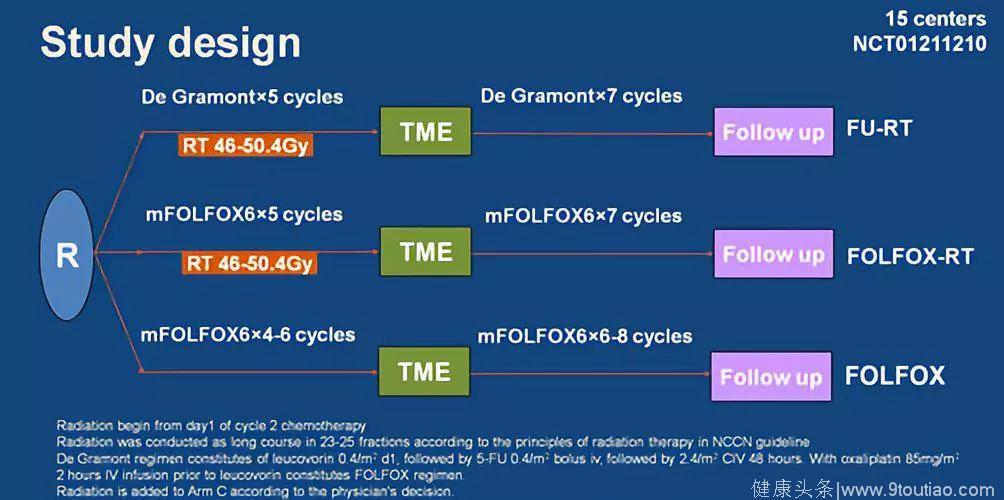
在今年的ASCO会议上,报告了该研究的主要研究终点3年DFS。结果显示,各组的3年局部复发率相似,均小于10%;而三组的3年DFS也相似,分别为75.7% vs. 77.1% vs. 74.9%,这与PETACC-6研究结果也相似。遗憾的是,FOLFOX联合放疗pCR率的提高并未转化成生存的获益,这有可能是由于pCR只代表局部的肿瘤退缩,完整的TME手术平衡了三组肿瘤退缩的差异。但我们也发现,在FOLFOX联合放疗组中,肝转移的发生率明显下降了。另外,在单纯FOLFOX化疗组中,3年的DFS也与其他两组相近,虽然没有做非劣效的设计,或许统计效能上不足以说明两者完全相等,但这给我们的启示是,在TME时代,对于部分选择性的直肠癌患者,放疗或许不是必要的,单纯化疗有可能可以取代当前的同步放化疗。期待正在进行的PROSPECT研究的结果会对这个问题有更好地补充。
但是,如果为了争取更高的pCR率,采取“Watch and wait”的治疗策略,那么FOLFOX联合放疗,或者全新辅助TNT的治疗策略,是首选的治疗模式。
事实上,ESMO最新指南以及我国的最新CSCO指南也将直肠癌的危险度作了分层,仅对一些危险度高的肿瘤,如MRF阳性,T4b,或侧方淋巴结阳性等建议放化疗;而对于中等或低等危险度的患者,则建议直接行TME手术。但由于远处转移是直肠癌治疗失败的主要原因,对于中等危险度的患者,相比直接手术,新辅助化疗或许会降低这一亚组患者转移风险。
ADORE研究是关于直肠癌新辅助治疗后,探索术后辅助治疗方案的研究。因为直肠癌的术后辅助治疗采用FOLFOX方案是参照结肠癌的研究外推而来,但是我们也看到,PETACC-6研究中,术后卡培他滨单药辅助治疗与CapeOX方案辅助治疗,生存预后无明显差异;在FOWARC研究中,标准CRT组采用Degramont方案辅助化疗,而FOLFOX-RT组采用FOLFOX方案辅助化疗,3年生存预后是相似的。因此ADORE研究探讨在5FU为基础的CRT后,术后分期仍为ypII-III期的直肠癌患者,奥沙利铂在术后辅助治疗中的地位。该研究的结果2014年已发表在Lancet oncology,总共纳入321例患者,总体研究结果是阳性的,直肠癌术后辅助治疗FOLFOX方案较5FU单药改善了直肠癌的3年DFS(71.6% vs.62.9%)和OS(85.7% vs. 95.0%)。
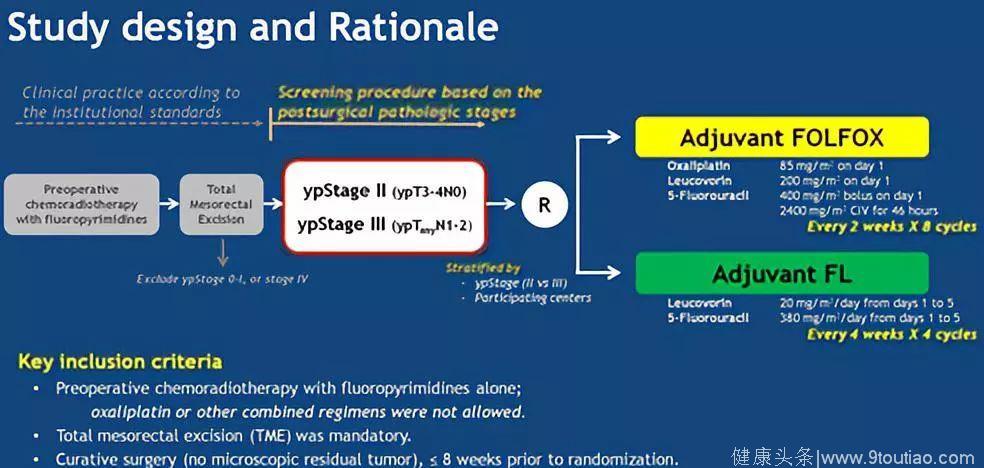
在本次大会上更新了6年的随访生存数据,两组6年的DFS分别为 68.2% vs. 56.8% (HR 0.63),提高了11.4%。进一步分析发现,DFS的获益主要是来自ypStage III期的患者(63.2% vs. 48.3%,p=0.01);ypStage II期患者中两组DFS分别为77.8% vs. 69.5%,虽然数值上提高了8%,差异无统计学意义,但需要说明的是,研究中ypStageII期患者两组中样本量较小,分别为58例和65例。对其他临床病理因素的分析发现,肿瘤分化差或差粘液腺癌,新辅助之后TRG分级较差,退缩不明显的患者更能从FOLFOX的辅助治疗中获益;另外,不存在脉管癌栓和神经束侵犯的患者能从FOLFOX辅助治疗中获益。前期报道3年的OS是获益的,但随访6年后,两组OS无明显差异(78.1% vs 76.4%);亚组分析发现,只有ypN2或者TRG分级较差的患者的OS从FOLFOX辅助化疗中获益。在ADORE研究中,我们同样发现FOLFOX组出现肝转移的比例较低(5.6% vs. 10.6%)。
值得我们思考的是,ADORE研究是一项II期研究,纳入特定的人群是新辅助之后降期不明显的ypStageII-III期患者,对于II期患者不能从FOLFOX辅助化疗中获益或者需要更大样本的研究验证,另外,对于新辅助治疗后达到病理完全缓解(pCR)的患者辅助化疗应该如何选择,是用FOLFOX还是5FU单,还是可以选择观察?另外,对于术后ypStage I期的患者,又应该如何选择化疗方案,这个研究都未能回答这个问题。
2、腹腔热灌注化疗 - 折戟沉沙?
Prodige-7是一项关于结直肠癌腹膜转移的研究,也是结直肠癌领域唯一的一项LBA,但最后公布的结果却差强人意。
腹膜转移是晚期结直肠癌不良预后因素,2017年AJCC第八版分期将结直肠癌腹膜转移单独列为IVC期,腹膜转移患者中位生存仅16个月。但是,对于部分腹膜转移患者,既往多项回顾性研究发现,通过细胞减瘤术(CRS)联合腹腔灌注化疗(HIPEC),可以延长患者的中位生存时间(32-41个月),既往研究腹腔热灌注采用的方案各异,有研究采用丝裂霉素±顺铂的方案或者奥沙利铂±伊立替康的方案,也有采用氟脲嘧啶热灌注的方案,但目前缺乏关于腹腔热灌注的前瞻性研究。
Prodige-7是第一项评估在CRS后HIPEC作用的III期研究。纳入结直肠癌单纯腹膜转移患者,限PCI评分≤25分,所有患者接受6个月围手术期系统化疗,减瘤手术达到R0/R1切除,或者R2切除(残留病灶大小≤1mm)。细胞减瘤术后再进行随机分组,一组接受腹腔热灌注化疗(术中灌注奥沙利铂460mg/m2,灌注时间30min或者术后灌注360mg/m2;同时静脉用5FU 400mg/m2联合亚叶酸钙);另一组仅进行系统化疗。主要的研究终点是OS,次要研究终点为RFS及安全性。
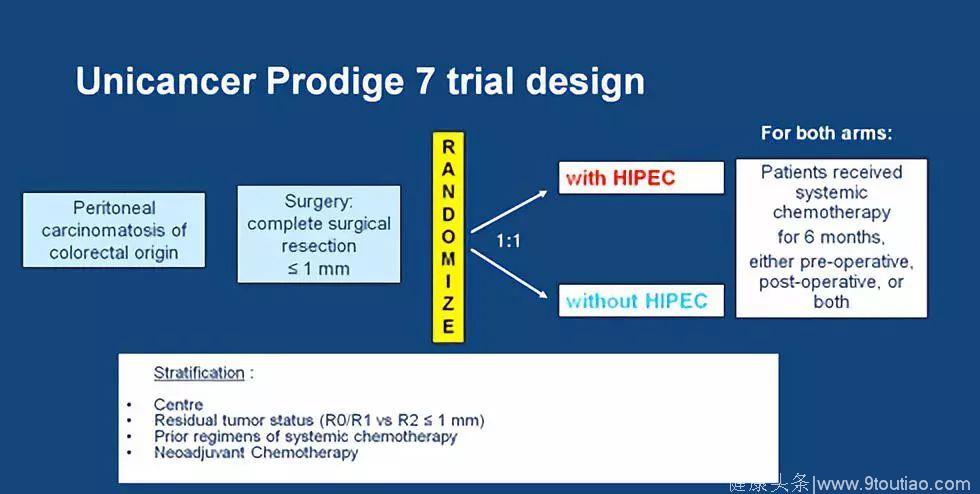
该研究纳入265名患者,同时性腹膜转移占40%,约60%的患者PCI评分小于11分,90%的患者减瘤术达到R0/R1。随访64个月后,两组OS是相近(41.7m vs. 41.2m),两组的RFS也无明显差异(13.1m vs. 11.1 m);而HIPEC组发生3-5级并发症发生率更高(24.1% vs 13.6%)。不同的PCI评分生存预后有显著的差异,这与既往研究结果相同;在亚组分析中发现,能从奥沙利铂的HIPEC治疗中获益的是PCI评分为11-15分的患者,但研究中这部分患者比例较低。
该研究是阴性结果,对于局限于腹膜转移的结直肠癌,在高质量的CRS手术后,全身系统的化疗或许更为重要,而在此基础上,HIPEC并未带来明显生存获益,反而增加了术后并发症的风险。但并不能因此完全否定HIPEC的作用,后续的研究需要进一步探索的是哪些患者需要行HIPEC以及采用哪种药物最为合适。
3、抗EGFR与抗VEGF - “殊途同归”
既往已有两项III期研究表明,两种靶向药物联合治疗未改善生存预后,而且增加了毒副作用。一项为2009年发表在NEJM上的CAIRO-2研究,CapeOX联合贝伐单抗对比CapeOX联合贝伐单抗+西妥昔单抗,结果表明,双靶联合PFS反而更短,而且生活质量受影响。另一项研究为2009年发表在JCO的PACCE研究,这里排除了卡培他滨的影响,比较FOLFOX或FOLFIRI方案联合贝伐单抗基础上,加减帕尼单抗的疗效,结果同样看到双靶联合治疗组PFS降低,而且副作用更明显,尤其在FOLFOX组PFS和OS的下降都达到了统计学差异。因此,指南也不推荐双靶(西妥昔单抗与贝伐单抗)联用。
大会的另一项口头报告E7208研究再次探索抗EGFR与抗VEGF的联合应用,不同的是选用了作用机制稍有不同的Ramucirumab(雷莫芦单抗),与安维汀无交叉耐药。这项II期研究探索的是KRAS野生型,一线FOLFOX联合贝伐珠单抗治疗进展后,二线伊立替康+西妥昔单抗(IC)对比伊立替康+西妥昔单抗联合雷莫芦单抗(mICR)的疗效,主要研究终点是PFS,次要研究终点是有效率及安全性。试验组下调了伊立替康剂量(150mg/m2),西妥昔单抗剂量(400mg/m2)以及雷莫芦单抗剂量(6mg/kg)。统计假设上预计对照组PFS 4.5个月提高到试验组7.65个月,α值定为0.15,检验效能90%。
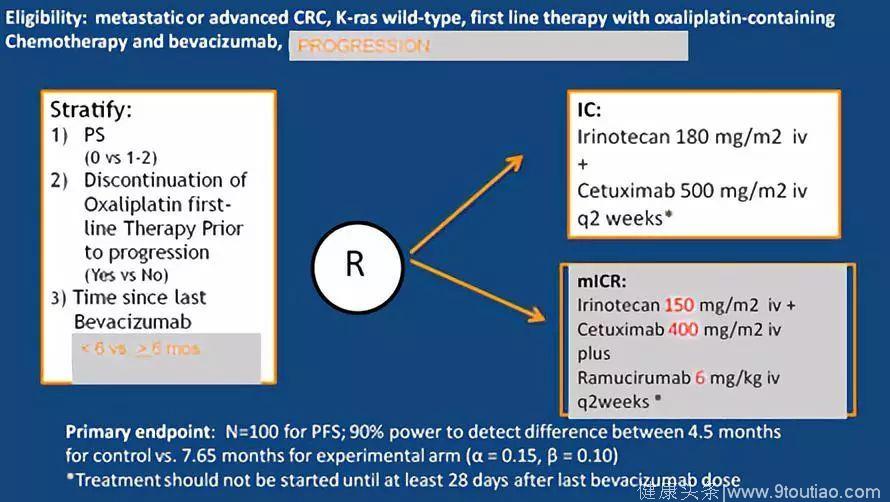
最终纳入分析的患者为97例,其中75%以上的患者在PD前停用奥沙利铂。虽然PFS达到了研究设计的终点(HR 0.65,单侧p=0.065<0.15),但两组中位PFS分别为5.7月和5.8个月;作为二线治疗,与RAISE研究、TML研究结果相似。根据分层因素分析,一线进展前已停用奥沙利铂的患者,PFS获益更为明显;另外,末次安维汀治疗时间是在6个月以前的亚组患者,PFS和OS获益更明显。
需要注意的是,研究入选的患者仅检测了KRAS状态,并非全RAS野生型,其次也没有对左右半肿瘤进行筛选。其次,如果生存无明显改善,这种联合的临床意义值得商榷。
另一项口头报告VALENTINO研究是探索抗EGFR药物维持治疗策略的非劣效研究。由于既往关于抗EGFR的III期临床研究的设计都是用药直至疾病进展或出现不可耐受的毒性,对于抗EGFR药物维持治疗目前尚无太多数据支持。而抗VEGF通路的贝伐珠单抗,经多个研究的验证,维持治疗、跨线治疗已成为标准。因此,抗EGFR单抗在探索抗VEGF同样的道路。
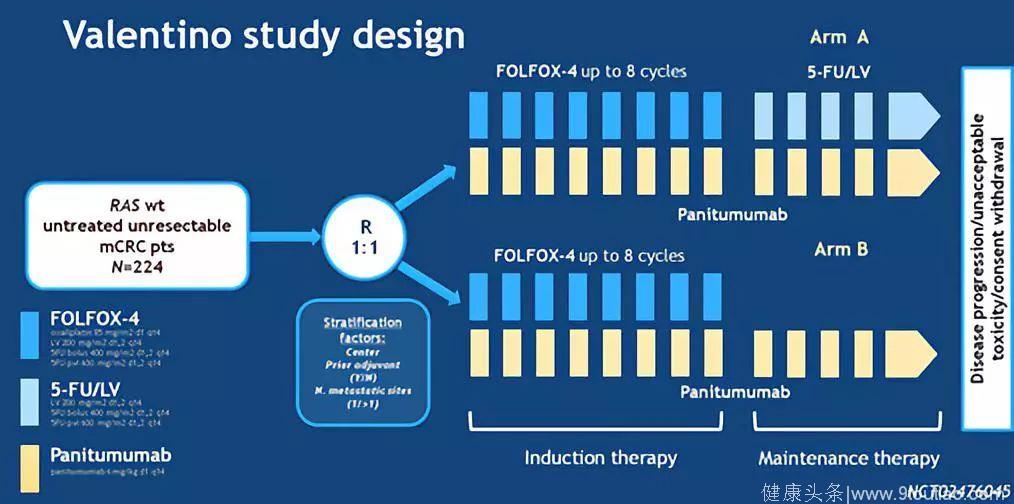
VALENTINO研究是探索在FOLFOX4联合帕尼单抗治疗4个月后,用单药帕尼单抗维持治疗是否非劣于5FU+帕尼单抗维持治疗。主要研究终点是10个月的PFS率,非劣效界值定为HR=1.515。该研究共纳入全RAS野生型转移性结直肠癌229例患者,入组时未限定左右半,但70%以上是左半结肠癌。结果表明,5FU+帕尼单抗维持治疗在PFS上优于帕尼单抗维持治疗,中位PFS分别为13.0m vs. 10.2m, HR=1.55 (95%CI,1.09-2.2),10个月PFS分别为62.8% vs. 52.8%,而且肿瘤持续应答时间更长。维持治疗期间,5FU+帕尼单抗组的3级皮疹发生率更高一些,但可耐受。
临床实践中,化疗联合抗EGFR单抗诱导治疗后,或许我们更多的是采用抗EGFR单药维持治疗,这项研究给了我们新的选择依据,5-FU联合帕尼单抗维持有更长的PFS。但帕尼单抗在我国未上市,这些数据是否可以直接推广到西妥昔单抗,值得探讨。另外,与抗VEGF维持治疗不同,抗EGFR单抗维持治疗,不可避免的问题是由于选择的压力,出现耐药克隆,血液ctDNA中可检测到RAS突变,抗EGFR治疗耐药或者疾病进展,因此,在使用抗EGFR单抗治疗中,ctDNA的监测也非常重要,当ctDNA检测转阴性时,后续治疗中可考虑EGFR单抗的再引入治疗。
责任编辑: