JCO来造势:cfDNA可预测三阴乳腺癌预后,液体活检又有重大突破!
液体活检真的很活,三阴乳腺癌预后也能搞定!
作者丨贾刚 东南大学 / 河南省人民医院
来源丨医学界肿瘤频道
前天,我们谈到Science爸爸刚发了一篇老厉害的文章(Science权威发布:癌症早诊特异度高达99%,液体活检强势来袭!),一时间,液体活检被推上人生巅峰,圈粉无数,赚足眼球!连界哥也忍不住想再次埋头苦学,触类旁通(蹭蹭热点)。
这不,听说液体活检又啃下了三阴乳腺癌(TNBC)这块大骨头,实属不易!界哥先跪为敬!
近日,来自哈佛大学和麻省理工学院研究所的研究者在JCO(Journal of Clinical Oncology)上发表了一项研究,研究表明,在转移性TNBC患者中,循环游离细胞 DNA( cfDNA)增加,并且特定的体细胞拷贝数改变(SCNAs),将预示着更差的生存率!
更为惊人的是,在64%的晚期TNBC患者血液中,检测出超过10%的肿瘤相关DNA,而这是预后不良的重要提示!
无怪乎TNBC普遍存活率较低了!
这是个大突破啊!快快快,我要看重点!
哈哈!不急不急,磨刀不误砍柴工,先来了解下三阴乳腺癌吧。
1
三阴乳腺癌,那叫一个头疼
那么三阴乳腺癌究竟是个什么鬼,吃人不眨眼?
三阴性乳腺癌(TNBC)是指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体(HER2)均阴性的一种特殊类型乳腺癌,目前约占乳腺癌总数的10-15%,但在乳腺癌相关死亡中却占到了三分之一。
痛点在于缺乏有效的治疗靶点。TNBC的内科治疗仍以化疗为主,晚期TNBC的治疗选择有限。多数患者接受蒽环类、紫杉类和环磷酰胺治疗,一旦复发转移,可选择的药物很少,患者的预后极差。
既往研究表明,原发性三阴性乳腺癌(pTNBC)细胞突变少,但伴随SCNAs产生的TP53基因缺失和基因组不稳定性发生频繁,提示SCNAs在TNBC的发生、发展和转移中可能发挥重要作用。
So what?迄今为止,由于缺乏有效的研究手段,并没有大量关于转移性三阴性乳腺癌(mTNBC)基因组学的研究,因而SCNAs在mTNBC中的作用依然停留在脑洞阶段,雾里看花,像雾像雨又像风~

所以说液体活检是个重大进步。它能够分析体液所携带的肿瘤信息,可以实现肿瘤的早期诊断,检测物有常用的循环肿瘤细胞(CTC)、循环肿瘤DNA(ctDNA)、循环游离细胞DNA(cfDNA)等。
目前mTNBC缺乏预后标志物,通过抽血这一无创方法获得的可靠标志物,无疑对于患者的管理具有重要意义。
与采用靶向体细胞突变检测相比,采用SCNAs检测估计cfDNA的肿瘤分数代表了一种颇具吸引力的替代选择。
这里,我们暂停一下,对,今天的主角就是cfDNA!
2
cfDNA:山路十八弯,终于到我上场!
cfDNA作为新人,可能大家还不太熟悉。甚至有的人脸盲,认成ctDNA了。所以,为了避免尴尬,我们先介绍下,什么是ctDNA。
ctDNA就是循环肿瘤DNA(Circulating tumor DNA),是原发肿瘤甚至是转移形成的新肿瘤上的细胞破裂掉落下来的DNA片段,进入了外周血循环系统。
而cfDNA,即循环游离细胞 DNA( circulating cell-free DNA) ,指的是体循环中所有细胞的游离DNA,包括循环中来源于肿瘤细胞和其他所有体细胞的DNA片段总和。
虽然缺乏肿瘤细胞特异性,但是cfDNA却能够提供相对全面的基因组信息,这或许能够帮助我们通过微创的方式来实现对肿瘤细胞的基因组图谱分析。
JCO的这项回顾性临床研究就分析了cfDNA在mTNBC中的价值。
该研究纳入了164个经组织活检病理证实为mTNBC的患者,采用低覆盖率基因组测序的方法对患者血液中SCNAs 及cfDNA肿瘤分数(即cfDNA中肿瘤细胞来源的比例,TFx)进行测量,在此基础上分析了TFx和患者生存的关系、识别出了mTNBC患者中主要的SCNAs,并分析了其与预后的关系。
通过对比mTNBC和pTNBC的基因组发现,二者在体细胞突变拷贝数和基因组改变比例方面非常接近,差别在于:
在mTNBC中,某些特定的SCNAs,像NOTCH2、AKT2和AKT3,更常见。
研究发现,10%的TFx似乎是一个分界点,TFx≥10%的患者预后明显更差。
随后,研究者进一步揭示了两种具有独立预后因素作用的染色体突变位点:18q11和19p13。
cfDNA竟然有这么大的作用,真嘞假嘞?
不吹牛,往下看。
首先,研究者比较了mTNBC中,转移灶组织活检标本和cfDNA中,体细胞拷贝数及突变的一致性。
结果显示,在转移灶活检标本中改变的DNA片段在cfDNA中同样可以检测到,而且具有较高的灵敏性和特异性(灵敏度0.92,特异度0.90)。
然而,cfDNA中的一些独特突变则很难在组织活检标本中检测到,提示cfDNA比组织活检标本包含了更全的基因组信息。
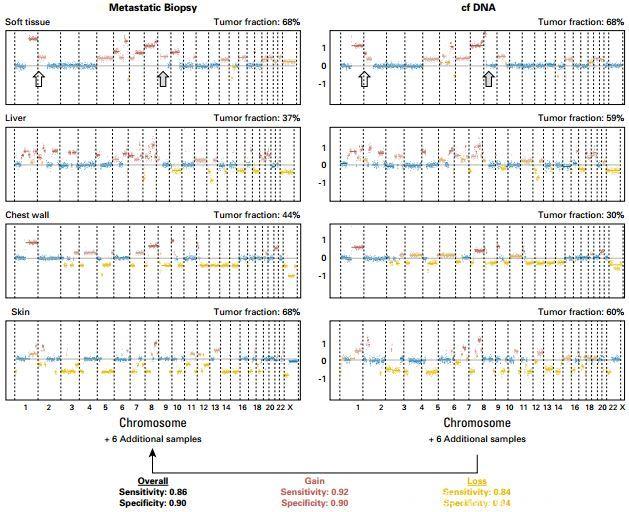
图1.TNBC转移灶活检标本和cfDNA中不同染色体的基因拷贝数对比
看来cfDNA很优秀嘛!
有戏,接着看。
临床上,一个常见的现象是,随着时间的推移和治疗的介入,一些类型的肿瘤开始变得越来越具有侵袭性。人们并不完全清楚其中的原因,但大量的研究提示一个可能的机制:拥有基因组不稳定性的pTNBC,在治疗之后发生转移的病灶中会发生大量的基因组学的改变。
然而,pTNBC并不按常规套路出牌。
研究对比100多例mTNBC和400多例pTNBC的cfDNA,并没有发现二者基因组改变的百分比有明显的差别,并且发现有改变的染色体类型也十分相似。
这说明大部分的染色体改变发生在肿瘤发生的早期,而不是发生在转移灶形成的过程中,也就是说,在肿瘤刚刚形成的时候,这种蕴藏在cfDNA中的潜在的转移能力(基因组不稳定性)已经“与生俱来”了!

图2 原发三阴性乳腺癌癌灶和转移三阴性乳腺癌cfDNA中基因拷贝数的变化
虽然,pTNBC和mTNBC之间缺乏大范围的SCNA改变,研究者还是发现在mTNBC染色体中存在一些特定的基因位点变化:
这些变化在常见的(1q,7q,8q)和不常见的(11q,18q,19p)基因改变区域都有发生,进而识别了一些在mTNBC中呈明显高表达的基因。
其中GATA3, NOTCH2, AKT2和AKT3四个基因无论在配对样本还是在整个队列中都明显扩增,而这种差别在全基因组范围内则并不显著。
由于这些SCNAs对化疗的耐药和远处转移具有重要影响,研究者推测,这些基因改变在化疗耐药的mTNBC中要比在化疗敏感的mTNBC中发生更频繁!

图3 pTNBC原发灶和mTNBC的cfDNA中25个肿瘤相关基因的的表达变化
一直以来,对于和mTNBC生存期相关的基因组决定簇人们知之甚少,该研究通过计算每一个基因对mTNBC患者生存期影响的相对风险比,发现了两个全新的生存相关染色体改变:
18q11和19p13,并且确认二者的产生和扩增是mTNBC生存期的独立预后因素(独立于临床病理因素和TFx)。
带有这种基因改变的TNBC亚型,无论是原发性疾病还是转移性疾病都会快速进展,并导致生存期缩短。
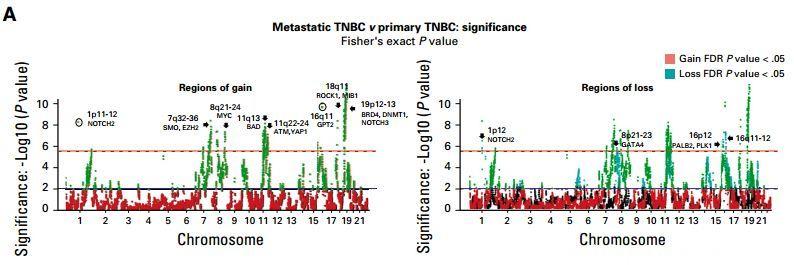
图4 pTNBC和mTNBC中染色体的获得和丢失
3
以上看不懂?这是一个简版Review
看完全文,有没有种不明觉厉的赶脚?
不骗你,界哥膝盖都跪青了。
这么厉害,一点不输Science!
连澳大利亚墨尔本大学、彼得麦卡勒姆癌症中心的肿瘤专家都隔空喊话,发表同期述评称赞,cfDNA有望指导转移性三阴性乳腺癌预后!
所以你真的看懂了吗?
不怕,界哥最后再来梳理下:
- 相比转移灶组织活检,cfDNA检测包含了更全的基因组信息。
- 在cfDNA中,肿瘤相关DNA超过10%,即TFx≥10%的患者预后明显更差。
- 在原发性三阴乳腺癌形成时,蕴藏在cfDNA中的潜在转移能力已经形成,即染色体改变已经发生,并非在转移之后,才发生基因组学的改变。
- 转移性乳腺癌中,GATA3, NOTCH2, AKT2和AKT3四个基因扩增显著,可能与转移性乳腺癌的化疗耐药形成高度相关。
- 18q11和19p13的产生和扩增是mTNBC生存期的独立预后因素。带有这两种基因改变的TNBC亚型,无论是原发性疾病还是转移性疾病都会快速进展,并导致生存期缩短。
总的来说,这项研究证实,通过检测血液中cfDNA得到的TFx能够提供一种独立于临床病理因素的重要预后信息。
cfDNA液体活检的来袭,将有助于识别转移性疾病的独特基因组特征,帮助发现更有临床价值的生物标志物,同时也能加深我们对转移、耐药以及全新治疗靶点的理解。
这是一项全新的技术,借由最近的这两篇大牛研究,我们似乎看到液体活检正跨着骏马,朝我们挥鞭而来。
我想起了那句经典台词:我的意中人是个盖世英雄,有一天他会踩着七色云彩从死神手里抢下我。
界哥嘚啵嘚
那个人看起来,好像一条……不对不对,串戏了……
(本文为医学界肿瘤频道原创文章,转载需经授权并标明作者和来源。)