首款可自动给药连续血糖监测系统获 FDA 批准
美国 FDA 近日批准了 Dexcom G6 集成连续血糖监测(CGM)系统的营销授权。Dexcom G6 CGM 系统是 2 岁及以上糖尿病患者的最新一代 CGM 系统。FDA 认为 Dexcom G6 既可用作独立 CGM,也可用于自动胰岛素给药(AID)系统。这款新型 Dexcom G6 是首个获得 FDA 此项分类的 CGM。
近 10% 的美国人患有糖尿病,它会损害机体制造或正确调节胰岛素的能力。糖尿病患者必须定期监测他们的血糖水平,因为持续的高血糖会导致心脏病,中风,失明,肾衰竭和神经损伤,导致脚趾,脚或腿的截肢。血糖水平也可能会降至太低,导致头晕,困惑,意识不清,并在极端情况下导致死亡。
Dexcom G6 是一种硬币大小的贴片装置,应用于腹部皮肤。它包含一个小型传感器,可持续测量体液中的葡萄糖水平。该设备每五分钟将实时葡萄糖读数传输到兼容的显示设备,如手机的医疗应用程序上,并且在患者血糖进入过高或过低的危险水平时触发警报。如果它与自动胰岛素给药系统结合,在血糖升高时可以触发胰岛素从泵中自动释放出来。
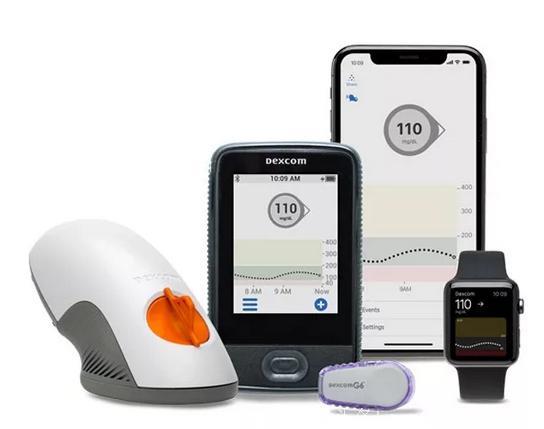
图片来源:Dexcom 官方网站
FDA 评估了两项关于 Dexcom G6 临床研究的数据,其中包括 324 名患有糖尿病的成人和 2 岁儿童患者。这两项研究均包括 10 天内的多次临床访视,与实验室血糖值测量方法比较了这款设备的读数。研究期间未发生严重不良事件报告。
FDA 通过 de novo 审查途径审查了该设备的数据。这种途径适用于与合法销售设备有显著区别的新颖,低至中等风险产品。随着这一授权,FDA 正在制定特殊控制标准,确保集成 CGM 系统的准确性,可靠性和确认临床相关要求,以及 CGM 设备所需的研究和数据类型。这些特殊控制与一般控制一起,为设备的安全性和有效性提供了保证。
“作为一款工厂校准的实时 CGM 系统,Dexcom G6 具有出色的准确性,对于糖尿病患者而言是一场变革,他们不再需要刺痛手指进行糖尿病管理,”休斯敦得克萨斯儿童医院的内分泌学家 Daniel DeSalvo 博士说:“我可以以一名 1 型糖尿病患者的身份告诉你,Dexcom G6 作为一款 CGM 设备的所有功能和优点,它是过去二十年来我一直期待的设备。这个 CGM 系统将有助于减轻糖尿病管理的负担,同时改善糖尿病患者的生活。”
“我们密切关注糖尿病患者并不断寻找方法让他们更好的管理病情,FDA 的特殊控制措施为我们的行业制定了严格的新标准,明确了其他 CGM 系统获得批准的过程。” Dexcom 首席执行官 Kevin Sayer 先生说:“我们相信新的 Dexcom G6 设备是 Dexcom 和这个行业迈出的重要一步。”
该公司预计今年晚些时候会推出这款产品。我们期待这款产品可以为广大糖尿病患者更方便的控制血糖,改善病情。
参考资料:
[1] FDA Authorizes Marketing of the New Dexcom G6 CGM Eliminating the Need for Fingerstick Blood Testing for People with Diabetes
[2] FDA authorizes first fully interoperable continuous glucose monitoring system, streamlines review pathway for similar devices