30年来首个新机制抗抑郁药——FDA批准强生争议性抗抑郁新药
美国医药公司强生(JNJ)旗下Janssen 制药3月5日宣布,美国食品和药物管理局(FDA)已批准Spravato(esketamine)CIII鼻喷雾剂,联合口服抗抑郁药,用于难治性抑郁症(TRD)成人患者的治疗。后续可能会有一系列市场期待已久的相关新药获批。
30年来首个具有新作用机制的抗抑郁药
此次批准,使Spravato成为过去30多年来首个具有新作用机制的抗抑郁药物。在美国,FDA之前已授予Spravato治疗TRD和治疗伴有紧迫自杀风险的严重抑郁症突破性药物资格。与标准的口服治疗药物相比,Spravato通过鼻腔内给药的方式可提供快速起效的优势。需要指出的是,Spravato药物标签中附带有一则黑框警告,提示风险评估和减灾战略(REMS)以及在儿科患者和年轻成人中自杀想法和行为的风险。
Spravato的活性药物成分为esketamine,这是一种非竞争性和亚型非选择性活动依赖性N-甲基-D天冬氨酸(NMDA)受体拮抗剂,具有一种全新的独特作用机制,其作用原理与目前市面上的其他治疗抑郁症的药物不同。NMDA受体是离子型谷氨酸受体的一个亚型,在神经突触可塑性和神经元之间的信息交流方面具有关键性的作用。在抑郁症中,据认为阻断NMDA受体能改善大脑的可塑性、增强突触连接。
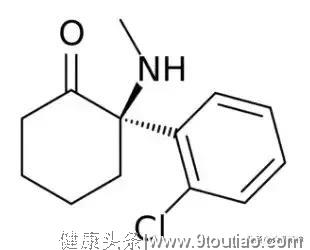
esketamine分子结构式
Spravato与氯胺酮化学成分接近。氯胺酮是一种麻醉药,以其对大脑的快速作用而知名,常常在派对上被滥用。研究显示,氯胺酮可以在数小时内缓解抑郁症状,而传统的抗抑郁药需要数周才能开始见效。
Spravato的惊人之处在于该药在难治性抑郁症患者群体中表现出的速效、持久的强大疗效。数据显示,对市面上大多数抗抑郁药难治的抑郁症患者,当转向Spravato治疗时,仅仅用药几天内,患者的情绪就出现了不可思议的明显改善,同时疗效持续的时间非常长。而目前市面上大多数抗抑郁药往往需要服用数周甚至数月才能起效。
Janssen 制药于2018年9月4日宣布向FDA提交了一份NDA,申请批准Spravato用于重度抑郁症(MDD)成人患者的治疗。咨询委员会支持批准Spravato鼻腔喷雾剂,是基于在难治性抑郁症成人患者中开展的5项III期临床研究的安全性和疗效数据,包括:3项短期研究、一项维持效果研究、一项长期安全性研究。此外,Spravato研究项目还提供了3项II期研究和19项I期研究的支持性数据,这些研究在难治性抑郁症患者和健康志愿者中开展。来自一项短期III期研究和一项长期III期研究的数据均表明,Spravato鼻腔喷雾剂联合一种新启动的口服抗抑郁药在该难治性群体中使抑郁症状实现了统计学显著的、临床意义的、快速的和持续的改善。所有入组III期研究的患者,在治疗期开始时,除了接受一种新启动的口服抗抑郁药外,还接受了Spravato或安慰剂。
长期安全性研究表明,Spravato总体上是可耐受的,与短期(4周)研究的数据相比,治疗长达52周期间没有出现新的安全信号。因Spravato相关不良事件导致的停药率较低,通常发生在第一周。大部分治疗期间发生的不良事件,包括离解症状、头晕/眩晕、血压升高和镇静,发生在给药后不久,而患者在保健专业人员的监督下,这些不良事件是短暂的,并在同一天得到解决。
除了全面的临床研究计划,该公司还提出了一个稳健的风险评估和缓解策略(REMS)。一旦Spravato被确定为合适的治疗方案,根据REMS,患者将在经认证的治疗中心接受治疗。Spravato不会直接处方给患者在家使用,该药将由患者在医疗保健提供者的直接观察下进行自我服药,并观察镇静、解离和血压变化至少2个小时,直到患者被确认安全后方可离开。此外,患者在得到良好的睡眠后,直到第二天才能驾驶或操作重型机械。所有患者都将登记在Spravato REMS注册中心,以进一步描述镇静、解离、滥用和误用造成严重不良后果的风险,并支持安全地使用该药物。
随机临床试验:Spravato鼻腔喷雾剂辅助口服抗抑郁药治疗耐药性抑郁症的疗效和安全性。
大约三分之一患有严重抑郁症(MDD)的患者对可用的抗抑郁药没有反应。该研究旨在评估Spravato鼻腔喷雾剂治疗难治性抑郁症(TRD)患者的疗效,安全性和剂量反应。
设计与方法
研究于2014年1月28日至2015年9月25日在多家门诊转诊中心进行了二期双盲、双随机、延迟启动、安慰剂对照研究。研究包括4个阶段:(1)筛查, (2)双盲治疗(第1-15天),(3)选择性开放标签治疗(第15-74天),(4)治疗后随访(8周)。筛选了诊断为MDD和对2种或更多抗抑郁药(即TRD)反应不足的126名成人,67人随机化,60人完成了两个双盲期。意向治疗分析用于评估结果。
干预措施
在第1阶段,参与者被随机分配(3:1:1:1)至安慰剂(n=33),esketamine 28mg(n=11),56mg(n=11)或84mg(n=12),每周两次。在第2阶段,28名安慰剂治疗的中度至重度症状的受试者被重新随机化(1:1:1:1)至4个治疗组中的1个;那些症状轻微的人继续服用安慰剂。参与者在研究期间继续他们现有的抗抑郁药物治疗。在开放标签阶段,给药频率从每周两次减少到每周一次,然后减少到每两周一次。
主要疗效终点是蒙哥马利-Asberg抑郁评定量表(MADRS)总分从基线到第8天的变化。
结果
67名参与者(38名女性,平均[SD]年龄,44.7[10.0]岁)被纳入疗效和安全性分析。所有3个esketamine组的MADRS总分的变化均优于安慰剂(esketamine28 mg:-4.2 [2.09],P=.02; 56mg:-6.3 [2.07],P=.001; 84mg:-9.0 [2.13],P<.001),剂量-反应具有显著的递增关系(P<.001)。尽管开放标签阶段的给药频率降低,但抑郁症状的改善是持续的(-7.2 [1.84])。在开放标签期间,因不良事件而中止研究的有4例(晕厥、头痛、解离综合征和异位妊娠各1例)。
结论和相关性
在迄今为止首次鼻内esketamine治疗TRD的临床研究中,抗抑郁作用在疗效和剂量相关方面都是迅速的。反应持续超过2个月,且给药频率较低。结果支持在更大的试验中进行进一步的研究。