规培课堂(六十九)——肝癌外科治疗规范
主讲:刘宏 整理:高晓红 审核:刘宏
2018年8月8日,我院普外科刘宏老师为全体规培学员进行了题目为《肝癌外科治疗规范》的专题讲座。
刘老师从背景知识,定义,原发性肝癌筛查、诊断,分期和治疗四个方面为大家做了详细的讲解。
原发性肝癌是目前我国第四位的常见恶性肿瘤及第三位的肿瘤致死病因,严重威胁我国人民的生命和健康。原发性肝癌主要包括肝细胞癌(Hepatocellular carcinoma ,HCC)、肝内胆管癌(Intrahepatic cholangiocarcinoma, ICC )和HCC-ICC混合型三种不同类型,三者在发病机制、生物学行为、组织学形态、治疗方法和预后等方面差异较大,其中HCC占到85%-90%以上。
1.背景:
1888年,Langenbuch有目的地成功施行了第一例肝切除术。21世纪是肝脏外科的“世纪”;20世纪50年代初期开始:分清了肝脏内部的管道系统;20世纪70年代成长:AFP的发现提高了肝癌的早诊率。阐明临床型肝癌和亚临床型肝癌, 提出“早诊断、早治疗”的观念,小肝癌的手术治疗取得了辉煌成就。20世纪90年代成熟:微创外科技术, 丰富了外科的内涵,适应证把握和安全性得到了进一步保障。通过三个阶段的发展,我国肝癌的治疗水平已居于世界前列。
2.原发性肝癌筛查和诊断:
①基本原则:高危人群包括乙型肝炎病毒和/或丙型肝炎病毒感染、长期酗酒、非酒精脂肪性肝炎、食用被黄曲霉素污染食物、各种原因引起的肝硬化、有肝癌家族史,尤其史年龄40岁以上的男性风险更大。
②主要手段:筛查周期为每隔6个月至少一次检查。主要有影像学检查:超声检查 X线计算机断层成像 核磁共振成像 数字减影血管成像 核医学影像检查 PET/CT、 SPECT/CT 。血清学分子标记物: AFP、AFP异质体、岩藻苷酶。病理学诊断。
B超:
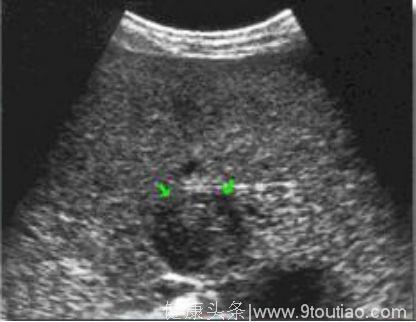
可显示肿瘤的大小,形态,所在部位以及肝静脉或门静脉内有无癌栓等,其诊断符合率可达84%,能发现直径2厘米或更小的病变,是目前较好有定位价值的非侵入性检查方法。
CT:
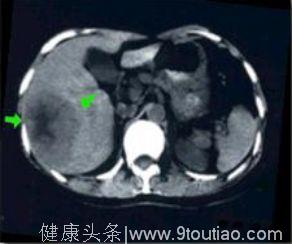
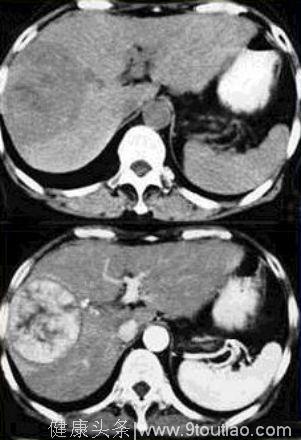
CT分辨率高,可检出直径约1厘米左右的早期肝癌,应用增强扫描有助与血管瘤鉴别。对于肝癌的诊断符合率高达90%。
血管造影:
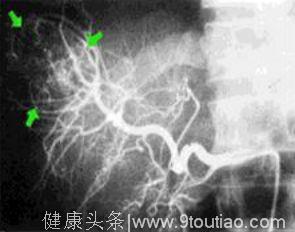
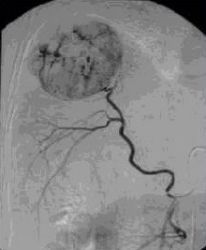
血管造影:对血管丰富的癌肿,有时可显示直径为0.5~1厘米的占位病变,其诊断正确率高达90%。可确定病变的部位、大小和分布,特别是对小肝癌的定位诊断是目前各种检查方法中最优者。
MRI:


核磁共振成象:诊断价值与CT相仿,可获得横断面、冠状面和矢状面图象,对良、恶性肝占位病变,特别是与肝血管瘤的鉴别优于CT,且无需增强即可显示肝静脉和门静脉。
③诊断路线:
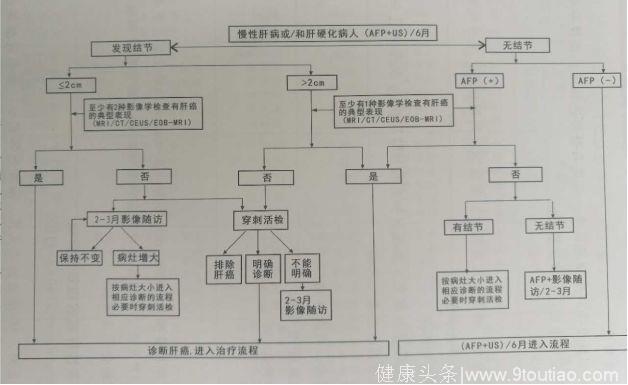
3.原发性肝癌分期和治疗:
原发性肝癌分期:BCLC、TNM、JSH、APASL、中国临床分期多种分期,具体如下:
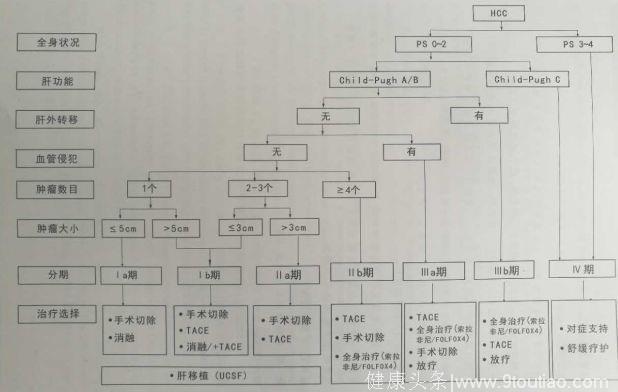
①原发性肝癌治疗包括:1.肝切除术:基本原则、肝功能储备的评估、根治性切除标准、手术切除技术、术前治疗、防止术后转移复发。2.肝移植术:选择标准、术后复发的预防、肝移植和肝切除的选择。
②基本原则:彻底性:完整切除肿瘤、切缘无残留肿瘤;安全性:最大限度地保留正常肝组织,保留由足够功能肝组织以术后肝功能代偿,降低手术死亡率及并发症。
③肝功能储备的评估:采用美国东部肿瘤协作组提出的功能状态评分(ECOG PS)来评估病人的全身情况:Child-Pugh 分级;肝储备功能(如ICGR15清除试验);肝脏硬度测定:;剩余肝体积的计算。
满足以下条件者可考虑手术治疗:Child-Pugh* A级,HVPG**<12mmHg,ICG15*<20%-30%,余肝体积须占标准肝体积的40%以上。
根治性切除标准:
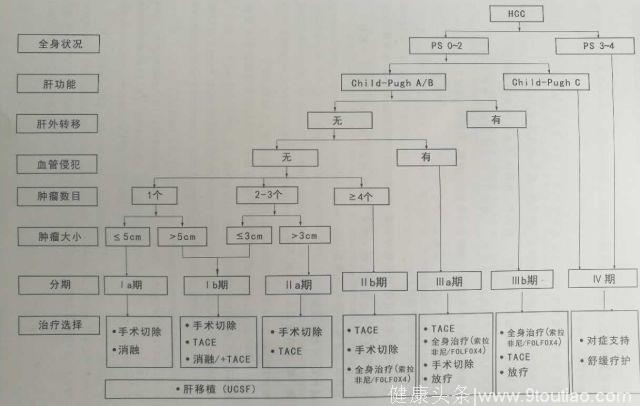
1.术中判断标准:
肝静脉、门静脉、胆管以及下腔静脉未见肉眼癌栓;无邻近脏器侵犯、无肝门淋巴结或远处转移;肝脏切缘距肿瘤边界大于1cm,如小于1cm,但病理无肿瘤细胞残留,即为切缘阴性。
2.术后判断标准:
术后2个月检查未见肿瘤病灶;AFP降至正常。
腹腔镜肝癌切除的指针:①病变位于Couinaud Ⅱ、Ⅲ、Ⅳb,Ⅴ,Ⅵ段;②病变大小以不影响第一和第二肝门的解剖为准,一般不超过10cm;③有丰富经验的一是可逐步开展腹腔镜半肝切除、肝3叶切除和CouinaudⅠ、Ⅶ、Ⅷ段肝切除。提高肝肿瘤可切除性的手段有:①术前TACE可使部分病人的肿瘤缩小后再切出;②经门静脉栓塞主瘤所在肝叶,使余肝代偿性增大后再切除;③联合肝脏分隔和门静脉结扎的二步切除术ALPPS;④对于开腹后探察发现肝硬化较重、肿瘤位置深在、多结节的肿瘤,可采用手术切除结合术中消融(如术中射频等)降低手术风险。
肝移植的选择标准——米兰标准
最早由Bismuth提出,1996年经意大利Milan的Mazzaferro总结并得到公认。具体标准为:单个肿瘤直径≤5cm;多发肿瘤数目≤3个、最大直径≤3cm。不伴有血管及淋巴结的侵犯。1998年,美国器官分配网(UNOS)开始采用Milan标准(加MELD/PELD评分,又称UNOS标准)作为筛选肝癌肝移植受体的主要依据,Milan标准逐渐成为世界上应用最广泛的肝癌肝移植筛选标准。
米兰标准的优点:疗效肯定, 5年生存率在75%以上,复发率小于10%;仅需考虑肿瘤的大小和数量,便于临床操作。
米兰标准的缺点:Milan标准过于严格,候肝期间肿瘤生长超出标准而被剔除;符合Milan标准的小肝癌行肝移植与肝切除相比,总体生存率无明显差异,只是前者的无瘤生存率明显高于后者。Milan标准很难适用于活体供肝肝移植以及中、晚期肝癌降期后进行肝移植受体的筛选。
肝移植的选择标准——UCSF标准
加州大学旧金山分校(UCSF)标准,2001年由美国Yao等提出,在米兰标准的基础上进行了一定程度的扩大,包括:单个肿瘤直径≤ 6.5cm;肿瘤数目≤3个、最大直径≤4.5cm、总的肿瘤直径≤8cm;不伴有血管及淋巴结的侵犯。UCSF标准同样扩大了Milan标准,但又不明显降低术后生存率; 近年来,支持应用UCSF标准的文献逐渐增多。
肝移植的选择标准——Pittsburgh标准
匹兹堡(Pittsburgh)改良TNM标准,2000年美国Marsh等提出,只将有大血管侵犯、淋巴结受累或远处转移这三者中出现任一项作为肝移植禁忌证,显著扩大了肝癌肝移植的适用范围。
匹兹堡标准的缺陷:
术前很难对微血管或肝段分支血管侵犯情况做出准确评估,许多有肝炎背景的肝癌患者,其肝门等处的淋巴结肿大可能是炎性的,需要行术中冰冻切片才能明确诊断。虽扩大了的肝癌肝移植指征可使一些中晚期肝癌患者可能由此受益,但其总体生存率却显著降低,减少了良性肝病患者获得供肝的机会。
肝移植的选择标准——国内标准
国内标准对于无大血管侵犯、淋巴结转移及肝外转移的要求比较一致,但是对于肿瘤的大小和数目的要求不尽相同。国内标准扩大了肝癌肝移植的适应证范围,并未明显降低术后累积生存率和无瘤生存率,可能更为符合我国国情和患者的实际情况。但是各自为政,有待于规范的多中心协作研究以支持和证明,从而获得高级别的循证医学证据,达到公认和统一。
肝移植术后复发的预防:
肿瘤的生物学行为是决定患者预后最主要的因素。目前认为,肝移植术后可以进行适当的药物治疗(包括抗病毒治疗以及化疗等),有可能会减少和推迟肝癌复发、改善生存,但是需要进一步研究以获得充分的循证医学证据。
总之,原发性肝癌的诊断应结合患者的肝病背景、发病年龄、临床表现、AFP等肝癌标志物的检测以及合理的影像学检查,全面分析,综合判断,尽快作出定性和定位诊断,以及指导治疗。刘老师在对肝癌诊疗的实践经验和临床研究进行详细讲解后,我们收获颇多,感触颇深,在获得知识的同时,也认识到自己的知识匮乏,今后我们要把握更多的学习机会,不断提升自己,贡献微薄之力。