ADA指南更新!糖尿病肾病诊治7大重点!| 探“泌”指南

开始划重点!

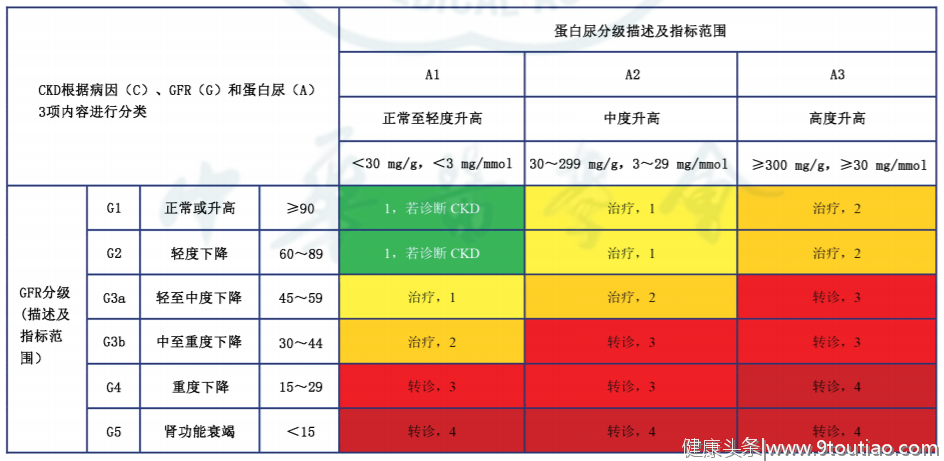
2020年指南新增推荐:在没有容量不足的情况下,不要因血清肌酐轻度增加(<30%)而停止肾素血管紧张素系统 阻断剂的使用(证据级别B)[1]。急性肾损伤(AKI)一般依靠血清肌酐在短期内持续升高50%或以上进行诊断,其反映了eGFR的快速降低[9]。糖尿病患者AKI的风险高于非糖尿病患者[10]。
参考文献:
李全民:火箭军总医院内分泌科主任,主任医师,医学博士(内分泌与代谢病专业)。研究方向为糖尿病发病机制及慢性并发症诊治研究,尤其擅长糖尿病肾病、糖尿病神经病变等的研究和治疗。
原创声明
本文原创,转载需联系授权
-End-