横跨十几种实体瘤,抗癌新药进入中国,儿童患者受益明显
全球第一款广谱靶向药拉罗替尼(Larotrectinib)自获批上市以来就受到全世界癌友圈的极大关注,前期研究显示,该药对肺癌、乳腺癌、头颈部鳞状细胞癌等17种实体瘤都有明显效果,并且,对儿童纤维肉瘤患者的有效率甚至高达93%。因此,癌友圈把这种药物称为抗癌“神药”。
拉罗替尼(Larotrectinib)是靶向NTRK融合基因的靶向药,NTRK基因融合突变非常罕见,在中国常见的肺癌、乳腺癌、结直肠癌中,只有1%~5%的患者存在这种突变,但所有存在NTRK融合突变的患者对靶向药都非常敏感,因此,这一突变也被称为“钻石”靶点基因。很多晚期患者都是因为NTRK基因适用的靶向药而获得重生的机会。
纤维肉瘤是一种儿童常见的恶性肿瘤,通常是先天性或出生后两年内发生。早期发现及时手术切除可有机会治愈,并且这种肿瘤对于化疗也是敏感的。然而,一旦复发,治疗手段非常有限,因此被称为儿童杀手之一。
M就是一个不幸的孩子,他刚出生时就被诊断患有先天性婴儿纤维肉瘤,因为肿瘤过大,他在出生的第4天就接受了手术切除。不幸的是,这种肿瘤的恶性程度实在是太高了,在2个月内,就出现了广泛的淋巴结复发,两个周期的化疗完全阻止不了癌症在体内的蔓延,MRI显示双侧颈部和腋窝淋巴结以及口底都有巨大的肿块,肿瘤的生长速度甚至超过了M身体的生长速度,最大的肿瘤已经长到了鸡蛋那么大。他的父母甚至做好了最坏的打算,不忍再看着他刚出生就承受成人都无法忍受的痛苦。
幸运的是,M的医生为他进行了全基因组测序,显示他存在ETV6-NTRK3融合突变。当时在开展一项针对NTRK融合的新药临床试验,就是大名鼎鼎的拉罗替尼(Larotrectinib,LOXO-101)。
M在3.5个月的时候开始每天两次接受LOXO-101的治疗,剂量为20 mg / kg。令大家都没有想到的是,仅经过4天的治疗,他的父母就发现,脖子上的肿块明显变小了,并且摸起来柔软了很多。在接下来的几周中,M的肿瘤迅速消退。在治疗的第56天,第一次的MRI显示目标病变已缩小至1.2×1.2×0.8 cm(约0.6 cm 3),临床评估为完全响应。在第112天的第二次MRI结果显示,淋巴结完全正常。在接受LOXO-101治疗16个月后的最后一次随访中,M已处于完全缓解状态,体内已检测不出任何病灶,并且在治疗过程中没有出现任何严重的毒副作用。
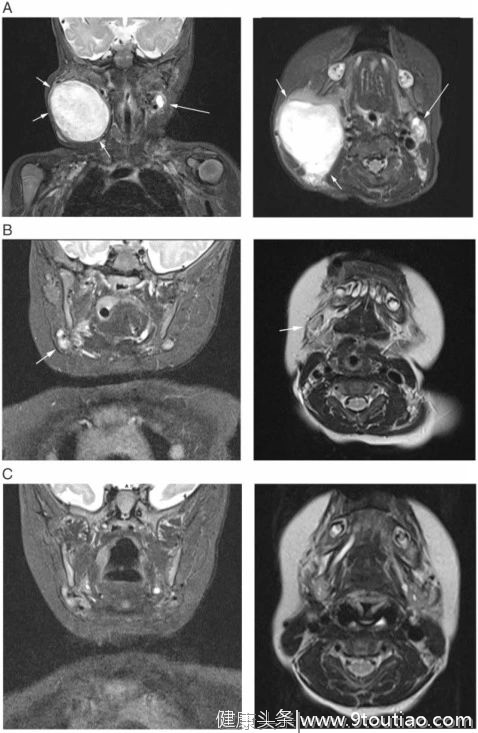
不得不说,M是不幸的,同时M又是幸运的。幸运的是M进行全基因测序发现了NTRK融合基因的存在,并且针对该突变的靶向药拉罗替尼已经问世,所以,幼小的M获得了重生的机会。
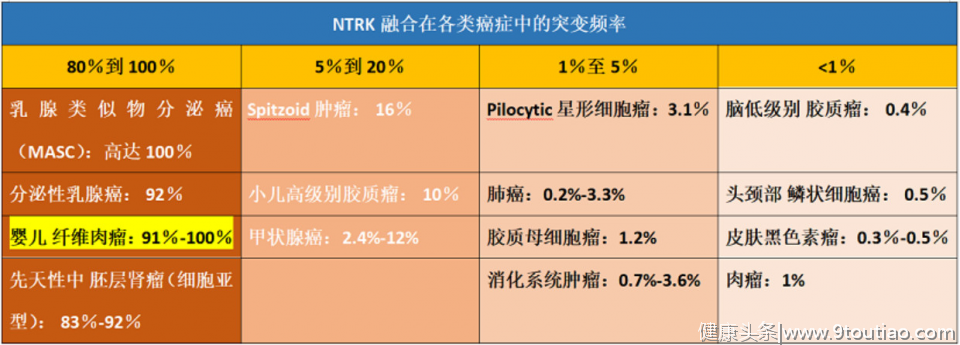
据统计,在91%~100%的婴儿纤维肉瘤中都存在NTRK融合基因,并且,一旦检测结果为阳性,使用拉罗替尼治疗,就有希望达到“治愈”的效果!
所以,我们建议,所有纤维肉瘤儿童家长,一定要为孩子进行基因检测,明确是否存在NTRK基因融合。同时也要提醒大家,融合突变的检测难度很高,基因检测时,千万不要图便宜找小公司检测,一定要找权威专业的大公司使用组织样本分析,以免错失孩子被”治愈“的希望!对此不了解的家长可登录全球肿瘤医生网向专业医生咨询,寻找货真价实、物美价廉的基因检测机构。
另外,虽然拉罗替尼(Larotrectinib,LOXO-101)效果惊艳,但目前该药仅在美国获批上市,并且口服胶囊形式的Larotrectinib采购价格为每月32,800美元(30天100mg),每年393600美元(约270多万人民币)。如此价格,对于患者来说堪称天价。某些儿童患者的口服液体制剂为每月1.1万美元,也是国内普通家庭无法承受的。
好消息是,全球肿瘤医生网小编了解到该药目前已在国内开展临床试验,如能提供符合条件的病例资料就有机会获得免费用药的资格。有相关适应症的患者可登录全球肿瘤医生网咨询详情,我们希望有更多患者获得“治愈”的机会。小编将部分招募信息汇总如下,供大家参考。
成人实体瘤招募信息:
这项研究是为了验证拉罗替尼对不同类型的肿瘤疗效。这些肿瘤必须存在一种特定的基因变化(NTRK1, NTRK2或NTRK3)。Larotrectinib是一种试验性的药物,可以阻止这些NTRK基因在癌细胞中的作用,因此可以用来治疗肿瘤。
试验分期:II期
主要终点指标:由独立放射学审查委员会测定最佳总缓解率
入组人数:总体140人中国13人
预计入组结束时间:中国2021年8月31日

儿童实体瘤招募信息:
本研究是验证拉罗替尼在儿童肿瘤患者中的安全性。该肿瘤必须存在特定(NTRK)基因改变。拉罗替尼旨在限制肿瘤细胞中NTRK基因的活性而治疗肿瘤。研究的第一部分(I期)验证儿童受试者中,剂量的安全性,药物在体内的吸收和改变,对于肿瘤的作用。第二部分(II期)主要目的是药物治疗的作用及其时长。
主要终点指标:1期:受试者发生不良事件的例数,不良事件持续的时间;II期由独立放射学审查委员会测定最佳总缓解率。
入组人数:国际多中心试验:总体159人中国5人
预计入组结束时间:中国2021年11月30日
