康宁杰瑞制药-B(9966.HK):ASCO公布亮眼临床数据,核心双抗构筑业务护城河
近期康宁杰瑞的表现可谓是大放异彩,自4月伊始股价仿佛踏上快车道,开启了近一个月的上涨。股价自低点到近期高位一度上涨154%,即使近期回调以后也较4月初上涨85.61%,大幅跑赢恒生医疗保健指数。追究原因,本轮上涨主要来自于公司在ASCO年会公布的核心在研产品KN046及KN026亮眼的临床数据。
图表一:康宁杰瑞股价近期表现
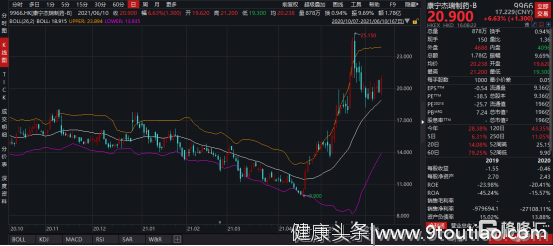
数据来源:WIND,格隆汇整理,数据截至2021年6月10日收盘
KN046:临床数据优势明显,有望创造更优治疗方案
国内多家企业在本次ASCO大会上公布了旗下PD-(L)1双抗的临床数据。其中,康宁杰瑞作为全球PD-(L)1/CTLA-4的双抗开发的领跑者,在本次ASCO大会上发布了三项KN046双抗临床试验结果,表现亮眼。
图表二:康宁杰瑞双抗药物ASCO临床试验数据
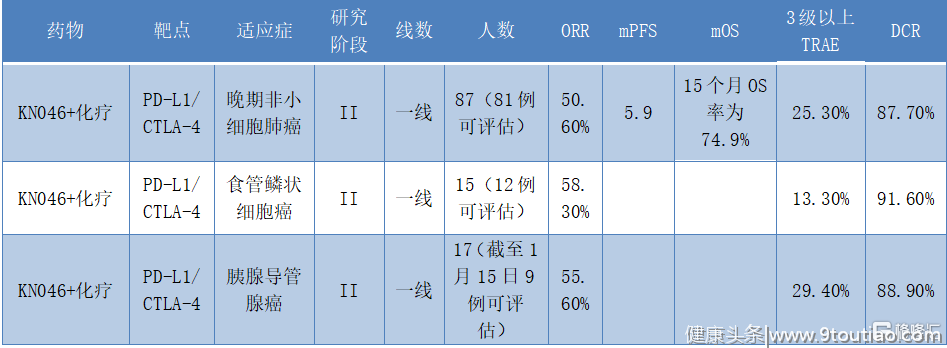
数据来源:ASCO,格隆汇整理
KN046是康宁杰瑞自主研发的全球性首创双特异性抗体,同时靶向 PD-L1及CTLA-4,属于非对称模式全长型双抗,具有明显的结构差异,可改善肿瘤微环境的定位并降低脱靶毒性。具体来看此次公布的临床数据情况:
1. KN046联合化疗治疗晚期非小细胞肺癌Ⅱ期的临床数据
KN046-202是由中山大学附属肿瘤医院张力教授作为主要研究者的临床试验,旨在评估KN046联合铂类化疗用于晚期非小细胞肺癌患者的疗效、安全性和耐受性。
本次试验共入组87例未接受过系统治疗的晚期非小细胞肺癌患者,其中51例非鳞癌患者,36例鳞癌患者。在81例疗效可评估的患者中,客观缓解率为50.6%,疾病控制率达87.7%,其中在鳞状非小细胞肺癌患者中,客观缓解率明显高于非鳞状非小细胞肺癌患者。中位无进展生存期为5.9个月,中位总生存期尚未达到;12个月和15个月的生存率均为74.9%,其中PD-L1 ≥1%的鳞癌患者中位PFS达到10.8个月。
从临床数据来看,KN046联合铂类化疗用于晚期非小细胞肺癌患者从客观缓解率、无进展生存期、总生存期等指标评判展示了良好的有效性和耐受性。针对鳞状非小细胞肺癌患者有更为突出的疗效,总体安全性良好,不良事件可控。
从市场空间来看,根据世界卫生组织国际癌症研究机构(IARC)发布的2020年数据显示,中国在2020年约有82万新发肺癌病例数,约有 71万肺癌导致的死亡人数,肺癌发病率在中国持续增长,其中非小细胞肺癌占肺癌的大多数。
KN046联合铂类化疗在临床上展示出良好的有效性、耐受性及安全性,意味着晚期非小细胞肺癌患者可能获得更优的治疗方案,具有巨大的价值。康宁杰瑞也正在开展KN046联合化疗治疗鳞状非小细胞肺癌Ⅲ期临床研究。
图表三:KN046+化疗治疗非小细胞肺癌临床数据
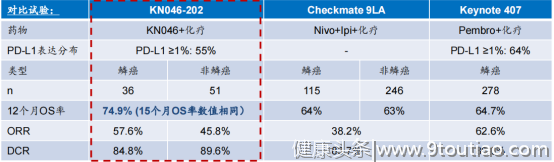
数据来源:公司资料,格隆汇整理
2. KN046联合化疗一线治疗胰腺癌的临床数据
KN046-IST-04是由海军军医大学第一附属医院金钢教授作为主要研究者的临床试验,旨在评估KN046联合白蛋白紫杉醇/吉西他滨作为不可切除的局部晚期或转移性胰腺导管腺癌一线治疗的有效性和安全性。
本次试验入组了17例经组织学或细胞学证实的不可切除局部晚期或转移性胰腺导管腺癌患者,ECOG PS 0-1分,既往未接受过针对不可切除局部晚期或转移性疾病的系统性治疗。其中9例患者接受至少一次肿瘤评估,进入疗效分析数据集,显示客观缓解率为55.6%,疾病控制率为88.9%。治疗相关不良事件(TRAE)发生率为64.7%,3级及以上占29.4%。
从市场空间来看,本次临床试验所治疗的胰腺癌是医学界公认的“癌中之王”,其中约90%的胰腺癌为胰腺导管腺癌(PDAC),发现难、进展快、致死率高,预后极差,病人早期没有明显症状,一旦发现多数已失去手术指征,临床上缺少有效的治疗手段。2015年至2020年,我国胰腺癌新发病例增长31.6%左右,死亡病例增加43.5%左右,患者新发病例与死亡病例几乎持平。
本次KN046联合白蛋白紫杉醇/吉西他滨作为不可切除的局部晚期或转移性胰腺导管腺癌一线治疗展示出高于当前国内外推荐治疗方案一倍以上的客观缓解率,具有极高的有效性,具备巨大的探索价值。根据公司发布的公开信息,这项Ⅱ期临床试验的更新数据将在今年举行的学术会议上发布,更多患者将进入疗效分析数据集。KN046联合化疗一线治疗胰腺癌的Ⅲ期临床研究将在2021年启动。该信息有重要的跟踪价值,有可能带来未来晚期胰腺癌治疗方案的改变。
图表四:KN046联合化疗治疗胰腺癌临床数据
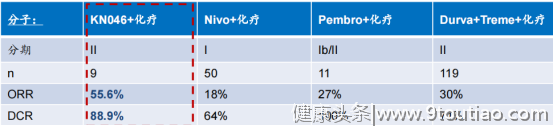
数据来源:公司资料,格隆汇整理
3. KN046联合化疗一线治疗食管鳞癌的Ⅱ期临床数据
KN046-204是由中国人民解放军总医院徐建明教授作为主要研究者的临床试验,旨在评估KN046单药治疗或联合化疗治疗不可切除局部晚期、复发或转移性食管鳞癌的疗效和安全性。康宁杰瑞在ASCO年会上公布了其中一个队列的临床研究结果。
本次公布临床数据的队列入组了15例既往未接受过系统性治疗的,经组织学或细胞学证实的不可切除局部晚期、复发或转移性ESCC患者。12例受试者进入疗效分析数据集,客观缓解率为58.3%,疾病控制率为91.6%。15例受试者进入安全分析数据集,治疗相关不良事件(TRAE)发生率为80.0%,3级及以上占13.3%。输液反应的发生率为7.8%,多为1-2级。免疫治疗相关不良反应(irAE)发生率为53.3%,最常见的≥3级irAE为恶心(1例,6.7%)和皮疹(1例,6.7%)。
从市场空间来看,本次临床试验所治疗的食管癌是全球常见的恶性肿瘤之一,根据世界卫生组织国际癌症研究机构2020年发布的数据显示,我国每年大约有32万食管癌新发病例,占全球食管癌病例的一半,其中约有90%-95%的食管癌患者确诊为鳞癌。食管癌的预后较差,总体5年生存率仅为20%左右,转移性患者的5年生存率仅为3.5%左右。
KN046单药治疗或联合化疗在临床上展示出良好的有效性,治疗相关不良事件发生率较高但大部分为轻度的一二级,严重性不强,安全性处于总体良好的水平。本次试验面向的癌种当前治疗方案预后较差,患者对优化治疗方案的需求亦能推进下一步临床研究的开展。
图表五:KN046联合化疗治疗食管鳞癌的临床数据

数据来源:公司资料,格隆汇整理
KN026:胃癌临床数据公布,安全性良好
此外,康宁杰瑞此次还在ASCO上公布了KN026在晚期HER2阳性胃和胃食管结合部癌的临床数据,整体来看安全性良好。
KN026-202是由中国人民解放军总医院徐建明教授作为主要研究者的临床试验,旨在评估KN026在HER2高表达(HER2阳性)和中低表达两个队列中的疗效。
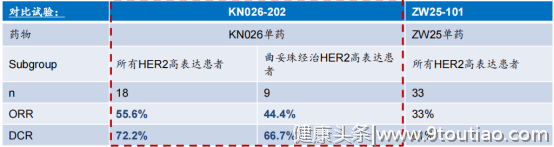
本次公布的入组患者31例,其中20例为HER2高表达,中位治疗时间为20周。在18例可评估的HER2高表达患者中,ORR为55.6%,DCR为72.2%,9个月无进展生存率60.4%,mPFS和mOS尚未达到。在9例既往接受过曲妥珠治疗的受试者中,ORR为44.4%,DCR为66.7%,mPFS为5.6个月,mOS11个月。在安全性上,三四级的KN026有关的TRAE仅为9.7%。
从市场空间上来看,近半数胃癌患者发生在中国,发病率与死亡率远高于全球平均水平,死亡率位列第三。根据2019年国家癌症中心发布数据显示,2015年中国胃癌发病人数约为40.3万人,占恶性肿瘤发病人数的10.26%,仅次于肺癌。由于胃癌早筛诊断率低,中国胃癌患者生存期相对较短,预后更差。根据兴业证券预计,中国胃癌药物市场规模将超过200亿元。
KN026此次公布的临床数据,安全性良好,为胃癌患者带来新的希望。而在联合治疗方向上,KN026+KN046作为全球首个双抗联合疗法,有望开启肿瘤免疫疗法新篇章,为患者提供无化疗肿瘤治疗的新方案。其治疗GC/GEJ已经获得美国FDA孤儿药资格认定,康宁杰瑞也正在进行KN026联合KN046Ⅱ期关键性临床研究(SEARCH-01),计划在20-30家中国和10-20家美国临床研究中心开展,评估KN026联合KN046治疗HER2阳性实体瘤的有效性、安全性和耐受性,其中包括晚期胃及胃食管结合部癌治疗的关键临床研究。
图表六:KN026在晚期HER2阳性胃和胃食管结合部癌的临床数据
数据来源:公司资料,格隆汇整理
长期看点在哪里?
从股价走势上来看,此次ASCO从公布摘要数据开始就引发了康宁杰瑞此轮股价上涨周期,成为短期重磅利好的主要催化剂。而对于康宁杰瑞这个双抗领头羊,长期投资看点在哪里?
首先,双抗市场空间大。相较于单抗以及联合疗法,双抗无论是在疗效、安全性以及成本上均有优势,被称之为“下一代抗体技术”,有望能够填补目前尚未满足的适应症空白,甚至取代部分现有疗法,未来伴随双抗药物逐步上市,市场仍有较大的发展空间。目前,已获批的两款双抗产品(Blincyto以及Hemlibra)自从上市以来的年复合增速分别达到138%和313%,Hemlibra上市三年就突破20亿美元销售额大关,成为当之无愧的重磅品种。
其次,双抗平台构建护城河,具备稀缺性。在双抗研发热度潮中,全球超过150款双抗药物进入临床阶段,其中绝大多数处于临床I期。康宁杰瑞研发的KN046是全球范围内最早进入临床III期的PD-(L)1双抗,在研发进度上处于全球领先水平。双抗的研发难点在于解决生产过程中的随机错配问题,这也造就了双抗技术平台的构建壁垒高。康宁杰瑞是全球少有的拥有自主研发异二聚体双抗技术平台的企业之一,具有稀缺性。
最后,公司产品管线丰富,即将迎来收获期。从研发进程来看,目前公司已经开发了16款创新生物药,产品管线兼具差异化以及创新优势,其中4款产品已经进入Ⅰ-Ⅲ期临床阶段,分别是KN046、KN026、KN035和KN019。按照公司的规划,2021年将会提交2-3项新药IND申请,分别为基于KN026的ADC、PD-L1/OX40 双抗以及新冠双抗中和抗体,研发进展逐步推进,有望保障产品持续上市,增厚公司业绩表现。
从商业化情况来看,2021下半年公司全球首个可皮下注射的PD-L1抑制剂KN035有望获批上市,产品进入收获期,标志着公司从研发过渡到商业化的关键里程碑。管线中还有2款双抗产品及他们的联合疗法处于临床后期阶段,为KN046和KN026,有望于2022年起陆续提交上市,逐步迎来管线收获期。此外,公司将建立核心商业化团队外加增加额外6000L产能,为后续产品商业化保驾护航。
图表七:2021年重要里程碑和催化剂

数据来源:公司资料,格隆汇整理
小结
长远来看,双抗赛道相对于目前竞争激烈的单抗技术,壁垒性高,具备稀缺性,未来发展潜力较大。而作为双抗领域的领头羊,康宁杰瑞此次在ASCO上公布了核心产品多项数据,亮眼的数据也为公司未来研发给予有力支持,产品进度全球领先,将占据先发优势。
从资本市场角度来看,近期公司股价开始打开新一轮的上升通道,来自于对于公司核心产品临床数据表现优异多重利好的逐步兑现,今年下半年公司将会在ESMO、SITC等会议上公布几项主要在研产品管线的临床数据,有望进一步催化公司价值得以提升。
从券商评级情况来看,今年以来,超过5家券商机构给予康宁杰瑞“买入”或“推荐”评级。根据WIND数据统计显示,WIND一致性目标价为29.62港元,距离公司当前股价仍有较大空间,值得关注与期待。
图表八:券商研报评级情况