又一篇Nature!中国科研人员首次揭示癌症致病机理,获国际关注!
2020年12 月24日,国际顶级学术期刊Nature(《自然》)在线发表了北京师范大学生命科学学院王占新实验室与南方科技大学的冷冻电镜中心、美国斯隆凯特琳癌症研究所的Dinshaw Patel实验室以及美国斯坦福大学的Or Gozani实验室合作完成的题为"Molecular basis of nucleosomal H3K36 methylation by NSD methyltransferases"的学术论文,首次揭示了NSD家族组蛋白赖氨酸甲基转移酶修饰核小体的分子机理,并探讨了该家族蛋白突变与人类癌症的关系。
人源NSD家族蛋白包括NSD1、NSD2和NSD3三个成员,都是组蛋白H3第36位赖氨酸的二甲基转移酶。NSD家族蛋白调控染色质结构,是重要的表观遗传调控因子,在高等动物细胞中发挥重要的生理功能,其成员的异常表达或者突变与人类多种癌症相关,比如NSD3与急性白血病和头颈癌等相关,NSD2与人类的多发性骨髓瘤以及Wolf-Hirschhorn综合征等疾病相关,目前还没有针对该家族蛋白的特效药。该工作解析了NSD3和NSD2与核小体复合物较高分辨率的冷冻电镜结构,发现NSD2和NSD3倾向于结合含有linker DNA的核小体。
NSD2或NSD3解离核小体核心颗粒出口或入口处缠绕的DNA,其催化结构域结合在核小体核心组蛋白与解离的DNA之间,通过与核小体DNA和组蛋白一系列位点特异的相互作用得到激活并发挥H3K36位点的甲基转移酶活性。这些与核小体位点特异的相互作用使得NSD蛋白的催化结构域以较为伸展的构象结合在核小体上,使得含有H3K36位点的组蛋白尾巴能够结合在催化位点并激活NSD蛋白。该工作进一步发现几个癌症相关的NSD2和NSD3突变,例如NSD2的E1099K和T1150A突变,以及这两个突变在NSD3中对应的E1181K和T1232A突变,都会分别增强NSD2或NSD3的催化活性,促进癌细胞的增殖并促进移植瘤在裸鼠体内的生长。
结构分析表明NSD2的E1099K突变及其对应的NSD3的E1181K突变虽然远离组蛋白H3的催化位点,但是该突变会通过增强NSD蛋白与核小体DNA的相互作用来增强其催化活性。NSD3的T1232A突变靠近组蛋白H3K36的结合位点,该突变会增强组蛋白尾巴与催化结构域结合的稳定性以增强其催化活性。
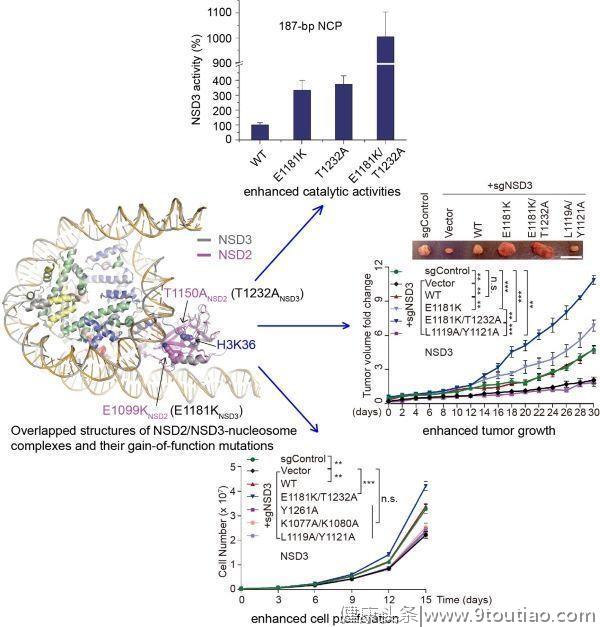
NSD2和NSD3结合核小体的冷冻电镜结构。其中一些致癌突变会增加NSD3的催化活性,增加癌细胞的增殖,并增加裸鼠移植瘤的生长速率。
此项成果首次揭示了NSD家族蛋白以核小体为底物催化组蛋白甲基化的分子机制,以及其癌症相关突变可能致病的分子机理,为进一步理解NSD家族蛋白的生理功能以及靶向NSD家族蛋白的药物研发提供重要分子基础。

该工作由北京师范大学生命科学学院细胞生物学研究所的王占新实验室、南方科技大学的冷冻电镜中心、美国斯隆凯特琳癌症研究所的Dinshaw Patel实验室以及美国斯坦福大学的Or Gozani实验室合作完成。南方科技大学的李婉秋博士、北京师范大学王占新实验室的田伟和邓谱涓博士以及Or Gozani实验室的Gang Yuan(袁刚)博士为本文的共同第一作者。王占新、Dinshaw Patel和Or Gozani为本文的共同通讯作者。生物物理所的李国红老师、北京大学的高宁老师和南方科技大学的龚欣老师为本工作提供了重要帮助。该工作得到了国家自然科学基金、北京师范大学自主基金、南方科技大学和深圳市基金以及美国多项基金的资助。上海蛋白质设施的冷冻电镜中心和南方科技大学的冷冻电镜中心为该工作数据的收集提供了重要支持。
延伸阅读:

王占新,1977年3月出生,博士,教授。2006年-2013年在美国Memorial Sloan-Kettering Cancer Center的结构生物学部做博士后工作,师从美国科学院院士Dinshaw J. Patel教授,研究与癌症相关的重要蛋白质分子的表观遗传学调控机理,在Cell、Nature和Annual Review of Biochemistry等学术期刊上发表论文多篇。2013年初回国担任北京师范大学生命科学学院教授,任职于细胞增殖与调控教育部重点实验室,细胞生物学研究所。通过结构生物学、生物物理生物化学和细胞生物学等方法研究重要蛋白质复合物参与表观遗传调控的分子机理,以及它们的异常与人类癌症的关系。研究的内容包括与白血病相关的蛋白MLL1、AML1-ETO等与修饰的组蛋白或者转录因子相互作用的分子机理,TRIM家族蛋白TRIM24、TRIM33等识别组合的"组蛋白密码"的分子机理以及其异常在癌症生成中的作用,转录延伸因子Paf1复合物的组装及其参与转录调控和表观遗传调控的机理等。通过对这些重要蛋白质复合物结构的精确测定及其在体内功能的分析,以期在原子水平阐明这些生物大分子正常的生理功能及其异常导致癌症的机理。
北京师范大学生命科学学院前身是创办于1904年的京师大学堂博物系,1923年更名为生物学系,1998年扩展为北京师范大学生命科学学院,是中国历史最悠久的生物院系之一。历经百余年的发展与壮大,拥有雄厚的科教实力与师资力量,建立了科学研究和高层次人才培养的卓越地位,培养出一批以秉志、俞德浚、汪堃仁、孙儒泳、王文采、刘瑞玉、郑光美、李蓬八位中国科学院院士和一位美国科学院院士王晓东等为代表的学术大师,以及众多生物教育和其他领域的杰出人才,为生命科学研究和教育事业的发展做出了重要贡献。
学院拥有东北虎豹生物多样性国家野外科学观测研究站,有生物多样性与生态工程教育部重点实验室、细胞增殖及调控生物学教育部重点实验室、基因工程药物及生物技术北京市重点实验室、抗性基因资源与分子发育北京市重点实验室等七个省部级重点实验室(研究中心),创造出了具有国际影响力的科研成果,发表于Nature Cell、Nature Immunology、Nature Communications、PNAS、Ecology Letter、Ecology等一流期刊,近年来获得一项国家自然科学二等奖,两项高等学校科学研究优秀成果奖-自然科学一等奖。
素材来源:北京师范大学