国内MET抑制剂即将上市,为非小细胞肺癌罕见突变患者改写命运
近期,中国国家药品监督管理局为MET抑制剂Savolitinib(沃利替尼)的新药申请授予了优先审查资格,用于治疗具有MET 外显子14跳跃突变(MET ex14)的非小细胞肺癌患者。这意味着,国内首个MET抑制剂的上市之期指日可待,这无疑是一个令人兴奋的消息!
为何这款药物如此受到期待呢?首先我们要了解一下它的上市背景。
01 认识MET突变
MET全称为间质-上皮细胞转化因子(mesenchymal-epithelial transition factor, MET)。
在所有NSCLC中,MET 14 号外显子跳跃突变率为3%-4%,也有国内研究显示其在中国肺腺癌患者中占比仅0.9%;MET拷贝数扩增在肺腺癌中发生率约为1%;而在恶性程度高、预后极差的肺肉瘤样癌(PSC)中,其突变率更是高达 4.9% - 31.8%。
相关研究建议,所有肺癌患者均应进行MET 14外显子跳跃突变检测,因其是一个全新的癌基因靶点,可作为靶向治疗的良好指标。
有研究认为,发生MET 14外显子跳跃突变的患者多年龄较大(在多项研究中患者中位年龄61~72.5岁)且有吸烟史。并且MET 14外显子跳跃突变具有一定的排他性,不与EGFR、KRAS、ALK等其他突变共存,但发生MET 14外显子跳跃突变的患者倾向于同时存在MET基因扩增及MET蛋白过表达。
MET 14外显子跳跃突变的致癌类型以肺癌为主,多为肺腺癌;MET 14外显子跳跃突变不仅是原发致癌驱动基因,也是EGFR-TKI药物出现获得性耐药的原因之一,此类耐药患者的EGFR通路仍活跃,但MET的活化可导致EGFR-TKI耐药。
02 获批MET抑制剂种类较少,国内仍为空白
针对MET突变的靶向药,已获批上市的只有两款,且都为今年新获批药物。
一款是Tepmetko®(Tepotinib,特泊替尼),该药是全球首个获批用于治疗非小细胞肺癌的c-MET选择性抑制剂,率先于2020年3月25日在日本获批应用于MET 14外显子跳跃突变的非小细胞肺癌患者。该批准基于VISION试验,结果显示,Tabrecta治疗非小细胞肺癌患者的客观缓解率为42%,中位缓解持续时间为12个月。
另一款是Tabrecta®(Capmatinib,卡马替尼),该药于2020年5月6日获得FDA批准应用于MET 14外显子跳跃突变的非小细胞肺癌成年患者。这项批准基于GEOMETRY试验,该试验显示,卡马替尼治疗非小细胞肺癌患者的客观缓解率为67.9%,疾病控制率达到96.4%;对于初治患者,中位缓解持续时间为11.14个月,中位无进展生存期达到9.69个月;对于经治患者,中位缓解持续时间为9.72个月,中位无进展生存期为5.42个月。
两款药物虽然效果都不错,但目前均未在国内上市,这极大限制了国内患者用药的便利性,使得国内众多MET突变肺癌患者只能望洋兴叹。
03 Savolitinib(沃利替尼)填补国内空白,堪称“及时雨”
Savolitinib(沃利替尼)的研发成功填补了国内市场的空白,对于国内患者无疑是“及时雨”,这一新型MET抑制剂在临床试验中表现优异。
Ⅱ期试验(NCT02897479)共筛选了597例中国患者,其中87例为MET ex14阳性患者,70例接受了Savolitinib治疗,客观缓解率达到49.2%,中位缓解持续时间达到9.6个月。试验暂未得到整体无进展生存期和总生存期数据,但阶段性中位无进展生存期和总生存期数据已经达到了6.9个月和14.0个月,显著超过其它基因型亚组患者。
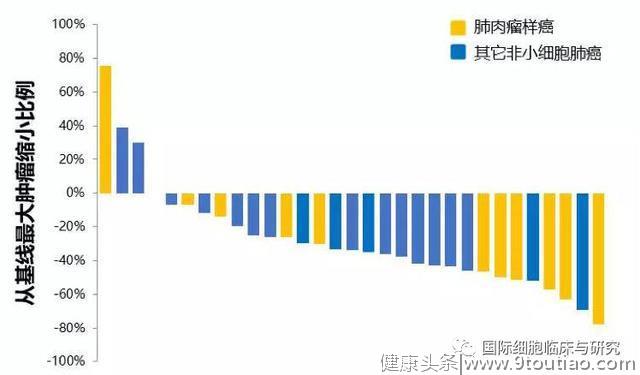
此次试验纳入的患者群体整体年龄较大,中位年龄达到68.7岁。此外,ECOG评分为1分的患者占81.4%,脑转移患者占24.3%,Ⅳ期患者占92.9%,60%的患者曾接受过全身治疗。
基于该试验良好的数据,中国国家药品监督管理局为MET抑制剂Savolitinib的新药申请授予了优先审查资格。该药的获批上市对于国内患者来说可谓是“久旱逢甘霖”,这部分患者终于摆脱了无药可用的困境,意味着很多国内MET突变非小细胞肺癌患者的命运将被改写。
04 国内c-MET抑制剂发展迅速,CBT-101疾病控制率94.4%,成为“后起之秀”
随着国外市场的兴起,国内c-MET抑制剂研发也迅速崛起,另一款MET靶向药伯瑞替尼(PLB-1001,CBT-101)在体外和体内非小细胞肺癌(NSCLC)模型中也展现出优异的活性,在众多在研药物中成为“后起之秀”。
在今年的美国癌症研究协会年会(AACR)报道了伯瑞替尼治疗c-Met 异常的晚期非小细胞肺癌的I期临床试验结果,研究共纳入37例经治但未接受c-Met抑制剂或HGF靶向治疗的局部晚期或转移性晚期非小细胞肺癌患者。
研究结果显示,伯瑞替尼总体耐受性良好,未出现剂量限制性毒性。在36例可评估疗效的患者中,伯瑞替尼的客观缓解率达到30.6%(11/36) ,整体疾病控制率为94.4% (34/36)。
目前,伯瑞替尼的Ⅱ期临床试验已正式开启,患者招募正在进行中,国内患者免费使用c-MET靶向药的机会来了。(国际细胞临床与研究)

至今为止,人类已经发现和研发出了成千上万种药物,在药的帮助下,我们得以战胜疾病,延续生命。研究者通过临床试验获得更新更好的治疗方法。患者可以提前接受未上市的新疗法。接受新药物治疗的患者有可能在临床试验中获得治愈、延长生存或减轻痛苦等疗效,对于现有治疗无效的癌症患者来说,无疑是新的希望。很多癌症患者就是通过参加临床试验,在国内获得了最新的靶向药物。有需要的患者,可以点文末“了解更多”直接登记参加!