人工智能对胃癌的早期诊断(附图)
胃癌是非常常见的恶性肿瘤,发病率和死亡率均很高,胃镜检查可用于检测早期胃癌。然而,早期检测胃癌仍存在不少困难。首先,早期胃癌通常表现出轻微的隆起或凹陷,伴有轻微的红肿,这影响了消化医生的准确识别。其次是难以预测胃癌的浸润深度。理想情况下,分化型,粘膜内胃癌或侵入浅粘膜下层(≤500μm:SM1)的胃癌应在胃镜下切除,而那些侵入粘膜下层(>500μm:SM2)的患者应手术切除,因为存在淋巴结和远处转移的风险。然而,M / SM1与SM2的区别并不容易。目前已有研究借助早期胃癌的特殊成像检测方法以克服这些问题。
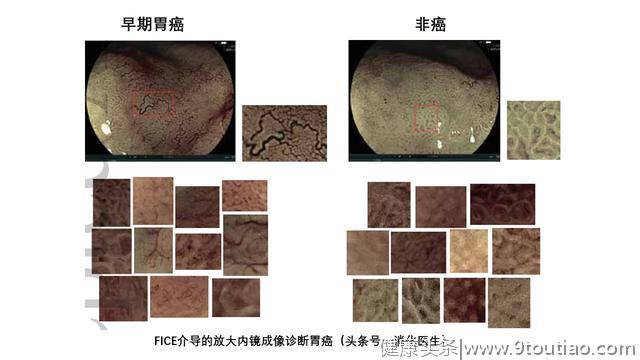
放大内镜结合窄谱成像,如NBI,内镜电子分光图像处理(FICE)技术和蓝色激光成像(BLI)在临床上可用于鉴别癌性区域与非癌性区域,然而,这种光学诊断需要大量的专业知识和经验,这阻碍了它在胃镜检查中的普遍使用。 日本学者开发了自动区分癌症和非癌症区域的软件。作者使用FICE图像技术并使用46个粘膜内胃癌验证模型。对胃癌的诊断准确度为86%,灵敏度为85%和特异性为87%,见下图。
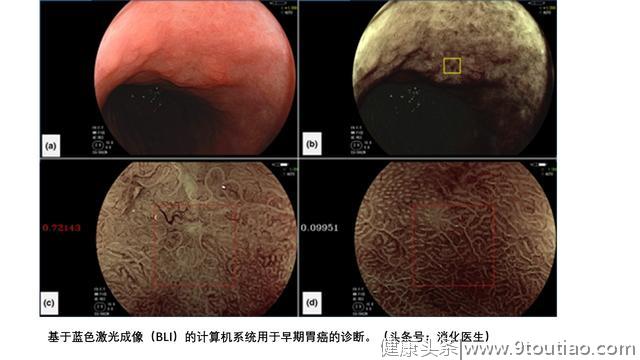
同一组应用类似的BLI技术来放大图像,评估用于BLI的计算机辅助诊断(CAD)系统以识别早期胃癌。作者对100例早期胃癌,以定量验证CAD模型。结果显示,癌变的CAD平均输出值为0.846±0.220,红色病变为0.381±0.349,周围组织为0.219±0.277,癌变的CAD值明显高于其他类别。基于这些发现,研究小组得出结论,自动定量分析可用于鉴别早期胃癌,见下图。(a)早期胃癌的白光图像。 (b)蓝色激光成像(BLI)下的相同病变(黄框)。 (c)放大病变中心的BLI图像。 计算机辅助诊断系统显示该癌症区域的值为0.72143。 (d)放大病变边缘区域的BLI图像。 计算机辅助诊断系统显示该非癌区域的值为0.09951。
日本学者Kanesaka等人的另一项研究推动了这一领域的发展。作者开发的软件不仅可以识别胃癌,还可以描绘癌症和非癌症区域之间的界限。该CAD算法用于分析放大NBI图像的分区像素切片的灰度共生矩阵特征,并且支持用于机器学习方法。该模型区分癌症的诊断性能显示:敏感性为97%和特异性为95%;区域一致性的敏感性为66%和特异性为81%。见下图,放大窄带成像识别和描绘早期胃癌的计算机辅助诊断。早期胃癌的原始放大窄谱图像(左图)。专家描绘的癌性区域用白色虚线表示,计算机辅助诊断描绘的癌性区域显示为黄色块(中图)。计算机检测到的微血管以红色显示(右图)。

2018年,日本学者Hirasawa等人首次报道了使用深度学习技术自动检测早期胃癌。作者的与众不同之处在于他们使用传统的内镜检查图像,而不是将NBI,FICE或BLI放大这些高要求、特殊的检测技术来诊断胃癌。作者使用13 584内镜图像训练网络,并使用从69个连续患有77个胃癌病变的患者中收集的2296个胃图像的测试集来评估其性能。该模型分析2296个测试图像并正确诊断71/77胃癌病变,总体敏感性为92%。这种构建的用于检测胃癌的技术在非常短的时间内处理了许多存储的内镜图像,具有临床相关的诊断能力并且可能在胃镜检查时实时诊断出胃癌。
关于胃癌浸润深度分析,日本学者Kubota等在344例胃癌患者的内镜图像上使用反向传播神经网络算法开发了CAD系统。他们的交叉验证评估显示,T1,T2,T3和T4阶段的诊断准确度分别为77%,49%,51%和55%。 T1亚组分析(粘膜内癌[T1a]和粘膜下浸润癌[T1b])的准确率为69%,这些早癌可通过内镜下微创手术而不是外科手术切除。
转发和分享是一种支持。